 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Лабораторая работа №5
|
|
«Диаграмма состояния сплавов системы железо-углерод»
Цель работы:
- изучение диаграммы состояния железоуглеродистых сплавов;
- анализ превращений, происходящих в сплавах при охлаждениях и нагревах;
- определение фазового и структурного состояния сплавов в зависимости от их состава и температуры.
1. Структуры железоуглеродистых сплавов
Железоуглеродистые сплавы – техническое железо, стали и чугуны – важнейшие металлические сплавы современной техники. Их производство по объему превосходит производство всех других металлов, вместе взятых, более чем в десять раз.
Диаграмма состояния железо – углерод является научной основой технологии черных металлов и дает основное представление о строении важнейших железоуглеродистых сплавов – технического железа, сталей и чугунов.
Структура сплава определяет его свойства. Важно знать, какие фазы и структуры формируются в сплавах в зависимости от их состава и температуры. Необходимо уметь управлять процессом структурообразования для обеспечения эксплуатационных свойств сплавов.
Компонентами железоуглеродистых сплавов являются железо и углерод.
Железо образует с углеродом кинетически устойчивое химическое соединение: цементит – Fe3C. Каждое устойчивое химическое соединение можно рассматривать как компонент. Так как на практике применяют металлические сплавы с содержанием углерода до 5%, то рассматривают часть диаграммы состояния от железа до химического соединения цементита, содержащего 6,67% углерода. Диаграмма состояния железо – цементит представлена на рис. 1.
2. Компоненты и фазы железоуглеродистых сплавов
Компонентами железоуглеродистых сплавов являются железо, углерод и цементит.
1. Железо – переходный металл светло-серебристого цвета. Имеет высокую температуру плавления, равную 1539o ± 5o С.
В твердом состоянии железо может находиться в двух модификациях. Полиморфные превращения происходят при температурах 911oС и 1392oС. При температуре ниже 911oС железо имеет объемноцентрированную кубическую решетку (α–Fe). В интервале температур 911…1392oС устойчивым является железо с гранецентрированной кубической решеткой (γ-Fe). Выше 1392oС железо вновь обретает объемноцентрированную кубическую решетку. Высокотемпературная модификация (именуемая δ-Fe) не представляет собой новой аллотропической формы. Кристаллические решетки железа представлены на рис. 2.
При температуре ниже 768oС железо ферромагнитно, а выше – парамагнитно. Точка Кюри железа, равная 768oС, обозначается А2. Это фазовый переход второго рода.
Железо технической чистоты обладает невысокой твердостью (80 НВ по Бринеллю) и прочностью, но высокими характеристиками
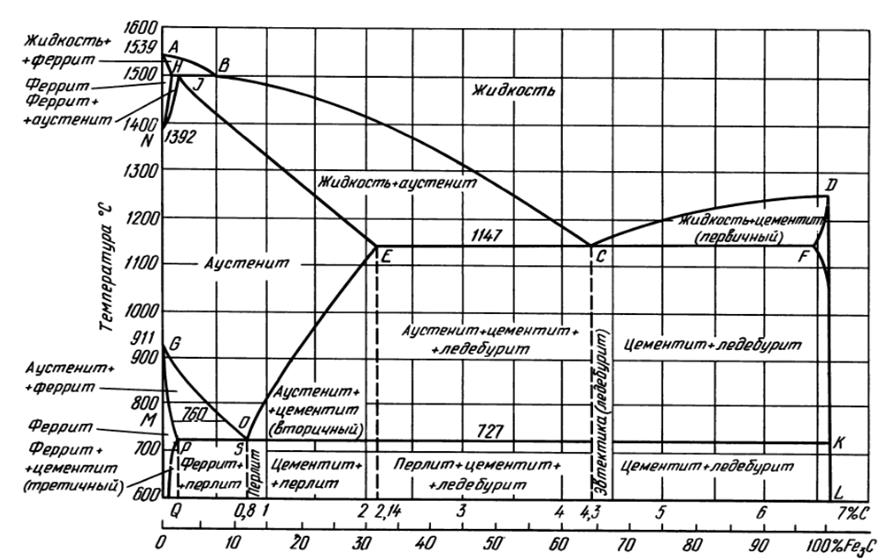
Рис. 1. Диаграмма состояния железо - цементит
пластичности. Свойства могут изменяться в некоторых пределах в зависимости от величины зерна.
Железо со многими элементами образует твердые растворы: с металлами – растворы замещения, с углеродом, азотом и водородом – растворы внедрения.

Рис. 2. Кристаллическая структура железа:
а – гранецентрированная кубическая (ГЦК) ячейка
б – обьемоцентрированная кубическая (ОЦК) ячейка
2. Углерод относится к неметаллам.
В сплавах железа с углеродом углерод находится в состоянии твердого раствора с железом, в виде химического соединения – цементита (Fe3C), а также в свободном состоянии в виде графита (в серых чугунах).
Структура графита слоистая. Он имеет очень низкую прочность, высокие тепло- и электропроводность, малый коэффициент трения. Под действием небольших внешних усилий он расслаивается. Температура плавления 3850 oС.
3. Цементит (Fe3C) – химическое соединение железа с углеродом (карбид железа), содержит 6,67 % углерода. Аллотропических превращений не испытывает.
При низких температурах цементит слабо ферромагнитен, магнитные свойства теряет при температуре около 217oС. Температура плавления 1250 oС.
Цементит имеет высокую твердость (более 800 НВ, легко царапает стекло), но чрезвычайно низкую, практически нулевую, пластичность.
Цементит – соединение неустойчивое (метастабильное) и при определенных условиях распадается с образованием свободного углерода в виде графита. Этот процесс имеет важное практическое значение при структурообразовании чугунов.
На рис. 3 представлена кристаллическая решетка цементита.
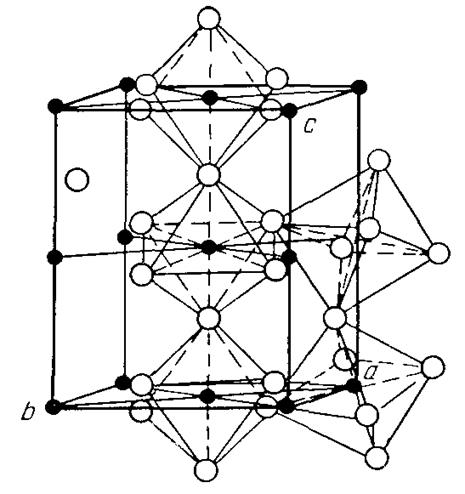
Рис. 3. Элементарная ячейка кристаллической структуры цементита
 - атомы железа,
- атомы железа,  - атомы углерода
- атомы углерода
В системе железо – углерод существуют следующие фазы:
1. жидкая фаза,
2. твердый раствор углерода в α-Fe – феррит (в случае δ-Fe – высокотемпературный феррит Фδ),
3. твердый раствор углерода в γ-Fe – аустенит,
4. химическое соединение – цементит.
Характеристика фаз системы железо – углерод представлена в табл. 1.
3. Процессы при структурообразовании железоуглеродистых сплавов
Каждая точка диаграммы состояния системы железо-цементит характеризует определённый состав сплава при соответствующей температуре (табл.2).
Превращения в сплавах системы Fe–Fe3С происходят как при затвердевании жидкой фазы, так и в твердом состоянии. Первичная кристаллизация идет в интервале температур, ограниченных линией ликвидуса (ABCD) и солидуса (AHJECF) (рис.1).
Линия АВСD – ликвидус системы. На участке АВ начинается кристаллизация феррита высокотемпературного, на участке ВС начинается кристаллизация аустенита, на участке СD – кристаллизация цементита первичного.
Линия AHJECF – солидус, ниже температур, соответствующих этой линии, система находится в твердом состоянии.
Вторичная кристаллизация вызвана превращением железа из одной модификации в другую и переменной растворимостью углерода в
Таблица 1
Фазы системы железо-углерод
| Фаза | Характеристика | Структура |
| Жидкая фаза | В жидком состоянии железо хорошо растворяет углерод в любых пропорциях с образованием однородной жидкой фазы. | - |
| Феррит (Ф) -твердый раствор внедрения углерода в железо с решеткой ОЦК. | Феррит имеет переменную растворимость углерода: минимальную – 0,006 % при комнатной температуре, максимальную – 0,02 % при температуре 727oС (точка P рис.1). Углерод располагается в дефектах решетки. При температуре выше 1392o С существует высокотемпературный феррит Фδ с предельной растворимостью углерода 0,1 % при температуре 1499oС (точка J рис.1). Свойства феррита близки к свойствам железа. Он мягок и пластичен, магнитен до 768o С. | 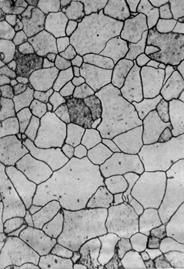
|
| Аустенит (А) – твердый раствор внедрения углерода в железо с решеткой ГЦК. | Углерод занимает место в центре гранецентрированной кубической ячейки. Имеет переменную предельную растворимость углерода: минимальную – 0,8% при 7270С, максимальную – 2,14% при 11470С. Аустенит имеет твердость 200…250 НВ, пластичен, парамагнитен. | 
|
| Цементит | Характеристика представлена выше. | 
|
Таблица 2
Характерные точки диаграммы состояния Fe - Fe3C
| Обозначение точки | Температура, °С | Концентрация углерода, % | Определение точки |
| А | Температура плавления железа | ||
| B | 0,51 | Состав жидкой фазы при перитектической реакции | |
| C | 4,3 | Состав эвтектики ледебурита | |
| H | 0,1 | Состав феррита при перитектической реакции | |
| J | 0,16 | Состав аустенита при перитектической реакции | |
| N | Полиморфное превращение Feα ↔ Feγ | ||
| E | 2,14 | Предельная растворимость углерода в Feγ | |
| D | 6,67 | Температура плавления цементита в Fe3C | |
| G | Полиморфное превращение Feγ ↔ Feα | ||
| P | 0,025 | Предельная растворимость углерода в Feα | |
| S | 0,8 | Состав эвтектоида - перлита | |
| Q | 0,006 | Минимальная растворимость углерода в Feα |
Избыток углерода из твердых растворов выделяется в виде цементита. Линии ES и PQ характеризуют изменение концентрации углерода в аустените и феррите, соответственно. Выделяющийся из жидкости цементит называют первичным, из аустенита – вторичным, из феррита – третичным. Соответственно на диаграмме состояния CD – линия первичного цементита, ES – линия вторичного цементита; PQ – линия третичного цементита. Химические и физические свойства этих фаз одинаковы. Влияние на механические свойства сплавов оказывает различие в размерах, количестве и расположении этих выделений.
Цементит первичный выделяется из жидкой фазы в виде крупных пластинчатых кристаллов. Цементит вторичный выделяется из аустенита и располагается в виде сетки вокруг зерен. Цементит третичный выделяется из феррита и в виде мелких включений располагается у границ ферритных зерен.
Дата публикования: 2015-10-09; Прочитано: 1059 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
