 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Изотермический процесс в химическом реакторе. Режим идеального смешения в проточном реакторе. Сложные реакции
|
|
Здесь рассмотрим только описание процесса и решение уравнение модели для частных реакции первого порядка. Параллельная схема превращения:
А 1 R
2 S
Модель:
(cA – c0)/ τ = -(k1+k2)cA
cR / τ = k1cA
cS / τ = k2cA
Решение:
cA = c0 / [1+(k1+k2)τ]
cR = k1τc0/ [1+(k1+k2)τ]
cS = k2τc0/ [1+(k1+k2)τ]
Последовательная схема превращения: A 1 R 2 S
Модель:
(cA – c0)/ τ =-k1cA
cR / τ = k1cA- k2 cR
cS / τ = k2 cR
Решение:
cA = c0 /(1+k1τ)
cR = k1τc0/ [(1+k1τ)(1+k2τ)]
cS = k1k2τ2c0/ [(1+k1τ)(1+k2τ)]
Качественный характер зависимостей c(τ), влияние на них температуры, а также изменение селективности c(τ) [SR (τ)] будут такими же, как и в режимах идеального вытеснения.
65. Изометрический процесс в химическом реакторе. Режим идеального смешения в проточном реакторе. Простая необратимая реакция A=R.
Математическая модель процесса: 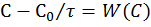 (1)
(1)
Скорость превращения для реакции первого порядка: W(C) = -kC; отсюда (1) принимает вид:  (2)
(2)
Или, переходя к степеням превращения 
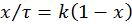 (3)
(3)
Решением (2) и (3) является 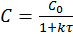 и
и 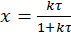 (4)
(4)
Зависимость С( 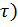 показана на рисунке:
показана на рисунке:
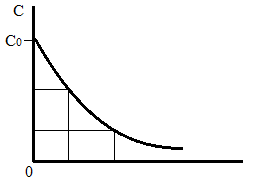
𝜏1 𝜏2 𝜏
Аналитическое решение уравнения (2) относительно С для реакции не первого порядка(кроме n=0,5 и n=2) ограничено.
Удобнее определять необходимое время реакции для достижения заданной концентрации С из (1): 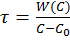 .
.
Интерпретация полученного решения
Для каждого конкретного проточного реактора UC-H условное время  - фиксированная величина. (
- фиксированная величина. (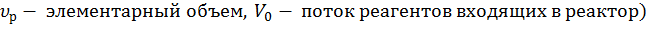
Зависимость С(𝜏), показанная на рисунке есть геометрическое место точек, соответствующих достижению заданных С при 𝜏 характерных для различных реакторов. То есть кривая есть графическое отображение функции (4), и зависимость С(𝜏) есть набор режимов различных реакторов, но не изменение концентрации в одном из них, как это имеет место в реакторах UB и UC-n.
Концентрация вещества в режиме UC-H одинакова во всех точках реактора и равна С, на входе - С0. Это означает, что на входе происходит скачок концентрации от С0 до С. Т.о. распределение концентраций в координатах «С-𝜏» является ступенчатой линией «Высота ступени», равная (С0 - С), для каждого реактора индивидуальна.
На рисунке такие зависимости даны при различных значениях 𝜏, то есть или для реакторов разного объема  , или для одного реактора, работающего при разных нагрузках V0 на него.
, или для одного реактора, работающего при разных нагрузках V0 на него.
66. Изотермический процесс в химическом реакторе. Режим идеального смещения в проточном реакторе. Простая обратимая реакция А↔R.
| (C-C0)/τ = W(C) |
(1)
| X/τ = k1(1-X)−k2X |
, или (2)
| X= k1τ/(1+(k1+ k2) τ) |
(3)
| Х= k1/(k1+ k2) |
, (4)
Что соответствует равновесной степени превращения.
Зависимость Х(τ) имеет вид:

рассматриваемая реакция имеет первый порядок в прямом и обратном направлениях, поэтому начальная концентрация С0 не влияет на степень превращения.
Дата публикования: 2015-10-09; Прочитано: 1265 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
