 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Изотермический процесс в химическом реакторе. Режим идеального смешения, периодического и идеального вытеснения. Сложная реакция с последовательной схемой превращения
|
|
Математическая модель процессов:
 = W(C); С=С0 при
= W(C); С=С0 при 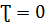 (1)
(1)
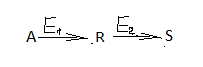 Схема реакции:
Схема реакции:
Процесс описывается системой уравнений (для реакций первого порядка):
∂СА/∂Ʈ=-k1CA; (2)
∂CR/∂Ʈ= k1CA-k2CR;
∂СS/∂Ʈ=k2CR; СА=С0; СR=CS=0 при Ʈ=0.
Решением первого уравнения является:
СA=C0 e -k1Ʈ; (3)
Подставив его во второе уравнение системы (2) получим:
∂CR/∂Ʈ=k1C0 e -k1Ʈ- k2CR; (4) Решением (3) с учетом СR=0 при Ʈ=0 является:
CR=  C0[ e -k1Ʈ- e -k2Ʈ]; (5)
C0[ e -k1Ʈ- e -k2Ʈ]; (5)
Подставляя (4) в третье уравнение системы (1) находим:
CS= С0[1- (k2 e -k1Ʈ- k1 e -k2Ʈ)/(k2-k1)] (6) График зависимостей (3), (5), (6) представлен на рисунке: Изменение концентрации расчетов в реакторе ИВ или ИС-n при последовательном протекании реакции. Сплошные линии построены при температуре Т1 и энергии активации Е1, штриховые при Т2>Т1 и Е1>Е2.  Как видно из рисунка расход в процессе компонента А приводит к уменьшению его концентрации СА. Изменение СR в ходе реакции различно: сначала она возрастает, отражая первый этап схемы А→R→S, затем СА уменьшается, вызывая замедление скорости образования R.
Как видно из рисунка расход в процессе компонента А приводит к уменьшению его концентрации СА. Изменение СR в ходе реакции различно: сначала она возрастает, отражая первый этап схемы А→R→S, затем СА уменьшается, вызывая замедление скорости образования R.
Одновременно накопление R усиливает его дальнейшее превращение в S. В какой-то момент (Ʈmax) скорости образования и расходования R сравниваются и далее R расходуется на образование S, чему соответствует уменьшение СR.
Таким образом в кинетике процесса выделяют следующие этапы: в начале превращения скорость образования S небольшая из-за малого содержания R.
Затем при накоплении определенного количества R, интенсивность образования S возрастает и в конце реакции остается один конечный продукт S.
Таким образом интегральная селективность по промежуточному продукту R уменьшается с глубиной превращения.
Дата публикования: 2015-10-09; Прочитано: 518 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
