 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Неизотермический процесс в химическом реакторе. Режимы идеально смешивания периодического и идеального вытеснения. Анализ процесса
|
|
Математическая модель процесса
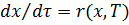
 (1)
(1)
при τ=0 x=xн; T=Tн
где  – адиабатический разогрев;
– адиабатический разогрев; 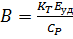 – параметр теплоотвода; Tx – температура теплоносителя, xн и Tн соответственно начальная степень превращения и температура на входе в реактор;
– параметр теплоотвода; Tx – температура теплоносителя, xн и Tн соответственно начальная степень превращения и температура на входе в реактор;
x=(C0-C)/C0. Аналитического решения (1) в общем случае нет.
В адиабатическом режиме B=0 => система (1) принимает вид:
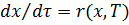 (2)
(2)
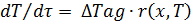 ; при τ=0 x=xн; T=Tн
; при τ=0 x=xн; T=Tн
Разделим второе уравнение системы (2) на первое
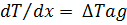 проинтегрируем его в пределах от xн до x и от Tн до T получим: T-Tн=
проинтегрируем его в пределах от xн до x и от Tн до T получим: T-Tн= 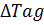 (x-xн) (3)
(x-xн) (3)
Где (T-Tн) – разогрев реакционной смеси до достижения степени превращения x. Если xн = 0, а реакция будет проведена до концы (х=1), то реакционная смесь нагреется на T-Tн= 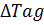 - на величину адиабатического разогрева. Анализируя уравнение 3 делаем вывод, что результат процесса (конечная температура I) зависит от изменения состояния химически реагирующей системы (степени превращения х) и не зависит от пути превращения, от кинетики. Зависимость степени превращения х от темперетуры I для адиабатического процесса в режиме UB дана на рисунке:
- на величину адиабатического разогрева. Анализируя уравнение 3 делаем вывод, что результат процесса (конечная температура I) зависит от изменения состояния химически реагирующей системы (степени превращения х) и не зависит от пути превращения, от кинетики. Зависимость степени превращения х от темперетуры I для адиабатического процесса в режиме UB дана на рисунке:
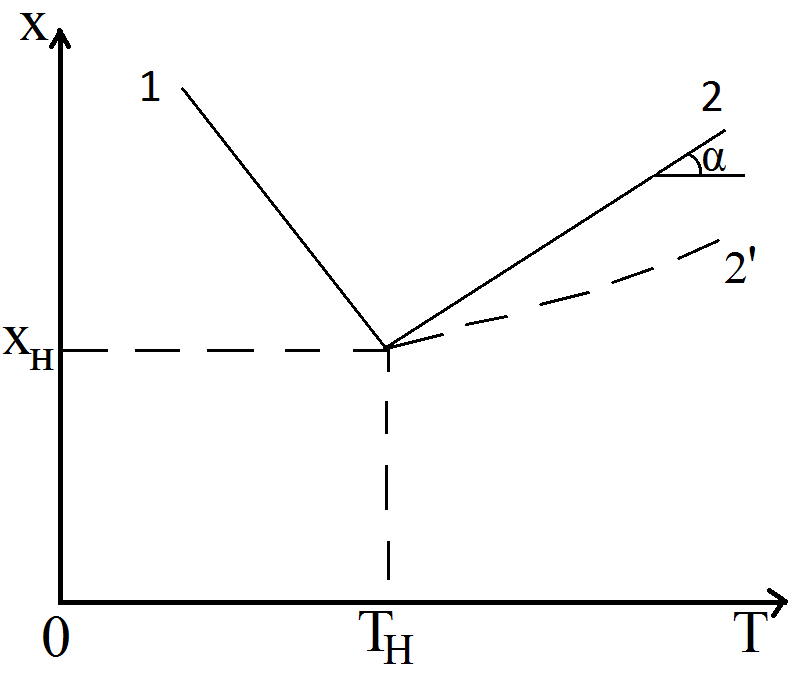 1 – эндотермическая реакция 2, 2' – экзотермическая реакция (сплошная линия соответствует ∆Tag, штриховая - ∆Tag'>∆Tag
1 – эндотермическая реакция 2, 2' – экзотермическая реакция (сплошная линия соответствует ∆Tag, штриховая - ∆Tag'>∆Tag
Зависимость x(T) адиабатического процесса представляет прямую линию с tgα, равным обратной величине адиабатического разогрева: 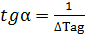 (см (3)), причем для экзотермической реакции наклон положительный (QP>0 и ∆Tag>0), а для эндотермической отрицательный (∆ QP<0 и ∆Tag<0).
(см (3)), причем для экзотермической реакции наклон положительный (QP>0 и ∆Tag>0), а для эндотермической отрицательный (∆ QP<0 и ∆Tag<0).
Чем больше адиабатический разогрев ∆Tag, тем более пологий наклон приобретает зависимость x(T), то есть реакционная смесь будет сильнее разогреваться или охлаждаться.
Протекание реакции сопровождается ростом степени превращения x и увеличением (экзотермическая реакция) или уменьшением (эндотермическая реакция) температуры T. Максимальный разогрев достигается при x=1 и xн=0 и равен ∆Tag
На процесс влияет исходная концентрация, увеличение которой приводит к повышению ∆Tag, и следовательно к ускорению превращения.
Неизотермический процесс в химическом реакторе. Режимы идеального смешения периодический и идеального вытеснения с теплообменом. Сопоставление адиабатического процесса и изотермическим.
Допустим, изотермический процесс осуществляется при температуре адиабатического экзотермического процесса и превышающую ее в эндотермическом процессе. 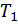 =.
=. 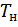 (.
(. 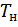 - температура на входе в реактор). В первом случае изотермический процесс будет менее интенсивным, чем адиабатический, а во втором большая степень превращения будет достигаться при меньшем времени реакции.
- температура на входе в реактор). В первом случае изотермический процесс будет менее интенсивным, чем адиабатический, а во втором большая степень превращения будет достигаться при меньшем времени реакции.
Если же температура изотермического процесса.  то интенсивность изотермического процесса будет выше, чем адиабатического, и это будет наблюдаться до тех пор, пока возрастающая в течение реакции температура не достигнет.
то интенсивность изотермического процесса будет выше, чем адиабатического, и это будет наблюдаться до тех пор, пока возрастающая в течение реакции температура не достигнет.  (для экзотермической реакции)
(для экзотермической реакции)
В эндотермическом процессе при  картина будет обратной. Если реакция обратимая, то общий характер зависимости степени превращения Х и температуры Т от
картина будет обратной. Если реакция обратимая, то общий характер зависимости степени превращения Х и температуры Т от 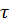 (условного времени реакции сохраняется, с отличием лишь в том, что процесс будет протекать только до равновесной степени превращения
(условного времени реакции сохраняется, с отличием лишь в том, что процесс будет протекать только до равновесной степени превращения 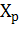 . Тогда максимальный разогрев будет:
. Тогда максимальный разогрев будет:
Т- 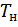 =
= 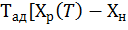 ] (4)
] (4)
Значения максимального разогрева определяют из графика «Т-Х»
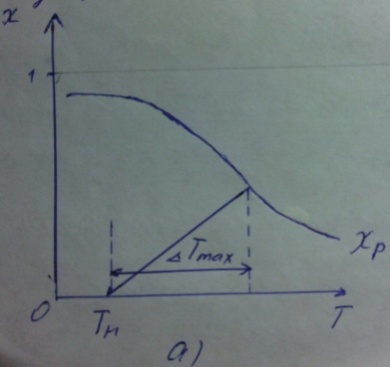
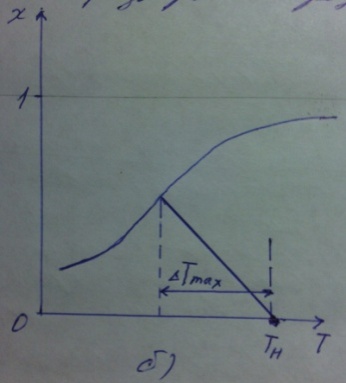
Зависимость 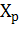 и
и 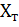 для адиабатического процесса.
для адиабатического процесса.
Определение максимального адиабатического разогрева 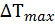 при протекании обратимых а)экзотермической и б) эндотермической реакции
при протекании обратимых а)экзотермической и б) эндотермической реакции 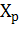 - равновесные степени превращения; прямые – адиабаты в режиме ИВ.
- равновесные степени превращения; прямые – адиабаты в режиме ИВ.
Пересечение кривых зависимостей 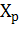 (Т) и Х(Т) адиабатического процесса соответствует максимальному нагреву в слое -
(Т) и Х(Т) адиабатического процесса соответствует максимальному нагреву в слое - 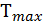 как показано на рисунке а) и б). Интерпритация результатов исследования модели на реальный объект.
как показано на рисунке а) и б). Интерпритация результатов исследования модели на реальный объект.
Исследованная модель описывает процесс в реакторах ИВ и идеального смешения периодическом ИС-п.
В первом случае зависимости Х (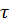 ) и Т(
) и Т(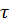 ) (степени превращения и температуры от условного времени реакции) описывают изменение Х и Т по длине реактора, не меняющегося во времени протекания реакции.
) (степени превращения и температуры от условного времени реакции) описывают изменение Х и Т по длине реактора, не меняющегося во времени протекания реакции.
Во – втором изменение во времени Х и Т распределение которых по объему реактора в каждый момент времени одинаковы.
Дата публикования: 2015-10-09; Прочитано: 1524 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
