 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Растворимость белков
|
|
Существует два типа белков – растворимые и нерастворимые в воде или водных растворах солей. При определенных условиях растворимые белки могут формировать осадки, а нерастворимые – образовывать растворы. Процессы растворения и осаждения белков используются в производстве лекарственных препаратов (антител и сывороток), реактивов для диагностики и исследований, пищевых и кормовых добавок, биологически активных добавок к пище, некоторых сортов клея и красок. Некоторые реакции осаждения белков лежат в основе процессов крашения тканей и дубления кожи. Таким образом реакции осаждения белков имеют большое технологическое значение. Также осаждение и растворение белков часто встречается в практике работы научно-исследовательских лабораторий и используется для очистки белков при их выделении и анализе.
Большинство белков хорошо растворимо в воде, что обусловлено наличием на «поверхности» их молекул полярных и заряженных групп, способных связываться с молекулами воды (то есть гидратироваться). Гидратация молекул белка - обязательное условие их растворения. Боковые радикалы некоторых аминокислот, способны диссоциировать в воде и формировать ионные группы, несущие заряд. Заряженные группы белка активно взаимодействуют с молекулами воды за счет ион-дипольных взаимодействий. Боковые радикалы других аминокислот не заряжены, но сильнополярны (-NH2-группа аспарагина и глутамина, - ОН-группа серина и треонина) образуют с молекулами воды водородные связи.
Растворимость белков сильно зависит от условий среды. Растворимые белки при определенных условиях могут терять растворимость и выпадать в осадок. Осаждение белков используют для их выделения и фракционирования, а также получения безбелковых фильтратов в исследовательской и производственной практике.
Чтобы добиться выпадения белка в осадок нужно либо снизить заряд белковых молекул, либо разрушить их гидратную оболочку (дегидратировать).
Реакции осаждения белков делят на две группы:
1) необратимые реакции осаждения, при которых белки претерпевают глубокие изменения и не могут быть снова растворены в первоначальном растворителе.
2) обратимые реакции осаждения, при которых осажденный белок может быть вновь растворен
В первом случае наступает денатурация, т.е. изменение нативной конформации белка сопровождающаяся утратой биологической активности. К необратимым реакциям относится осаждение белка солями тяжелых металлов, алкалоидными реактивами, минеральными и органическими кислотами и осаждение при нагревании. Во втором случае осаждаемые белки не подвергаются глубоким изменениям, молекула белка при этом сохраняет свои первоначальные, нативные, включая биологические, свойства и не подвергается заметной денатурации. К обратимым реакциям осаждения следует отнести осаждение белков органическими растворителями (спиртом и ацетоном) и высаливание белков нейтральными солями.
В качестве отчета о проделанной работе (работы 4.2 - 4.8) заполните таблицу
| Белок | Использованный осадитель и его концентрация | Осадок (есть/нет) | ||
| альбумин | дистиллированная вода | |||
| глобулин | ||||
| альбумин | 5% NaCl | |||
| глобулин | ||||
| альбумин | полунасыщенный раствор (NH4)2SO4 | |||
| глобулин | ||||
| альбумин | насыщенный раствор (NH4)2SO4 | |||
| яичный белок (1%) | нагревание | нейтральная среда | ||
| слабокислая среда | ||||
| сильнокислая среда | ||||
| сильнокислая среда + электролит | ||||
| щелочная среда | ||||
| этанол | ||||
| этанол + NaCl | ||||
| H2SO4 конц. | подслоение | |||
| смешивание | ||||
| НCl конц. | подслоение | |||
| смешивание | ||||
| HNO3 | подслоение | |||
| смешивание | ||||
| трихлоруксусная кислота | ||||
| сульфосалициловая кислота | ||||
| пикриновая кислота | ||||
| танин | ||||
| железосинеродистый калий | ||||
| сульфат меди | ||||
| ацетат свинца | ||||
4.2. Влияние нейтральных солей на растворимость белков
Нейтральные соли (например, Na2SO4, NaCl, (NH4)2SO4) в небольших концентрациях повышают растворимость белков в воде вследствие того, что они увеличивают степень диссоциации ионизированных групп белка и способствуют его гидратации.
Высокие концентрации нейтральных солей, напротив, осаждают (высаливают) белки из водных растворов. При растворении нейтральных солей их ионы конкурируют с молекулами белка за воду, необходимую для формирования гидратных оболочек. Высокая концентрация ионов нейтральных солей «оттягивает к себе» молекулы воды от белка, лишая его гидратной оболочки. Высаливание белков является обратимым процессом. Если удалить соль (при разбавлении водой, путем диализа или другим способом) белок вновь гидратируется. Высаливание часто используется в научно-исследовательской работе при очистке белков или в производстве медицинских препаратов иммуноглобулинов из сыворотки крови.
Ход работы
В пробирку №1 вносят 0,2 мл неразведенного яичного белка и 2 мл воды, содержимое перемешивают. При этом яичный альбумин растворяется, а яичный глобулин выпадает в виде небольшого осадка (или смесь мутнеет).
В пробирку №2 вносят 0,2 мл неразведенного яичного белка и 2 мл 5%-ного раствора хлорида натрия. В слабом солевом растворе растворяются и альбумины и глобулины.
В пробирку №3 наливают 2 мл яичного белка, добавляют равный объем насыщенного раствора сульфата аммония, содержимое перемешивают (получают полунасыщенный раствор сульфата аммония). При этом выпадает осадок яичного глобулина. Через 5 мин осадок отфильтровывают. В фильтрате остается другой белок – яичный альбумин. Для фильтрования раствора белка используют складчатый фильтр из быстрофильтрующей бумаги, который предварительно смачивают небольшим количеством дистиллированной воды.
Для высаливания альбумина к фильтрату добавляют измельченный порошок сульфата аммония до полного насыщения, т.е. пока не прекратится растворение соли. Выпавший осадок альбумина отфильтровывают через новый фильтр и с фильтратом проделывают биуретовую реакцию. Отрицательная биуретовая реакция указывает на отсутствие белка
4.3 Осаждение при нагревании
При температуре выше 50°С почти все белки претерпевают тепловую денатурацию. При этом, на выпадение белков в осадок значительное влияние оказывают присутствие электролитов и рН среды. Наиболее полное и быстрое осаждение происходит в изоэлектрической точке, т.е. при такой величине рН, когда коллоидные частицы белка являются наименее устойчивыми. Поэтому для полного осаждения белка при нагревании следует создать реакцию среды, соответствующую его изоэлектрической точке (белки, обладающие кислыми свойствами, осаждают в слабокислой среде, белки, обладающие щелочными свойствами - в слабощелочной).
В сильнокислых (за исключением азотной, трихлоруксусной и сульфосалициловой кислот) и сильнощелочных растворах денатурированный при нагревании белок не выпадает в осадок, так как частицы белка перезаряжаются (или происходит усиление имеющегося заряда). Они несут в первом случае положительный, во втором случае – отрицательный заряд, что повышает их устойчивость в растворе в результате электростатических сил отталкивания. Однако нагревание в сильнокислых растворах в присутствие достаточного количества какой-либо нейтральной соли белки могут выпадать в осадок.
Ход работы.
В 5 пронумерованных пробирок наливают по 1 мл 1%-ного раствора яичного белка.
Содержимое первой пробирки нагревают на спиртовке. Жидкость мутнеет, но так как частицы денатурированного белка несут заряд, они удерживаются во взвешенном состоянии (яичный альбумин является кислым белком и в нейтральной среде заряжается отрицательно).
В пробирку 2 добавляют 500 мкл 1%-ного раствора уксусной кислоты и нагревают. Выпадает осадок вследствие того, что белок теряет заряд и приближается к изоэлектрическому состоянию.
В пробирку 3 добавляют 100 мкл 10%-ного раствора уксусной кислоты и содержимое нагревают. Осадок белка не образуется, даже при кипячении, так как в сильнокислой среде частицы белка перезаряжаются, приобретая положительный заряд.
В 4 пробирку добавляют 100 мкл 10%-ного раствора уксусной кислоты и 100 мкл насыщенного раствора хлорида натрия. Образуется осадок белка вследствие адсорбции ионов хлорид-иона (образование двойного электрического слоя) и нейтрализации положительного заряда на частицах белка.
в пробирку 5 добавляют 100 мкл 10%-ного раствора гидроксида натрия и нагревают. Осадок белка не образуется даже при кипячении, так как в щелочной среде отрицательный заряд на частице белка усиливается.
Результаты этой и последующих работ раздела «Осаждение белков» вносят в таблицу 7.
4.4 Осаждение органическими растворителями
Белки нерастворимы во многих полярных органических растворителях (спирт, ацетон, и др.). Однако их осаждение происходит только из нейтральных и слабокислых растворов и особенно полно в присутствие электролитов. Органические растворители дегидратируют частицы белка (разрушают водную оболочку) и тем самым понижают их устойчивость в растворе.
Кратковременное воздействие этилового спирта или ацетона не нарушает естественной структуры белка, тогда как продолжительное воздействие приводит к денатурации.
Ход работы:
В пробирку наливают 0,5 мл 1%-ного раствора яичного белка и 2 мл спирта или ацетона. Отметьте наличие/отсутствие осадка
Затем добавить 0,2 мл насыщенного раствора хлорида натрия. Отметьте наличие/отсутствие осадка
4.5 Осаждение концентрированными минеральными кислотами
Осаждение белка под действием минеральных кислот происходит не только вследствие дегидратации и нейтрализации заряда белковых частиц, но и в результате образования солей, денатурации. В избытке серной или соляной кислот, а также при их длительном воздействии выпавший осадок денатурированного белка растворяется, по-видимому, за счет перезарядки белка и частичного гидролиза. В избытке азотной кислоты этого растворения не происходит (точный механизм этого явления не установлен, возможно, что ион NO3- мешает перезарядке белковой молекулы).
Ход работы.
В три пробирки наливают по 15-20 капель концентрированной соляной, серной и азотной кислот. Затем наклонив пробирку под углом 45°, осторожно по стенке пробирки, чтобы жидкости не смешивались (подслоение) налить 1 мл 1%-ного раствора белка. На границе двух слоев жидкости появляется осадок белка в виде тонкой пленки. Осторожно встряхивая пробирки, обнаруживают растворение осадка белка в случае осаждения соляной и серной кислотами, в пробирке с азотной кислотой белок не растворяется
4.6 Осаждение органическими кислотами
Белки из растворов могут осаждаться органическими кислотами, однако различные органические кислоты неодинаково действуют на белок. Трихлоруксусная (CCl3COOH) и сульфосалициловая кислоты (рис. 13) являются чувствительными и специфическими реактивами, вызывающими осаждение белков, и поэтому широко используются для доказательства наличия белка в растворе. Сульфосалициловая кислота осаждает не только белки, но и высокомолекулярные полипептиды.
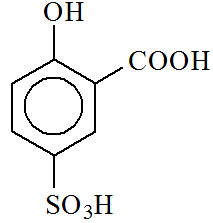
Рис. 13. Сульфосалициловая кислота
Ход работы.
В две пробирки наливают по 0,5 мл 1%-ного раствора белка, в одну пробирку добавляют 200 мкл 10%-ного раствора сульфосалициловой, в другую 200 мкл 10%-ного раствора трихлоруксусной кислоты. Отметьте наличие/отсутствие осадка.
4.7 Осаждение алкалоидными реактивами
Осаждение «алкалоидными» реактивами обусловлено наличием в белке азотистых гетероциклических группировок аналогично тем, которые находятся в молекулах алкалоидов. (Алкалоиды – низкомолекулярные азотосодержащие вещества основного характера, обладающие высокой биологической активностью). Более полное осаждение наблюдается при отрицательном заряде белковой молекулы (например, при достаточном подкислении), что облегчает взаимодействие белка с отрицательно заряженными ионами осадителя.
Ход работы.
В три пробирки наливают по 1 мл 1%-ного раствора яичного белка, и по 200 мкл 1%-ного раствора уксусной кислоты. Затем в первую пробирку приливают 200 мкл 10%-ного раствора пикриновой кислоты (рис. 14), во вторую 200 мкл насыщенного раствора танина, в третью – 200 мкл 5%-ного раствора железосинеродистого калия. Отмечают образование осадка.
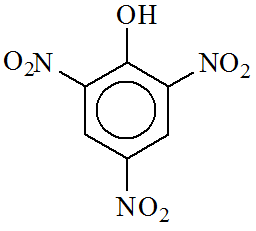
Рис. 14. Пикриновая кислота
4.8 Осаждение солями тяжелых металлов
При действии солей тяжелых металлов на растворы белка происходит денатурация белковой молекулы. Осаждение денатурированного белка обусловлено адсорбцией тяжелого металла на поверхности белковой молекулы и образованием нерастворимых комплексов. При осаждении белков некоторыми солями тяжелых металлов, например, уксуснокислым свинцом и сульфатом меди, избыток этих солей ведет к растворению (пептизации) первоначально образовавшегося осадка, что связано с адсорбцией тяжелого металла на поверхности коллоидных частиц и появлением положительного заряда на молекуле белка. При избытке солей серебра и ртути пептизация осадка не происходит.
Ход работы
В две пробирки вносят по 0,5 мл 1%-ного раствора яичного белка и по 100 мкл: в первую пробирку – 7%-ного раствора сульфата меди, во вторую 5%-ного раствора уксуснокислого свинца. Во всех пробирках образуется осадок.
В первую пробирку добавляют еще 0,5-1 мл 7%-ного раствора сульфата меди, при этом наблюдается растворение осадка.
Вопросы для самоподготовки
В чем суть процесса диализа?
Каково практическое значение диализа?
Каково практическое значение процессов осаждения растворения белков?
Какие два условия необходимо выполнить для осаждения белка?
Что такое обратимые и необратимые реакции осаждения?
Что происходит при необратимом осаждении белка?
Какие обратимые реакции осаждения вы знаете?
Какие необратимые реакции осаждения вам известны?
Что происходит с молекулами белков при высаливании и осаждении органическими растворителями?
Дата публикования: 2015-09-17; Прочитано: 6627 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
