 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Криолит-алюминий тотығы балқымаларын электролиздеу кезіндегі ток пен энергияның шығымдары
|
|
Фарадей заңына сүйенсек алюминий баламасының молярлық массасын бөлу үшін, (27/3=9 г/моль), электролит арқылы 26,8 ампер сағат электр қуатын өткізу керек, яғни теория жүзінде бір ампер сағат электр қуаты 0,335 грамм алюминиді бөліп шығаруы керек. Іс жүзінде электр тоғының бір бөлігі алюминиді бөліп шығару үшін жұмсалмай, басқа жанама процестерге (электр тоғының кемуі, алюминидің электролиз өнімдерімен қайта әрекеттесуі ж.т.с.с) жұмсалады, сол себептен бөлініп алынған алюминидің мөлшері әруақытта теориялық көрсеткіштен кем болып келеді.
Іс жүзінде бөлініп алынған алюминий мөлшерінің ( qіс), Фарадей заңы бойынша бөлінуі керек болатын алюминий мөлшеріне (qт) бір мөлшердегі электр қуатымен қатынасын токтың шығуы деп атайды, ηш
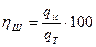 (4.7)
(4.7)
кәдімгі жағдайда ηш = 85-90%, немесе
 (4.8)
(4.8)
Ал энергияның шығуы
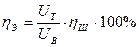 , (4.9)
, (4.9)
мұндағы UТ – өндірістік жағдайдағы электр қозғауыш күшінің
(э.қ.к) үйектеулігі, (яғни үйектелмеген және
кернеу күшінің шамадан тыс артуын есепке
алғандағы кернеу ыдырауы) шамамен 1,6 В тең;
UВ – астаудың кернеуі, 4,5-5,0 В тең.
Егер ηш = 0,85 болып, және Uв= 4,5 В, онда
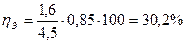 (4.10)
(4.10)
Энергия бірлігіндегі алюминидің теориялық шығымы мынадай
 , г/квт сағат (4.11)
, г/квт сағат (4.11)
мұндағы С – алюминий баламасының молярлық массасы;
J – тоқтың күші;
τ – электролиз процесінің ұзақтығы, сағат;
UТ – электр қозғаушы күшінің (э.қ.к) үйектелуі.
Энергия бірлігіндегі алюминидің іс жүзінде өндірістегі шығымы мынадай
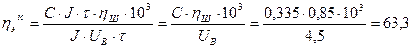 г/квт сағат (4.12)
г/квт сағат (4.12)
Осы теңдеуден көріп отырғанымыздай астауға келетін электр қуатының тек 1/3 бөлігі ғана электрохимиялық процеске жұмсалып, ал қалған 2/3 бөлігі электролиз процесіне қажетті 950-960 оС температураны ұстап тұруға және токтың кемуі мен басқа жансақ химиялық әрекеттесулерге жұмсалып шығындалады.
Токтың шығымы электролиз температурасы, токтың тығыздығы, электродтардың арақашықтықтары және электролиттің құрамы сияқты маңызды факторларға тәуелді. Енді осы факторларға жеке-жеке қысқаша тоқталып өтейік:
1) температураның әсері. Температура жоғарлағанда алынған алюминий мен электролиттің өзара әрекетесу реакцияларының жүру уақытының ұзаруының салдарынан, токтың шығымы төмендейді

 2Al +AlF3 3AlF (4.13)
2Al +AlF3 3AlF (4.13)
Бұл реакция криолиттік қатынас 3 санынан кем болғанда жүреді, ал криолиттік қатынас 3 санынан артық болғанда мынадай реакция жүреді
 Al + 3NaF AlF3 + 3Na (4.14)
Al + 3NaF AlF3 + 3Na (4.14)
Бірақ теператураның тым төмендеп кетуі, балқыманың тұтқырлығының жоғарлауына және металл мен электролиттің бөліну жағдайларының нашарлауына байланысты токтың шығымын төмендетеді;
2) токтың тығыздығының әсері. Токтың катодтық тығыздығы артқан сайын токтың да шығымы артады. Егер катодтық токтың тығыздығы шамадан тыс артып кетсе, катодқа басқа металдың иондары қонуы мүмкін, мысалы натридің иондары, сонымен бірге токтың катодтық тығыздығы тым төмендеп кетсе де жоғарыдығы жағдай қайталанылады;
3) полюсаралық қашықтықтың әсері (анод пен балқыманың беткі қабатындағы металдың, яғни катодтың қашықтығы).
Полюсаралық қашықтықтың артуымен токтың шығымы да артады, өйткені электролиттегі еріген алюминидің анод кеңістігіне түсу мүмкіндігі төмендейді, демек оның тотығуы мен жоғалымы да азаяды.
Кәдімгі жағдайда электролиздеу процесі кезінде полюсаралық қашықтық L=5-7см тең, бірақ токтың катодтық тығыздығы мен d және L көрсеткіштерінің шамадан артық өсіп кетуі астаудың кенеуінің өсуіне мәжбір етеді.
Астаудың кернеуі токөткізгіш жүйелерді есепке алмағанда төмендегідей қосындылардан тұрады
 , (4.15)
, (4.15)
мұндағы UТ – электр қозғауыш күшінің (э.қ.к) үйектелуі;
ρ – электролиттің меншікті кедергісі, Ом/см3;
d – токтың орташа тығыздығы,
L – полюсаралық қашықтық, см.
Бұл теңдеуден астаудың кернеу көрсеткіші электролиттегі d мен L сәйкес екендігі көрініп тұр. Полюсаралық қашықтықтың артуы астаудың кернеуін өсіріп, металл бірлігінде электрэнергиясының шығынына артырады, сонымен қатар полюсаралық қашықтықтың ұлғаюы астаудың температурасын жоғарлатып, алюминидің жоғалымдарын көбейтеді.
Сондықтан токтың тығыздығы мен полюсаралық қашықтықтығының ықшамды көрсеткіштерін тауып алу өндірісте өте маңызды;
4) ток бойынша металл шығымының жоғарғы көрсеткіші криолиттік қатынастың (NaF:AlF3 моль)=2,6-2,8 сандарының аралығында.
Осындай құрамды электролитте натрий иондарының катодта өріс алу мүмкіндігі төмендеп, алюминидің электролитте еруіне байланысты оның жоғалымы азайады және электролиттің температурасы мен тығыздығы біршама төмендейді. CaF2 және MgF2- тұздарының әсерінен электролиттің тығыздығы жоғарлайтын болса, оған Al2O3 қосу арқылы тығыздықты орынына келтіріп отырады. Электролиттің электрөткізгіштігінің кемуі CaF2 және MgF2- тұздарының әсерінен аса көп емес, бірақ электролиттің жеңіл балқуының артуы электролиздің температурасын төмендетуге мүмкіндік туғызады. Бұл фактор токтың шығымына қолайлы жағдай жасайды.
Алюминиден жасалған өндірістік астаулардың ток шығымына электролит пен металдың астаудағы деңгейі мен көлемі, және астаудың жұмыс кеңістігінің пішіні сияқты технологиялық факторлар елеулі әсер етеді.
Дата публикования: 2015-07-22; Прочитано: 633 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
