 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Растворы неэлектролитов
|
|
Вопросы для самопроверки
1. Что такое раствор? В чем отличие растворов от химических соединений?
2. Рассчитайте процентную, молярную и моляльную концентрации раствора, полученного смешением 1 г NaC1 и 100 г H 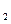 O (плотность раствора примите равной 1).
O (плотность раствора примите равной 1).
3. Укажите возможные виды взаимодействия между компонентами в растворе.
4. В чем сущность физической теории растворов? В чем ее отличие от сольватной теории?
5. Что называется осмосом? Каков его механизм? Каково его биологическое значение?
6. В чем выражается аналогия между осмотическим давлением и давлением газов?
7. Какие растворы называются изотоничными? гипертоническими? гипотоническими? Рассчитайте процентную концентрацию раствора глюкозы, изотоничного с кровью (осмотическое давление крови равно 7,3 атм., плотность раствора примите равной 1)..
8. Используя кривые зависимости (давление водяных паров - температура для воды, водных растворов и льда), поясните, почему растворы замерзают при более высокой температуре, чем вода.
9. На основе представлений об осмотическом давлении поясните, почему растения не могут существовать на засоленных почвах.
10. Какой из трех приведенных растворов замерзает при более низкой температуре: содержащий в 1 л воды 18 г глюкозы, 18 г формальдегида или 18 г поваренной соли? Дайте ответ, не вычисляя значений температур замерзания.
11. Что такое криоскопия? эбулиоскопия? Рассчитайте молекулярную массу моносахарида, если при растворении 1,8 г его в 1 л воды температура замерзания полученного раствора понизилась на 0,186 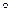 .
.
Решение типовых задач
1. Вычислить осмотическое давление раствора глицерина, содержащего 0,46 г глицерина в 100 мл раствора при 20 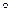 С.
С.
Решение. По закону Вант-Гоффа Росм= CRT,
где С - концентрация вещества в молях на литр раствора
(молярная);
R - универсальная газовая постоянная R=8,31 
Т - абсолютная температура;
Росм - осмотическое давление раствора.
Молярная концентрация С определяется из соотношения:
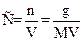 ,
,
где n - число молей растворенного вещества в данном объеме раствора;
g - вес растворенного вещества в граммах:
V - объем раствора в литрах;
М - молекулярная масса растворенного вещества.
Тогда:
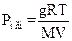 ,
, 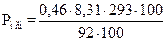 .
.
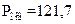 Па=1,2 атм
Па=1,2 атм
2. Раствор, содержащий 0,48 г глицерина на 25 г воды, замерзает при температуре -0,387  С. Вычислить молекvлярную массу глицерина и осмотическое давление раствора при 0
С. Вычислить молекvлярную массу глицерина и осмотическое давление раствора при 0  С.
С.
Решение.
а) Определение молекулярного веса глицерина.
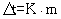
где К – криоскопическая константа, равная для водных растворов 1,86 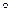 С;
С;
m – моляльная концентрация (моль/1000 г растворителя);
 ,
,
где p – вес растворенного вещества в граммах;
W – вес растворителя в граммах;
M – молекулярная масса вещества;
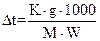 ,
, 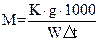 ,
,
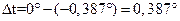 ,
,
 , M = 92.
, M = 92.
б) Определение осмотического давления.
Осмотическое давление раствора вычисляется с помощью уравнений:
Pосм=CRT и 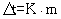 ,
,
Для разбавленных водных растворов 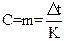 ,
,
 ,
,
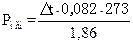 ,
, 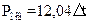 ,
,
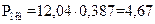 атм.
атм.
ЗАДАЧИ ДЛЯ КОНТРОЛЬНОЙ РАБОТЫ
71-80. Для приведенных ниже растворов рассчитайте осмотическое давление при 20°С и молекулярную массу растворенного вещества (среднюю для биологических объектов), руководствуясь данными таблицы:
Дата публикования: 2015-07-22; Прочитано: 835 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
