 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Алканы. Циклоалканы
|
|
Алканы (парафины) – это соединения углерода с водородом, в молекулах которых атомы углерода соединены между собой одинарной связью (предельные углеводороды). Общая формула гомологического ряда алканов СnН2n+2. Радикал, получающийся при отрыве одного атома водорода от молекулы предельного углеводорода, называется алкилож, общая формула алкилов СnН2n+1.
Формулы и названия первых шести алканов (С1–С6) и отвечающих им радикалов:

Для радикала С5Н11 использование названия амил не рекомендуется. Для составления названий алканов с разветвленной цепью, например
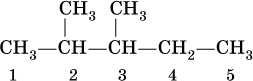
выбирают самую длинную углеродную цепь (в примере – 5 атомов) и получают основу названия (5 – пентан). Нумеруют цепь (от 1 до 5) так, чтобы заместители (–СН3) получили наименьшие номера (2 и 3). В названии арабскими цифрами указывают положение заместителей, а приставками ди – 2, три – 3, тетра – 4 и т. д. – число одинаковых заместителей. Таким образом, в нашем примере алкан должен быть назван 2,3‑диметилпентан.
При наличии разных заместителей их названия расставляют по алфавиту, т. е., например, сначала метил, а затем этил.
Для некоторых разветвленных предельных углеводородов используются, наравне с систематическими, традиционные названия, например, для алканов состава С4Н10и С5Н12 с формулами:

Такие же названия используются для разветвленных радикалов:

При обычных условиях первые алканы – метан, этан, пропан и бутан (С1–С4) – представляют собой газы без цвета и запаха, малорастворимые в воде. Последующие гомологи (С5–C15) – жидкости (при 20 °C), высшие гомологи (C16 и выше) – твердые вещества.
В алканах атомные орбитали углерода имеют sр3‑гибридизацию; четыре электронных облака атома углерода направлены в вершины тетраэдра под углами 109,5°. Ковалентные связи, образуемые каждым атомом углерода, в алканах малополярны.
Поэтому алканы – сравнительно инертные вещества, вступают только в реакции замещения, протекающие с симметричным (радикальным) разрывом связей С – Н. Эти реакции обычно идут в жестких условиях (высокая температура, освещение). В результате становится возможным замещение водорода на галоген (CI, Br) и нитрогруппу (NO2), например, при обработке метана хлором:

Вторая и последующие стадии реакции протекают легче, чем первая, из‑за смещения электронной плотности к атому хлора:

и увеличения подвижности остающихся атомов водорода. Названия продуктов: СН3Cl – хлорметан, СН2Cl2 – дихлорметан, СНCl3 – трихлорметан (хлороформ), СCl4 – тетрахлорметан (тетрахлорид углерода).
В тех алканах, где кроме первичных есть также вторичные и третичные атомы углерода, замещение обычно протекает с образованием смеси однозамещенных продуктов (т. е. в каждой молекуле замещается один атом водорода), например:

Циклоалканы – предельные углеводороды циклического строения, общая формула гомологического ряда СnH2n(п 
3), формула совпадает с таковой для алкенов. Важнейшие циклоалканы:

При комнатной температуре С5Н10 и С6Н12 – бесцветные жидкости, малорастворимые в воде. Химические свойства циклоалканов подобны свойствам алканов, например:

Получение: источниками алканов и циклоалканов в промышленности служат нефть, природный газ, каменный уголь. В лаборатории применяют такие способы синтеза алканов:
1) реакция Вюрца – действие натрия на галогенпроизводные углеводородов:

2) каталитическое гидрирование этиленовых углеводородов (катализаторы Pt, Pd, Ni):
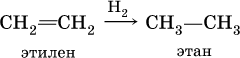
3) сплавление солей карбоновых кислот с гидроксидом натрия:

Циклоалканы синтезируют из дигалогенпроизводных алканов:

Алканы широко используются как исходное сырье в химической промышленности, моторное топливо (бензин, керосин и др.); циклоалканы применяются в органическом синтезе.
При горении метана выделяется много теплоты:

Поэтому его (в виде природного газа) применяют в качестве топлива в быту и в промышленности.
Дата публикования: 2014-11-04; Прочитано: 5870 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
