 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Кислотно-основные свойства аминокислот
|
|
α-Аминокислоты в силу своего химического строения проявляют кислотно-основные (амфотерные) свойства, которые определяют многие физико-химические и биологические свойства белков. На этих свойствах основаны, почти все методы выделения и идентификации аминокислот и белков.
При нейтральном значении рН аминокислоты в растворах находятся в виде биполярного иона (цвиттер-иона), при этом аминогруппа протонирована (-NH3+), а карбоксильная группа - диссоциирована (-СОО-):
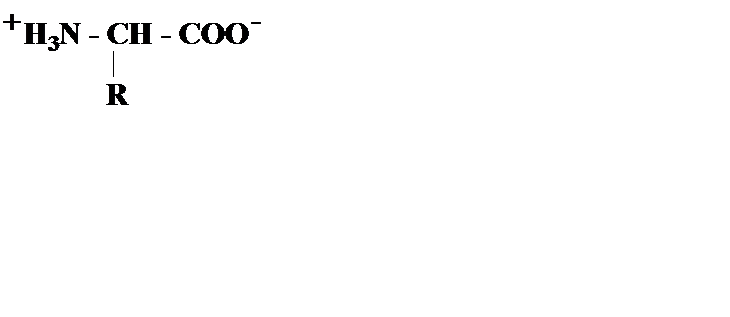
| (рН ≈7) |
Ионизация аминокислоты зависит от рН среды: в кислых растворах ионизирована аминогруппа, а в щелочных - карбоксильная группа:
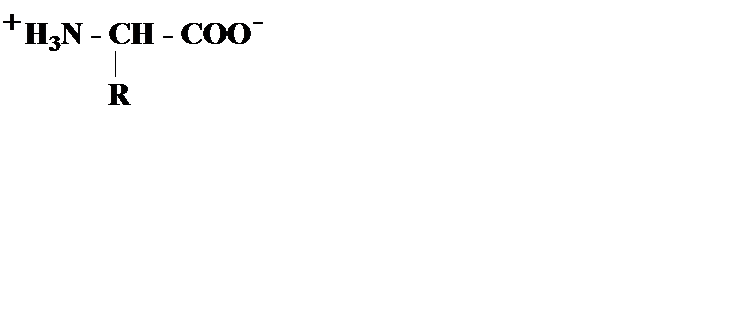
| 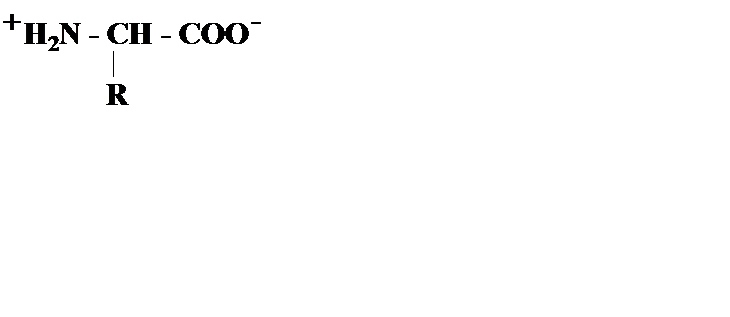
|
| (рН=1) | (рН=11) |
В кислой среде α-аминокислоты выступают как основания (по аминогруппе), а в щелочной - как кислоты (по карбоксильной группе). У некоторых аминокислот может ионизироваться также радикал (R), в связи, с чем все аминокислоты можно разделить на заряженные и незаряженные (при физиологическом значении рН=6,0 - 8,0) (см. табл. 4). В качестве примера первых можно привести аспарагиновую кислоту и лизин:

| 
|
| Аспарагиновая кислота (отрицательно заряженная кислота, проявляет кислотные свойства) | Лизин (положительно заряженная кислота, проявляет основные свойства) |
Если радикалы аминокислот нейтральные, то они не оказывают влияния на диссоциацию α-карбоксильной или α-аминогруппы, и величинырК (отрицательный логарифм, показывающий значение рН, при котором эти группы наполовину диссоциированы) остаются относительно постоянными.
Величины рК для α-карбоксилыюй (pK1) и α-аминогруппы (рК2) сильно различаются. При рН < pK1 почти все молекулы аминокислоты протежированы и заряжены положительно. Напротив, при рН > рК2 практически все молекулы аминокислоты являются отрицательно заряженными, так как α-карбоксильная группа находится в диссоциированном состоянии.
Следовательно, в зависимости от рН среды аминокислоты имеют суммарный нулевой положительный или отрицательный заряд. Значение рН, при котором суммарный заряд молекулы равен нулю, и она не перемещается в электрическом поле ни к катоду, ни к аноду, называется изоэлектрической точкой и обозначается pI.
Для нейтральных α-аминокислот значение pI находят как среднее арифметическое между двумя значениями рК:

При рН раствора меньше pI аминокислоты протонируются и, заряжаясь положительно, перемещаются в электрическом поле к катоду. Обратная картина наблюдается при рН > pI.
Для аминокислот, содержащих заряженные (кислотные или основные) радикалы, изоэлектрическая точка зависит от кислотности или основности этих радикалов и их рК (рК3). Значение pI для них находят по следующим формулам:
для кислых аминокислот:

для основных аминокислот:

В клетках и межклеточной жидкости организма человека и животных рН среды близко к нейтральному, поэтому основные аминокислоты (лизин, аргинин) имеют положительный заряд (катионы), кислые аминокислоты (аспарагиновая, глутаминовая) имеют отрицательный заряд (анионы), а остальные существуют в виде биполярного цвиттер-иона.
Дата публикования: 2015-11-01; Прочитано: 5899 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
