 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Реакции электрофильного присоединения к несимметричным алкенам
|
|
Когда мы рассматривали реакцию гидрогалогенирования или гидратации на примере этена, у нас не возникало вопроса к какому из атомов углерода при двойной связи присоединится протон водорода на стадии образования σ-комплекса: в молекуле этена (и других симметричных алкенов) оба углерода при двойной связи равноценны. В случае же этих реакций в несимметричных алкенах возможно образование двух продуктов присоединения, а значит, возникает проблема: какой из них будет преобладающим. Рассмотрим это на примере гидрохлорирования пропена:
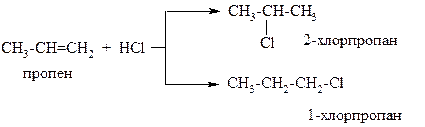 |
Теоретически, в реакции гидрохлорирования пропена могут образоваться 1-хлорпропан и 2-хлорпропан, однако на практике в основном получается 2-хлорпропан. Эта реакция протекает по правилу Марковникова: при присоединении реагентов типа H+X- (например, HCl, HBr, HOH) к несимметричным алкенам протон водорода присоединяется к более гидрогенизированному атому углерода при двойной связи.
Чтобы объяснить такой порядок присоединения, необходимо рассмотреть статический и динамический факторы.
Статический фактор – это распределение электронной плотности в нереагирующей молекуле.
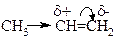 Атом углерода при двойной связи sp2-гибридизован, он более электроотрицателен, чем sp3-гибридизованный углерод метильной группы. Поэтому электронная плотность связи CH3-CH= смещена к углероду с двойной связью. Так как π-связь поляризуется легче, чем σ-связь, электроны π-связи смещаются к соседнему атому углерода, т.е. происходит её поляризация. В конечном итоге на первом атоме углерода возникает частичный отрицательный заряд (δ-), а на втором – частичный положительный (δ+). Конечно же, протон водорода (положительно заряженная частица) будет направляться к тому углероду, где есть избыток электронной плотности, а он и есть более гидрогенизированный атом углерода при двойной связи.
Атом углерода при двойной связи sp2-гибридизован, он более электроотрицателен, чем sp3-гибридизованный углерод метильной группы. Поэтому электронная плотность связи CH3-CH= смещена к углероду с двойной связью. Так как π-связь поляризуется легче, чем σ-связь, электроны π-связи смещаются к соседнему атому углерода, т.е. происходит её поляризация. В конечном итоге на первом атоме углерода возникает частичный отрицательный заряд (δ-), а на втором – частичный положительный (δ+). Конечно же, протон водорода (положительно заряженная частица) будет направляться к тому углероду, где есть избыток электронной плотности, а он и есть более гидрогенизированный атом углерода при двойной связи.
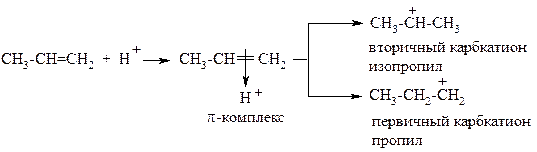 Теперь рассмотрим динамический фактор – сравним стабильность промежуточных частиц (карбкатионов). Вы уже знаете: чем стабильнее промежуточная частица (интермедиат), тем больше вероятность её образования.
Теперь рассмотрим динамический фактор – сравним стабильность промежуточных частиц (карбкатионов). Вы уже знаете: чем стабильнее промежуточная частица (интермедиат), тем больше вероятность её образования.
На стадии образования σ-комплекса теоретически могут образоваться два карбкатиона – пропил (первичный) и изопропил (вторичный). Атом углерода с полным положительным зарядом смещает к себе электронную плотность соседней (или соседних) C-C σ-связи, уменьшая собственный недостаток электронной плотности. Вторичный карбкатион более стабилен из-за большей компенсации положительного заряда на углероде:
 |
Если рассуждать о стабильности карбкатионов вообще, то самыми стабильными являются третичные, затем – вторичные, первичные, а самым нестабильным – катион метил:
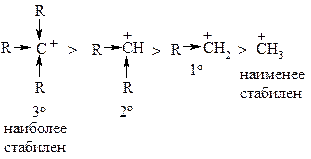 |
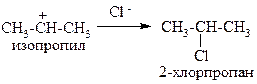 Так как в рассматриваемом примере более стабильным является изопропил-катион, именно он в первую очередь сможет провзаимодействовать с анионом хлора, а значит преобладающим продуктом этой реакции является 2-хлорпропан (т.е. протон водорода присоединился к более гидрогенизированному атому углерода):
Так как в рассматриваемом примере более стабильным является изопропил-катион, именно он в первую очередь сможет провзаимодействовать с анионом хлора, а значит преобладающим продуктом этой реакции является 2-хлорпропан (т.е. протон водорода присоединился к более гидрогенизированному атому углерода):
Классическое правило Марковникова можно без оговорок применять только к самим алкенам. В случае их производных нужно обязательно рассматривать статический и динамический факторы, влияющие на ход реакции (например, позже мы будем рассматривать реакции электрофильного присоединения в акриловой кислоте, которые протекают против правила Марковникова).
В современной интерпретации правило Марковникова формулируется так: направление присоединения реагентов типа HX к производным алкенов определяется относительной устойчивостью промежуточных карбкатионов.
Реакция гидрирования алкенов протекает по механизму радикального присоединения в присутствии катализаторов (никель, платина), на поверхности которых происходит гомолитический разрыв молекулы водорода. В результате гидрирования алкенов образуются алканы:
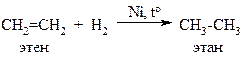 |
Реакции окисления алкенов протекают с образованием различных продуктов в зависимости от условий. Мы рассмотрим только так называемое мягкое окисление алкенов. Его проводят разбавленным раствором перманганата калия при комнатной температуре (реакция Вагнера).
В результате реакции образуются гликоль (двухатомный спирт) и диоксид марганца:
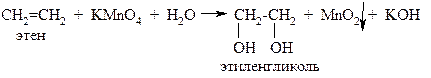 |
Эту реакцию используют как качественную на наличие двойной связи: в результате исчезает малиновое окрашивание перманганата калия и появляется бурый осадок диоксида марганца.
Дата публикования: 2015-09-18; Прочитано: 4304 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
