 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Механизмы образования химической связи
|
|
Обменный механизм. К обменному механизму образования химической связи относятся случаи, когда в образовании электронной пары от каждого атома участвует по одному электрону.
В молекулах Н2, Li2, F2 и Cl2 связи образуются за счет неспаренных s- и
р-электронов этих атомов. В молекулах HF и HCl связи образуются
s-электронами водорода и p-электронами галогенов. Особенностью образования соединений по обменному механизму является насыщаемость, которая показывает, что атом образует не любое, а ограниченное количество связей. Их число, в частности, зависит от количества неспаренных валентных электронов. Из квантовых ячеек N и Н
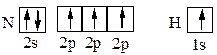
можно видеть, что атом азота имеет 3 неспаренных электрона, а атом водорода – один. Принцип насыщаемости указывает на то, что устойчивым соединением должен быть NH3, а не NH2, NH или NH4.
Донорно-акцепторный механизм – образование ковалентной связи за счёт двухэлектронного облака одного атома (донор) и свободной орбитали другого(акцептор). Примером образования химической связи по донорно-акцепторному механизму является реакция аммиака с ионом водорода:
H+ + ׃NH3 = NH4+
Роль акцептора электронной пары играет пустая орбиталь иона водорода. В ионе аммония NH4+ атом азота четырехвалентен. В молекуле аммиака заселены все четыре орбитали азота, из них три – по обменному механизму электронами азота и водорода, а одна содержит электронную пару, оба электрона которой принадлежат азоту. Такая электронная пара называется неподеленной электронной парой.
Донорно-акцeпторная связь отличается только способом образования; по свойствам она одинакова с остальными ковалентными связями
Дата публикования: 2014-10-16; Прочитано: 1892 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
