 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Свободнорадикальное окисление и антиоксидантная система организма
|
|
Одна из особенностей окислительно-восстановительных реакций - возможность их протекания как по гетеролитическому механизму, когда реагирующими частицами являются электрофил (окислитель) и нуклеофил (восстановитель), так и по гемолитическому механизму, когда реагирующими частицами являются радикалы. Все окислительно-восстановительные реакции, глубина протекания и скорость которых полностью контролируются организмом с помощью ферментов, протекают по гетеролитическому механизму. В то же время в организме имеет место свободнорадикальное окисление-восстановление, которое при низкой интенсивности является метаболически нормальным. Свободные радикалы участвуют в процессах клеточного деления, обновления ядерных мембран и многих других важных процессах. Но это необходимо и полезно до тех пор, пока интенсивность образования радикалов и их концентрация в клетке не превышают определенной нормы.
Главным источником радикалов в организме является молекулярный кислород, а в случае радиационного воздействия - вода. Молекула кислорода парамагнитна (разд. 12.2.5), так как она содержит два неспаренных электрона и представляет собой бирадикал  . При полном восстановлении молекула кислорода, принимая четыре электрона и четыре протона, превращается в две молекулы воды. При неполном восстановлении кислорода образуются различные его активные (токсичные) формы. К активным формам кислорода относятся:
. При полном восстановлении молекула кислорода, принимая четыре электрона и четыре протона, превращается в две молекулы воды. При неполном восстановлении кислорода образуются различные его активные (токсичные) формы. К активным формам кислорода относятся:

Под действием света молекулярный кислород переходит в синглетное состояние, т. е. в синглетный кислород 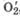 , в котором все электроны спарены. Синглетный кислород неустойчив, период полураспада - 45 мин. Он более активен в реакциях окисления, чем молекулярный кислород. Окислительная способность различных активных форм кислорода возрастает в следующей последовательности:
, в котором все электроны спарены. Синглетный кислород неустойчив, период полураспада - 45 мин. Он более активен в реакциях окисления, чем молекулярный кислород. Окислительная способность различных активных форм кислорода возрастает в следующей последовательности:
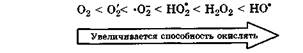
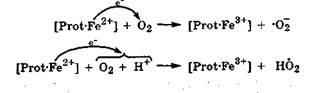 |
В организме токсичные кислородсодержащие радикалы возникают при взаимодействии О2 с металлопротеинами (гемоглобин, цитохромы), содержащими катионы металлов в низших степенях окисления (Fe2+, Cu+, Мn2+), получая от них электрон:
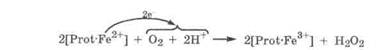 |
При радиационном воздействии на организм его вода подвергается радиолизу. При радиолизе воды ее молекула распадается с образованием различных радикальных частиц в зависимости от энергии облучения. При небольшой энергии облучения (Е1) молекула воды, переходя в возбужденное состояние
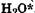 , затем распадается на два радикала
, затем распадается на два радикала 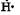 и
и  Эти активные частицы могут образовывать другие активные формы кислорода.
Эти активные частицы могут образовывать другие активные формы кислорода.
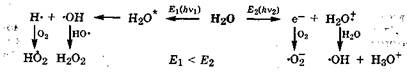
При большой энергии облучения (Е2) происходит настолько сильное возбуждение молекулы воды, что она распадается на быстрый электрон и катион-радикал воды ( I. Быстрый электрон через 10-11 с подвергается гидратации, попадая в микрополости водных ассоциатов (разд. 6.1). Он может взаимодействовать дальше с образованием новых радикальных частиц (например,
I. Быстрый электрон через 10-11 с подвергается гидратации, попадая в микрополости водных ассоциатов (разд. 6.1). Он может взаимодействовать дальше с образованием новых радикальных частиц (например,  |. Катион-радикал воды, взаимодействуя с молекулой воды, образует гидроксидный радикал -ОН и гидроксоний-ион Н30+. Таким образом, в результате радиолиза воды в организме происходит увеличение кислотности (закисление) среды (ацидоз - разд. 8.5) и образуются активные формы кислорода. При энергии облучения около 100 эВ и при комнатной температуре при взаимодействии с одним квантом распадается от 6 до 8 молекул Н2О. Возникающие при радиолизе атомарный водород Н- и гидратированный электрон являются чрезвычайно активными частицами с сильными восстановительными свойствами. Благодаря этому они легче взаимодействуют с кислородом, образуя его активные формы. Возрастание концентрации свободных радикалов способствует процессам свободнорадикального окисления-восстановления.
|. Катион-радикал воды, взаимодействуя с молекулой воды, образует гидроксидный радикал -ОН и гидроксоний-ион Н30+. Таким образом, в результате радиолиза воды в организме происходит увеличение кислотности (закисление) среды (ацидоз - разд. 8.5) и образуются активные формы кислорода. При энергии облучения около 100 эВ и при комнатной температуре при взаимодействии с одним квантом распадается от 6 до 8 молекул Н2О. Возникающие при радиолизе атомарный водород Н- и гидратированный электрон являются чрезвычайно активными частицами с сильными восстановительными свойствами. Благодаря этому они легче взаимодействуют с кислородом, образуя его активные формы. Возрастание концентрации свободных радикалов способствует процессам свободнорадикального окисления-восстановления.
Образовавшиеся радикальные частицы эффективно атакуют биосубстрат прежде всего по пространственно доступным и малополярным связям С—Н. Возникающая при этом радикальная частица, в которой неспаренный электрон находится у атома углерода субстрата, дальше легко окисляется активными формами кислорода вплоть до разрыва связей С—С, что приводит к глубокой деструкции молекул биосубстрата. По такой схеме происходит так называемое пероксидное окисление липидов.
Активные формы кислорода, прежде всего радикал 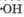 , эффективно атакуют связи С—Н, особенно в аллильном положении у ненасыщенных жирных кислот, так как при этом образуется аллил-радикал, стабилизированный за счет взаимодействия неспаренного электрона с
, эффективно атакуют связи С—Н, особенно в аллильном положении у ненасыщенных жирных кислот, так как при этом образуется аллил-радикал, стабилизированный за счет взаимодействия неспаренного электрона с 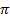 -электронами соседней двойной связи:
-электронами соседней двойной связи:
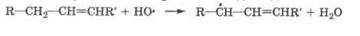 |
Таким образом происходит зарождение цепи (разд. 5.4), т. е. I этап свободнорадикального окисления. Развитие цепи (II этап) включает окисление аллилрадикалов молекулярным кислородом с возникновением алкилпероксидных радикалов:

При взаимодействии этих радикалов с молекулами воды образуются неустойчивые гидропероксиды и снова возникают активные гидроксидные радикалы. Накопление радикалов в системе способствует дальнейшему развитию цепи окисления и резкому возрастанию скорости процесса.

Обрыв цепи (III этап) происходит, когда радикалы взаимодействуют, не образуя новых радикалов. Например, при столкновении гидропероксида с супероксидным анион-радикалом происходит его окисление с разрывом связей С—С и образованием двух карбоновых кислот:

Скорость свободнорадикального окисления определяется концентрацией радикалов и практически не регулируется организмом.
При экстремальных и патогенных воздействиях на организм образование кислородных радикалов в клетках и тканях резко усиливается, так как интенсифицируются окислительное фосфо-рилирование и гидроксилирование ксенобиотиков. Происходящее при этом с участием различных цитохромов окисление может способствовать появлению в организме активных форм кислорода и тем самым - свободнорадикальному окислению. Усиление свободнорадикального окисления вызывают разнообразные физические факторы: радиоактивное, ультрафиолетовое и лазерное излучение, шум, вибрация, а также различные болезни: простудные и легочные заболевания, атеросклероз, инфаркт миокарда, инсульт мозга, остеохондроз, диабет, язва желудка, туберкулез, злокачественные образования. Возможно, что свободнорадикальное окисление в перечисленных случаях является не только следствием этих болезней, но и одной из причин их возникновения.
В организме свободнорадикальное окисление сдерживается многокомпонентной антиоксидантной буферной системой, которая, превращая радикалы в малоактивные соединения, прерывает цепные реакции. Эти функции осуществляют:
- антиоксидантные и антиперекисные ферменты: суперок-сиддисмутаза, каталаза, глутатионпероксидаза;
антиоксиданты - органические соединения с выраженными восстановительными свойствами: различные тиолы (глутатион, цистеин, дегидролипоат), аскорбиновая кислота (витамин С), |3-каро-тин, а также витамины Е (токоферол), К, Р и стероидные гормоны.
Ферментные защитные средства. Аэробные клетки защищают себя от вредного воздействия супероксидного анион-радикала  с помощью ферментов супероксиддисмутаз, содержащих катионы меди
с помощью ферментов супероксиддисмутаз, содержащих катионы меди  или марганца
или марганца  которые катализируют превращения супероксидного анион-радикала в пероксид водорода:
которые катализируют превращения супероксидного анион-радикала в пероксид водорода:

Снижение концентрации токсичного пероксида водорода в клетках осуществляется с помощью ферментов каталазы и глутатион-пероксидазы. Каталаза - железосодержащий фермент - эффективно способствует распаду пероксида водорода на воду и кислород:

Глутатионпероксидаза катализирует взаимодействие пероксида водорода и гидропероксидных радикалов с довольно сильным восстановителем глутатионом (G—SH), являющимся трипептидом, содержащим тиольную группу аминокислоты цистеина:

Регенерация глутатиона осуществляется восстановлением с помощью НАДФ(Н): 
Антиоксиданты. Все антиоксиданты, взаимодействуя с активными формами кислорода, прерывают свободнорадикальное окисление и переходят в окисленные формы, которые под действием соответствующих ферментов опять превращаются в восстановленные формы.
Антиоксиданты - вещества, обратимо реагирующие со свободными радикалами и окислителями и предохраняющие от их воздействия жизненно важные метаболиты.
Эффективными антиоксидантами являются тиолы R—SH, т. е. соединения, содержащие тиольную группу, которая за счет атома серы со степенью окисления -2 легко окисляется, образуя дисульфиды R—S—S—R (тиол-дисульфидная система):

 |
За счет сильных восстановительных свойств тиолы (табл. 9.2) являются эффективными ловушками радикалов, и поэтому на их основе созданы радиопротекторы - средства, защищающие организм от радиации, например синтетические препараты унитиол (2,3-димеркаптопропансульфонат натрия) и N-ацетилцистеин.
Тиолы вносят значительный вклад в буферную емкость ан-тиоксидантной системы. Восстановление дисульфидов в тиолы в организме происходит под действием восстановленных форм пиридин-протеинов, содержащих НАД(Н) и НАДФ(Н).
Другим эффективным антиоксидантным средством является аскорбиновая кислота (витамин С), которая под действием окислителей, особенно радикалов, легко отдает два электрона и два катиона водорода, переходя при этом в дегидроаскорбиновую кислоту:

Вероятно, именно за счет антиоксидантной активности прием витамина С в повышенных дозах способствует предотвращению простудных и других заболеваний или снижению остроты их протекания.
В отличие от аскорбиновой кислоты, которая хорошо растворима в воде, другие природные антиоксиданты (B-каротин, витамины А, Е, К, Р) хорошо растворимы в жирах. Антиоксидантные свойства этих веществ в основном определяются наличием в них легко окисляемых группировок. Витамин А и B-каротин содержат длинную углеводородную систему сопряженных двойных связей, витамин Е (токоферол) - хиноидную группировку, витамин К - нафтохиноидную группировку, а витамин Р - резорциновую группировку. Все эти вещества являются эффективными ловушками свободных радикалов в организме. С помощью лекарственных и профилактических средств на основе антиоксидантов достигается увеличение сопротивляемости организма свободнора-дикальному окислению. Таким образом, хотя организм не может эффективно контролировать развитие и скорость свободно-радикального окисления, но с помощью антиоксидантной буферной системы достигается сдерживание этого процесса.
Увеличение в клетке (ткани) концентрации свободных радикалов или пероксидов приводит к снижению буферной емкости антиоксидантной системы, что создает реальную угрозу воздействия этих окислителей на жизненно важные субстраты и развития так называемого «окислительного стресса». Для оценки буферной емкости антиоксидантной системы предложено (В. В. Соколовский, 1984) использовать коэффициент тиол-дисульфидного соотношения крови. Буферная емкость антиоксидантной системы будет тем больше, чем больше в системе содержится тиолов. Контроль за тиол-дисульфидным соотношением дает более полнук информацию об уровне активности антиоксидантной системы, чем другие показатели: содержание витамина А, витамина С, витамина Е или активность супероксиддисмутазы. Этот показатель позволяет судить о состоянии одного из важных звеньев биохимического механизма неспецифической реакции организма на экстремальные воздействия.
Дата публикования: 2014-10-16; Прочитано: 6722 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
