 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Обмен веществ (метаболизм) и энергии в клетке клеточные мембраны, их строение и функции
|
|
5.1. Клетка как открытая система. Ассимиляция и диссимиляция
Клетка как структурная и функциональная единица живого представляет собой открытою систему, т.е. постоянно обменивается веществом и энергией с окружающей средой.
Под клеточным обменом веществ понимают непрерывное поступление веществ в клетку из внешней среды, химическое превращение этих веществ и выделение конечных продуктов химических реакций.
Функции клеточного обмена веществ:
1. Обеспечение клетки строительным материалом, необходимым для образования клеточных структур;
2. Снабжение клетки энергией, которая используется на процессы жизнедеятельности (синтез веществ, транспорт веществ и др.);
3. Сохранение относительного постоянства состава и физико-химических свойств клеток;
4. Самообновление клеток и тканей.
Различают внешний обмен – поглощение и выделение веществ, и внутренний обмен – химическое превращение этих веществ в клетке.
Внутренний обмен, или метаболизм, представляет собой совокупность двух противоположных реакций: анаболический и катаболический.
Анаболические реакции – это реакции синтеза сложных органических веществ из более простых. Протекают они с затратами энергии, обеспечивая постоянство состава клеток и тканей организма. Совокупность этих реакций носит название ассимиляции или пластического обмена. Примером ассимиляции может быть биосинтез белка, синтез углеводов из воды и углекислого газа в процессе фотосинтеза, синтез нуклеотидов, ДНК, РНК, полисахаридов, липидов и других соединений.
Катаболические реакции – это реакции расщепления сложных органических веществ (жиров, белков и углеводов) до более простых с выделением энергии, значительная часть которой идет на образование АТФ. Эти реакции часто называют энергетическим обменом, или диссимиляцией.
Совокупность реакций ассимиляции и диссимиляции составляют основу жизнедеятельности клетки, а, следовательно, ткани, органа и организма вцелом.
| Обмен веществ |
| поглощается |
| энергия |
| выделяется |
| Из простых синтезируются более сложные |
| Химические соединения |
| Сложные распадаются до простых |
| Обеспечение клетки строительным материалом |
| задача |
| Обеспечения клетки энергии |
| пластический |
| энергетический |
| АТФ-расходуется |
| АТФ образуется |
| АТФ (АДЕНОЗИНТРИФОСФАТ) |
Рис. 5.1. Обмен веществ и АТФ в клетке
АТФ + Н2О ↔ АДФ + Н3РО4 + 40 кДж
Не всегда процессы ассимиляции находятся в соответствии с процессами диссимиляции. В период интенсивного роста и развития организма процессы ассимиляции преобладают. Напротив, при старении, интенсивной физической работе, недостатке питательных веществ процессы диссимиляции преобладают над процессами ассимиляции.
Различают автотрофную и гетеротрофную ассимиляцию. При гетеротрофной ассимиляции (животные, грибы) источником энергии служат вещества пищи (химическая энергия), при автотрофной ассимиляции – энергия света используемая для фотосинтеза (рис.5.2.)

Рис.5.2. Обмен веществ и энергии у автотрофных и гетеротрофных клеток
Из рис. 5.2. видно, что существование жизни на Земле зависит от энергии Солнца и сложных ее преобразований в авто- и гетеротрофных клетках организмов. В упрощенном виде поток энергии в живой природе можно представить так:
1. Энергия Солнца → автотрофы → органические вещества → АТФ → различные формы работы.
2. Энергия Солнца → автотрофы → органические вещества → гетеротрофы → АТФ → различные формы работы
Автотрофы – сами синтезируют органические вещества с неорганических.
Гетеротрофы – употребляют готовые органические вещества, синтезированные другими организмами.
5.2. Поток энергии в клетке
В основе потока энергии в клетке лежат процессы питания организмов и клеточного дыхания.
1. Питание – процесс приобретения вещества и энергии живыми организмами.
2. Клеточное дыхание – процесс, с помощью которого живые организмы высвобождают энергию из богатых ею органических веществ при их ферментативном расщеплении (диссимиляции) до более простых. Клеточное дыхание может быть аэробным и анаэробным.
3. Аэробное дыхание – получение энергии происходит при участии кислорода в процессе расщепления органических веществ. Его еще называют кислородным (аэробным) этапом энергетического обмена.
Анаэробное дыхание – получение энергии из пищи без использования свободного атмосферного кислорода. В общем виде поток энергии в клетке можно представить следующим образом (рис 5.3.)
| ПИЩА |
| САХАР, ЖИРНЫЕ КИСЛОТЫ, АМИНО-КИСЛОТЫ |
| КЛЕТОЧНОЕ ДЫХАНИЕ |
| АТФ |
| СО2, Н2О, NH3 |
| ХИМИЧЕСКАЯ, МЕХАНИЧЕСКАЯ, ЭЛЕКТРИЧЕСКАЯ, ОСМОТИЧЕСКАЯ РАБОТА |
| АДФ + Н3РО4 |
Рис.5.3. Поток энергии в клетке
Химическая работа: биосинтез в клетке белков, нуклеиновых кислот, жиров, полисахаридов.
Механическая работа: сокращение мышечных волокон, биение ресничек, расхождение хромосом при митозе.
Электрическая работа – поддержание разности потенциалов на мембране клетки.
Осмотическая работа – поддержание градиентов вещества в клетке и окружающей ее среде.
5.3. Этапы энергетического обмена (аэробного дыхания)
Процесс аэробного дыхания проходит в три этапа: 1) подготовительный; 2) бескислородный; 3) кислородный.
Первый этап – подготовительный или этап пищеварения, включающий в себя ферментативное расщепление полимеров до мономеров: белков до аминокислот, жиров до глицерина и жирных кислот, гликогена и крахмала до глюкозы, нуклеиновых кислот до нуклеотидов. Протекает в желудочно-кишечном тракте при участии пищеварительных ферментов и цитоплазме клеток при участии ферментов лизосом.
На этом этапе выделяется небольшое количество энергии, рассеивающейся в виде тепла, а образовавшиеся мономеры подвергаются в клетках дальнейшему расщеплению или используются как строительный материал.
Второй этап – анаэробный (бескислородный). Он протекает в цитоплазме клеток без участия кислорода. Мономеры, образовавшиеся на первом этапе, подвергаются дальнейшему расщеплению. Примером такого процесса является гликолиз – бескислородное неполное расщепление глюкозы.
В реакциях гликолиза из одной молекулы глюкозы (С6Н12О6) образуются две молекулы пировиноградной кислоты (С3Н4О3 – ПВК). При этом от каждой молекулы глюкозы отщепляется 4 атома Н+ и образуются 2 молекулы АТФ. Атомы Водорода присоединяются к НАД+ (никотинамидадениндинуклеотид, функция НАД и подобных к нему переносчиков состоит в том, чтобы в первой реакции принимать Водород (восстанавливаться), а в другой – его отдавать (окисляться).
Сумарное уравнение гликолиза выглядит так:
С6Н12О6 + 2АДФ + 2Н3РО4 + 2НАД+→ 2С3Н4О3 + 2АТФ + 2Н2О +2НАД·Н2
В процессе гликолиза выделяется 200 кДж/моль энергии, из которой 80 кДж или 40% идет на синтез АТФ, а 120 кДж (60%) рассеивается в виде тепла.
В анаэробных организмах (многие бактерии, микроскопические грибы, внутрикишечные паразиты) этот этап является конечным. ПВК (в зависимости от типа брожения) может превращаться в молочную кислоту (С3Н6О3), этиловый спирт (С2Н5ОН). Некоторые клетки (например, мышечные, клетки растений) при недостатке кислорода могут переходить на анаэробное дыхание. В этих случаях:
а) в животных клетках образуется 2 молекулы молочной кислоты, которая в дальнейшем превращается в гликоген и депонируется в печени;
б) в растительных клетках происходит спиртовое брожжение с выделением СО2. Конечным продуктом является этанол.
Анаэробное дыхание по сравнению с кислородным дыханием эволюционно более ранняя, но менее эффективная форма получения энергии из питательных веществ.
Третий этап – аэробный (кислородный, тканевое дыхание) протекает в митохондриях и требует присутствие кислорода.
Органические соединения, образовавшиеся на предыдущем бескислородном этапе, окисляются путем отщепления водорода до СО2 и Н2О. Отсоеденившееся атомы Водорода с помощью переносчиков передаются до Кислорода, взаимодействуют с ним и образуют воду. Этот процесс сопровождается выделением значительного количества энергии, часть которой (55%) идет на образование воды. В кислородном этапе можно выделить реакции цикла Кребса и реакции окислительного фосфорилирования.
Цикл Кребса (цикл трикарбоновых кислот) происходит в матриксе митохондрий. Его открыл английский биохимик Х. Кребс в 1937 году.
Цикл Кребса начинается реакцией пировиноградной кислоты с уксуснокислой. При этом образуется лимонная кислота, которая после ряда последовательных преобразований снова становится уксуснокислой и цикл повторяется.
В ходе реакций цикла Кребса из одной молекулы ПВК образуется 4 пары атомов Водорода, две молекулы СО2, одна молекула АТФ. Углекислый газ выводится из клетки, а атомы Водорода присоединяются к молекулам переносчиков – НАД и ФАД (флавинадениндинуклеотид), в результате чего образуются НАД·Н2 и ФАД·Н2.
Передача энергии от НАД· Н2 и ФАД·Н2, которые оброзовались в цыкле Кребса и на предыидущем анаэробном этапе, к АТФ просходит на внутренней мембране митохондрий в дыхательной цепи.
Дыхательная цепь или цепь переноса электронов (электронно-транспрортная цепь) содержится во внутренней мембране митохондрий. Её основу составляют переносчики электронов, которые входят в состав ферментных комплексов, катализирующих окислительно-востановительные реакции.
Пары Водорода отщепляются от НАД·Н2 и ФАД·Н2, в виде протонов и электронов (2Н++2е), поступают в электронно-транспортную цепь. В дыхательной цепи они вступают в ряд биохимических реакций, конечный результат которых – синтез АТФ (рис.5.4.)
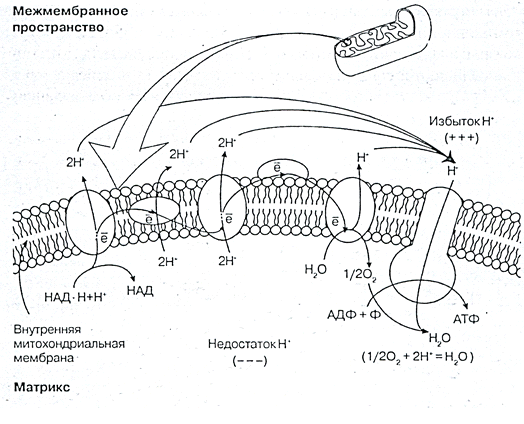
Рис. 5.4 Электронно-транспортная цепь
Электроны и протоны захватываются молекулами переносчиков дыхательной цепи и переправляются: электроны на внутреннюю сторону мембраны, а протоны на внешнюю. Электроны соединяются с Кислородом. Атомы Кислорода при этом становятся отрицательно заряженными:
О2 + е- = О2-
На внешней стороне мембраны накапливаются протоны (Н+), а изнутри анионы (О2-). В результате этого возрастает разность потенциалов.
В некоторых местах мембраны встроены молекулы фермента для синтеза АТФ (АТФ-синтетаза), который имеет ионный (протонный) канал. Когда разница потенциалов на мембране достигает 200мВ, протоны (Н+) силой электрического поля проталкиваются через канал и проходят на внутреннюю сторону мембраны где взаимодействуют с О2-, образуя Н2О
½ О2 + 2Н+ = Н2О
Кислород, поступающий в митохондрии необходим для присоединения электронов (е-), а затем протонов (Н+). При отсутствии О2 процессы, связанные с транспортом протонов и электронов, прекращаются. В этих случаях многие клетки синтезируют АТФ, расщепляя питательные вещества в процессе брожения.
Суммарное уравнение кислородного этапа
2С3Н4О3 + 36Н3РО4 + 6О2 + 36 АДФ = 6СО2 + 42 Н2О + 36АТФ + 2600кДж
1440 (40·36) аккумулируется в АТФ
1160 кДж выделяются в виде тепла
Суммарное уравнение кислородного дыхания, включающее бескислородный и кислородный этапы:
С6Н12О6 + 38АДФ + 38Н3РО4 + 6О2 = 38АТФ +6СО2 + 44Н2О
Конечные продукты энергетического обмена (СО2, Н2О, NH3), а также избыток энергии выделяются из клетки через клеточную мембрану, строение и функции которой заслуживают особого внимания.
5.4. КЛЕТОЧНЫЕ МЕМБРАНЫ, ИХ СТРОЕНИЕ И ФУНКЦИИ
Возникновение биологических мембран сыграло определяющую роль на последнем этапе химической эволюции пробионтов – в их превращении в прокариотичекие клетки.
Мембраны отграничивают содержимое клетки от окружающей среды (других клеток, межклеточного вещества). Большинство органоидов клетки имеет мембранное строение. Мембраны формируют оболочку ядер, митохондрий и пластид. Они образуют лизосомы, аппарат Гольджи, эндоплазматическую сеть, вакуоли растительных и грибных клеток, пульсирующие вакуоли простейших и другие органоиды. Все эти структуры представляют собой компартменты (отсеки), в которых осуществляются специфические биохимические процессы.
Благодаря компартментации цитоплазмы обеспечивается разделение функций между разными структурами клетки. Одновременно создаются условия для закономерного взаимодействия различных структур цитоплазмы между собой.
Мембраны (за исключением мембран митохондрий и пластид) связаны между собой структурно и функционально могут превращаться друг в друга (течение мембран). Например, из эндоплазматического ретикулюма образуются мембраны комплекса Гольджи, а последние служат материалом для регенерации плазмалеммы, образования лизосом. После деления клетки, из мембран ЕПС образуется ядерная мембрана. Внешняя мембрана ядра является продолжением мембраны ЕПС.
Мембраны играют большую роль в упорядочности и скорости протекания биохимических реакций в клетки так как многие ферменты расположены на мембранах строгой очередности, которая соответствует последовательности протекания взаимосвязанных реакций одного метаболического пути. В этой связи, напомним, что скорость протекания химических реакций в пробирке, главным образом, зависит от концентрации веществ и температуры, которые определяют вероятность их встречи и взаимодействия.
Функции биологической мембраны:
1. Структурная – является структурным компонентом плазмалеммы,
большинства органоидов, кариолеммы;
2. Разделительная – разделяет цитоплазму клетки на отсеки;
3. Транспортная – обеспечивает транспорт веществ;
4. Рецепторная – узнает определенные вещества;
5. Ферментативная – некоторые белки являются ферментами
6. В биологических мембранах происходят процессы, связанны с восприятием и передачей информации, формированием и передачей возбуждения, преобразованием энергии и др.
Среди биологических мембран наиболее постоянной универсальной для всех эу- и прокариот являются плазматическая мембрана, которая ограничивает цитоплазму - плазмалемма.
Плазматическая мембрана, или плазмалемма.
Это биологическая мембрана толщиной 6-10 нм, покрывающая цитоплазму, через которую происходит обменные процессы между клеткой и окружающей средой.
Она состоит из липидов (в основном фосфолипидов), белков и углеводов, которые образуют комплексы с белками и липидами (гликопротеины и гликолипиды соответственно).
На рис. 5.5. представлена общепринятая в настоящее время так называемая жидкостно-мозаичная модель строения биологических мембран.
Основу биологической мембраны составляет фосфолипидный двойной слой (билипидный слой). Мембранные липиды имеют гидрофобную (водоотталкивающую) часть и гидрофильную (водорастворимую) часть.

Рис. 5.5. Схема строения мембраны
В бислое молекулы липидов расположены таким образом, что их неполярные водоотталкивающие концы обращены внутрь мембраны, а полярные водорастворимые концы ориентированы к внутренней и внешней среде. Белки, входящие в мембрану, не составляют сплошного слоя на внешней и внутренней поверхности билипидного слоя.
Мембранные белки представлены тремя разновидностями:
- периферические белки расположены на поверхности билипидного слоя;
- интегральные белки пронизывают всю толщу молекул. Эти белки образуют каналы – поры. Через которые проходят водорастворимые вещества;
- полуинтегральные белки погружены в мембрану лишь наполовину.
Эту модель мембраны называют «жидкостно-мозаичной» поскольку в мембране имеется много различных белков, образующих своего рода мозаику, и что многие из них перемещаются в жидких липидных слоях мембраны.
Углеводы не входят самостоятельно в состав мембраны. Они связаны с периферическими белками или липидами, образуя гликопротеины и гликолипиды. Гликопротеиновый комплекс толщиной 10-20 нм покрывающий сверху плазмолемму получил название гликокаликс. В гликокаликсе происходит внеклеточное пищеварение, в нем располагаются многие рецепторы клетки. С его помощью происходит адгезия клеток. Адгезия клеток – способность их слипаться друг с другом и субстратами.
Свойства и функции плазмалеммы
Клеточные мембраны являют собой подвижные, динамические структуры, поскольку молекулы белков и липидов удерживаются слабыми гидрофильно-гидрофобными взаимодействиями и могут перемещаться в плоскости мембраны. Это явление получено название текучести мембран. Благодаря текучести мембраны способны быстро восстанавливаться после повреждения, а также растягиваться и сжиматься.
Плазматическая мембрана живых клеток заряжена (снаружи положительный заряд, разность потенциалов 20-100мВ).
Белки, гликопротеины и белки клеточных мембран в клетках разных типов неодинаковы. Поэтому каждый тип клеток характеризуется своей индивидуальностью, которая в основном определяться гликопротеинами. Например, у человека эритроциты разных групп крови по системе АВ0 различаются по антигенам А и В, которые по своей химической природе являются гликопротеинами. Яйцеклетка и сперматозоид узнают друг друга по гликопротеинам клеточной поверхности, после чего возможно оплодотворение.
Таким образом, глюкопротеины клеточных мембран могут функционировать как информационные молекулы клетки.
В мембранах содержаться специфические рецепторы, ферменты, антитела.
Мембранные белки – антитела осуществляют защитную функцию. Они способны связывать антигены (микроорганизмы, чужеродные для клетки вещества), препятствуя их проникновению в клетку.
Мембранные рецепторы – это так называемые сигнальные белки плазматической мембраны, которые способны связывать физиологически активные вещества: гормоны и нейрогормоны. Рецепторы специфичны – для каждого гормона существуют свои рецепторы.
Действие гормона на клетку осуществляется через рецепторы. После связывания гормона с рецептором может измениться проницаемость мембран, их полярность, обменные процессы, генерироваться нервный импульс.
Для того чтобы клетка обладала способностью отвечать на различные сигналы, поступающие из внешней среды, передаваемые с помощью гормонов, она должна нести на своей поверхности соответствующий набор рецепторов. Например, клетки печени имеют рецепторы для инсулина, глюкагона, адреналина и других гормонов. Когда гормон связывается со специфическим рецептором, то это запускает цепь событий, в результате которых проявляется действие гормона.
Важнейшим свойством мембраны является ее избирательная проницаемость, т.е. одни вещества проходят через нее легче и даже в сторону большей концентрации. Максимально проникающей способностью через мембрану обладает вода и растворенные в ней газы. Перемещение заряженных ионов через мембрану происходит значительно медленнее. Хорошо проникают через биологические мембраны вещества, растворимые в липидах (например, алкоголь).
Различают пассивный и активный транспорт веществ через клеточную мембрану.
Пассивный транспорт веществ происходит без использования энергии по градиенту концентрации (из области, где их концентрация выше, в область, где их концентрация ниже). Пассивный транспорт небольших полярных молекул (СО2, Н2О) и неполярных (О2,N2) осуществляется путем диффузии и осмоса.
Диффузия – это процесс, в ходе которого молекулы (или ионы) переходят через мембрану из области с высокой концентрацией в область низкой концентрации в результате броуновского движения (теплового движения атомов и молекул).
Различают простую и облегченную диффузию веществ через клеточную мембрану (рис.5.6.).

Рис. 5.6. Виды диффузии веществ через мембрану
Простая диффузия происходит через те участки мембран, где преобладают липиды. Характеризуется низкой избирательностью мембраны к веществам, которые переносятся. Известным примером такой диффузии может быть газообмен O2 и СO2 в легких и тканях. Простая диффузия легко происходит через липидный слой мембран веществ, хорошо растворимых в липидах, к которым относятся многие лекарства.

Рис. 5.7. Простая диффузия
При облегченной диффузии специальные мембранные белки-переносчики временно соединяются с молекулой вещества и проводят его через мембрану. Процесс пассивен в том смысле, что перенос осуществляется по градиенту концентрации, и характеризуется тем, что он:
· специфичен для определенных молекул (например, переносчик осуществляет транспорт только Д-, но не L-глюкозы);
· осуществляется быстрее, чем обычная диффузия;
· достигает насыщения.
Специфические носители имеются для многих молекул, таких, как глюкоза, лактоза, аминокислоты, нуклеотиды, глицерол и др.
В любой конкретной клетке имеются конечное число переносчиков для данной молекулы или йона. Когда все они заняты, скорость переноса становится максимальной. Следовательно, процесс достигает насыщения. Когда разность концентраций вещества равно нулю, переносчики, продолжая работать, переносят молекулы внутрь и наружу клетки с одинаковой скоростью, поэтому в целом диффузия не наблюдается.
Осмос – диффузия воды через мембрану из менее концентрированного в более концентрированный раствор. Естественно в более разбавленном растворе концентрация воды «выше», чем в концентрированном. В процессе осмоса происходит выравнивание концентраций двух растворов, разделенных избирательно проницаемой мембраной.

Рис. 5.8. Осмос
Активный транспорт – перенесение веществ против градиента концентрации с использованием энергии. Он осуществляется с помощью белков-переносчиков, образующих так называемые ионные насосы для переноса ионов в сторону более высокого биохимического потенциала. Наиболее известным является Na+/K+– насос в клетках животных, который обуславливает активный транспорт в клетку ионов Калия и выведения из нее ионов Натрия. Благодаря этому внутри клетки поддерживается высокая концентрация K+ и меньшая Nа+ по сравнении с внешней поверхностью плазмолеммы. Ионы (Na+, K+, Ca2+) переносятся через мембраны нервных, мышечных и других клеток благодаря наличию в них ионных каналов. Ионные каналы – надмолекулярные системы биологических мембран, имеющих липопротеидную природу и обеспечивающие избирательное прохождение определенных ионов через мембрану. Ионные каналы открываются и закрываются в зависимости от величины и разности электрических потенциалов на мембране или действия химических медиаторов. Некоторые вещества (ионофоры) сами способны создавать ионные каналы в липидном слое мембраны. Такими веществами являются многие антибиотики.
Нарушение работы ионных насосов и каналов сопровождается развитием патологических состояний в организме.
Действие ряда лекарственных препаратов основано на изменении свойств каналов и переносчиков, что позволяет регулировать транспорт веществ в клетке, ткани, органе и организме в целом.
Макромолекулы белков, полисахаридов, нуклеиновых кислот, липопротеидов поступают в клетку путем эндоцитоза. Эндоцитоз – способность клетки активно поглощать питательные вещества в виде мелких пузырьков (пиноцитоз) или твердых частиц (фагоцитоз). В результате этого образуются мелкие мембранные вакуоли, которые соединяются с лизосомой. Под влиянием ферментов лизосом макромолекулы вакуолей расщепляются до мономеров, которые используются в клетке как пластический и энергетический материал.

Рис.5.9. Обобщенная схема транспорта веществ через плазмалемму

Рис.5.10. Эндо- и экзоцитоз веществ
На основе изложенного выше можно выделить следующие основные функции плазмалеммы:
1. Ограничивают цитоплазму, определяют размеры и форму клеток.
2. Устанавливают связь клеток между собой и окружающей средой.
3. Обеспечивает перемещение веществ в клетку и из нее.
4. Выполняет рецепторную функцию (получение и преобразование сигналов из внешней среды; узнавание веществ).
ЯДРО. МОРФОЛОГИЯ ХРОМОСОМ. КАРИОТИП ЧЕЛОВЕКА
6.1. Строение и функции ядра
Ядро – информационный и регуляторный центр еукариотической клетки, поскольку именно с ним связано хранение и передача наследственной информации, все процессы синтеза белков, в том числе и ферментов. В свою очередь именно белки играют основную роль в регуляции биохимических, физиологических и морфологических процессов клетки.
Большинство эукариотических клеток имеют одно ядро, но встречаются двухъядерные (инфузории) и многоядерные (мышечные волокна, гепатоциты, млечные сосуды растений). Некоторые высокоспециализированные клетки в зрелом состояние не имеют ядра; таковы, например эритроциты млекопитающих, ситовидные трубки растений.
Форма и размеры ядра очень изменчивы и зависят от формы и величины клетки, выполняемой ее функции. Размеры ядра от 1 мкм (у простейших) до 1 мм (у некоторых рыб и теплокровных). Форма ядра обычно округлая или эллипсовидная. В клетках с высокой функциональной активностью форма ядер сложная. В результате этого увеличивается соотношение объема ядра к объему цитоплазмы (ядерно-цитоплазматическое соотношение), от которого зависит интенсивность биохимических процессов в клетке, ее рост, деление.
По химическому составу ядро отличается от остальных компонентов клетки высоким содержанием ДНК и РНК. В ядре сосредоточено 99% ДНК клетки в виде комплекса с белками - дезоксирибонуклеопротеидов (ДНП).
Ядерно - цитоплазматическое взаимодействие
Процессы взаимодействия ядра и цитоплазмы обеспечивают морфофункциональное единство клетки. Из цитоплазмы в ядро поступают вещества (обычно белковой природы), которые регулируют активность генов. В ядре также находятся нуклеотиды, АТФ; ферменты, необходимые для репликации ДНК, синтеза РНК, а также белки, входящие в состав хроматина, ядрышек и других структур ядра. Из ядра в цитоплазму выходят продукты генной активности: и-РНК, т-РНК, субъединицы рыбосом (р-РНК в комплексе с белками), которые обеспечивают синтез белков в цитоплазме – структурных белков, белков-ферментов.
Таким образом, ядро управляет всеми белковыми синтезами и через них функциональными и морфологическими процессами в клетке, а цитоплазма − регулирует (по принципу обратной связи) активность генетического аппарата ядра и снабжает его материально и энергией.
Выделяют два состояния ядра: интерфазное и делящееся. В интерфазном ядре происходит реализация генетической информации, а в период деления ядра – ее передача.
Структура интерфазного ядра
В интерфазном ядре различают: ядерную оболоночку, кариоплазму (ядерный матрикс, нуклеоплазма), хроматин и ядрышко (одно или несколько) (рис. 6.1.).

Рис.6.1. Схема строения клеточного ядра
Ядерная оболочка образована двумя мембранами (наружной и внутренней), между которыми находится перинуклеарное пространство шириной от 20 до 60 нм.
Наружная мембрана в некоторых местах переходит в каналы эндоплазматической сети, на ней располагаются рибосомы. Изнутри ядерная оболочка подстелается белковой сеткой – ядерной ламиной. До ламины теломерными участками присоединяются хромосомы (нити хроматина).
Ядерная оболочка пронизана множеством пор, диаметром около 90 нм, через которые происходит обмен веществ между ядром и цитоплазмой. Основная функция ядерной оболочки: регуляция потоков веществ между ядром и цитоплазмой. Через поры из ядра выходят разные виды РНК, субъединицы рибосом, а внутрь ядра поступают необходимые белки, нуклеотиды, ионы, вода.
Кариоплазма (ядерный матрикс) – внутреннее содержимое ядра, в котором располагаются хроматин и одно или несколько ядрышек. В состав кариоплазмы входит вода, минеральные соли, белки-ферменты, нуклеотиды, РНК, ионы. В нуклеоплазме имеются белковые фибриллы толщиной 2-3 нм, выполняющие роль внутреннего скелета ядра и соединяющие ядрышка, нити хроматина, ядерные поры. Кариоплазма осуществляет взаимосвязь всех структур ядра и обменные процессы с цитоплазмой клетки. Генетический материал в интерфазном ядре находится в виде хроматина.
Хроматин – комплекс ядерной ДНК с белками (дезоксирибонуклеопротеин – ДНП). В интерфазном ядре хромосомы деконденсированы (деспирализованы) и не выделяются по отдельности, а воспринимаются все вмести в виде глыбок, гранул, нитчатых структур, которые получили название хроматина. Существование хромосом в неделящихся клетках в форме хроматина обеспечивает возможность удвоения ДНК и реализации заключенной в ней генетической информации. Различные участки молекул ДНК в составе хроматина обладают разной степенью спирализации, а поэтому различаются степенью окраски и характером генной активности. После фиксации и специфической окраски в кариоплазме становятся видимыми два типа хроматина: хорошо окрашенный гетерохроматин и светлый эухроматин.
Гетерохроматин – это сильно конденсированные (уплотненные), а поэтому функционально неактивные участки хромосом. До 90% хроматина находится именно в такой форме. На электронно-микроскопических фотографиях гетерохроматин выглядит как сильно окрашенные темные участки ядра, расположеные в основном вблизи внутренней ядерной мембраны и вокруг ядрышка.
Эухроматин – слабо конденсированные (деспирализованные) функционально активные участки хромосом, расположеные между глыбами гетерохроматина. Под электронным микроскоп он выявляется в виде светлых участков ядра. На эухроматиновых участках считывается информация и образуется РНК. В клетках с интенсивным синтезом белка эухроматина больше.
Считается, что гетерохроматин неактивен в связи с высокой конденсацией, а эухроматин – активен. С другой стороны, только незначительная часть генов эухроматина активна, т.е. нахождение участков хромосом в состоянии эухроматина является недостаточным условием для экспрессии генов.
Различают конститутивный (структурный) и факультативный гетерохроматин.
Конститутивный – гетерохроматин содержится в обеих гомологичных хромосомах и локализуется в околоцентромерных и теломерных участках хромосом, а также определенных, постоянно конденсованных, участках некоторых хромосом. Полагают, что его роль заключается в прикреплении хроматина к ядерной оболочке, взаимном узнавании гомологичных хромосом в мейозе, разделении соседних структурных генов, участии в процессах регуляции их активности.
Факультативный гетерохроматин присутствует только в одной из гомологичных хромосом. Примером хроматина такого типа может быть половой хроматин, который в норме выявляется в клетках гомогаметного пола.
Половой хроматин – сильно спирализованная генетически инактивированная Х-хромосома, которая при специфическом окрашивании выявляется в интерфазных ядрах в виде темного тельца (тельца Барра). Количество телец полового хроматина в ядре на единицу меньше чем число Х-хромосом, т.е. равно nx-1(рис 6.2.).

Рис. 6.2. Половой хроматин (тельца Барра):
а-при кариотипе ХХ, ХХУ; б-при кариотипе ХУ, ХО; в-при кариотипе ХХХ
В сегментоядерных лейкоцитах Х-половой хроматин имеет вид специфической структуры, которая получила название «барабанные палочки» (рис. 6.3.)

Рис.6.3. Барабанные палочки в сегментоядерных лейкоцитах при кариотипе ХХ
Определение Х-полового хроматина используют для выявления нарушений кариотипа по числу Х-хромосом.
Химическую основу хроматина составляет двуспиральная ДНК (около 40%) и беки-гистоны (40%). Известно 5 типов гистонов, связанных с ДНК: Н1, Н2А, Н2В, Н3 и Н4. Благодаря основным радикалам гистоны взаимодействуют с ДНК, а благодаря гидрофобным радикалам они взаимодействуют между собой. Эти взаимодействия приводят к образованию нуклеосом.
Нуклеосома – нуклеопротеиновая структура, состоящая из гистонового октамера (глобула), обвитого участком ДНК длиной 140-160 пар нуклеотидов (рис. 6.4.).

Рис. 6.4. Нуклеосомы

Гистоновый октамер состоит из 8 молекул (по 2 молекулы гистонов Н2А, Н2В, Н3, Н4). Соседние нуклеосомы соединяются друг с другом короткими отрезками ДНК длиной 60 нуклеотидных пар.
Молекула ДНК принимает участие в образовании большого количества нуклеосом. В результате образуется хроматиновое волокно в виде «бусинок на нитке», при этом происходит укорочение ДНК примерно в 7 раз (рис 6.5.).

Двойная спираль ДНК –
Нуклеосомный уровень –
Уровень фибрилл –
Уровень петельных доменов –
Хромонемный уровень –
Метафазная хромосома –
Рис. 6.5. Уровни организации хроматина эукариот.
Нуклеосомный уровень организации хроматина свойствен как для эухроматина, так и для гетерохроматина. Но в тех локусах хроматина, на которых в данное время функционируют ферментные комплексы (репликации, транскрипции, репарации) ДНК, освобождается от взаимодействия с гистонами. В этих случаях нуклеосомная организация временно исчезает с тем, чтобы в последующим снова восстановится.
В отличие от этого, в гетерохроматине до нуклеосомного уровня добавляются последующие уровни компактизации хроматина.
Второй уровень – образование хроматиновых фибрил (глобул) за счет сближения нуклеосом, что обеспечивается гистоном Н1.
Третий уровень – образование петельных доменов (хромомер) за счет укладки хроматиновых фибрилл в петли.
Четвертый уровень – хромонемный. Образуется за счет сближения в линейном порядке хромомерных петель с образованием хромонемной нити.
Таким образом, хромосомы образуются из хроматина интерфазного ядра в процессе спирализации и конденсации дезоксирибонуклеопротеинов.
Хромосомы
Хромосомы (греч. хрома – краска, сома - тело) были так названы в связи со способностью их к интенсивному окрашиванию. Являются еденицами организации генетического материала и обеспечивают его точное распределение при делении клетки. Хромосомы лучше всего различимы (и изучаются) на стадии метафазы.
На стадии метафазы митоза хромосома состоит из двух нуклеопротеидных копий - хроматид. Хроматиды соединяются в области неспирализованой первичной перетяжки – центромеры. В центральной части центромеры расположен кинетохор, к которому присоеденяются нити веретена деления во время митоза.
Центромера делит хромосому на два плеча. Плечи имеют свои обозначения: короткое – p, и длинное – q. В зависимости от расположения центромеры различают следующие типы хромосом:
· метацентрические (равноплечие), в которых центромера расположена по средине (p=q);
· субметацентрические (неравноплечие), когда центромера смещена к одному концу хромосомы (q>p);
· акроцентрические (одноплечие или палочковидные), когда центромера расположена на краю хромосомы и одно плечо очень короткое (одноплечие - q).
Некоторые хромосомы имеют вторичные перетяжки, отделяющие спутники или сателлиты (рис.6.5.). Они характерны, например, для хромосом 13 – 15, 21 и 22 человека. В области вторичной перетяжки ряда хромосом имеется ядрышковый организатор – область формирования ядрышка.

А.

Б.
Рис. 6.5. Схема строения метафазной хромосомы (А), типы хромосом (Б).
Концевые участки хромосом получили название теломеры. Они препятствуют соеденинею хромосом между собой и сохраняют хромосому как дискретную индивидуальную единицу.
Правила хромосом:
1. Правило постоянства числа хромосом – у всех организмов одного вида соматические клетки имеют постоянное число хромосом.
2. Правило парности хромосом – в соматических клетках с диплоидным набором хромосом имеються пары одинаковых по структуре, форме и генному составу хромосом – так называемые гомологичные хромосомы (одна – материнская, вторая – отцовская).
3. Правило индивидуальности хромосом – каждая пара хромосом имеет свои особенности, что проявляется в размерах, форме, положении центромеры, чередовании светлых и темных полос при диференциальной окраске.
4. Правило непрырывности хромосом. В основе его лежит удвоение ДНК и формирование новых сестринских хроматид перед каждым делением клетки.
Набор хромосом соматических клеток конкретного вида живых организмов, называют кариотипом. Количество хромосом в кариотипе не зависит от уровня организации живых организмов. Некоторые протисты имеют их более тысячи, у шимпанзе – 48, у собаки - 78, у коровы - 60, у дрозофилы – 8, у рака отшельника - 254 и т.д.
У человека кариотип представлен 46 хромосомами (23 пары); 44 (22 пары) – аутосомы и две половые хромосомы: ХХ у женщины и ХУ у мужчины.
Исследуется кариотип обачно на стадии метафазы, когда каждая хромосома состоит из двух хроматид и максимально спирализована. Для изготовления препаратов хромосом человека обычно используют клетки лейкоцитов переферической крови. Сначала до культуры клеток добавляют колхицын, который останавливают деление клеток на стадии метафазы. Далее прибавляют гипотонический раствор 0,56% NaCl который отделяет хромосомы одну от другой, после чего их фиксируют и окрашивают. После такой обработки каждая хромосома имеет четкие очертания и видима в световом микроскопе (рис. 6.6)
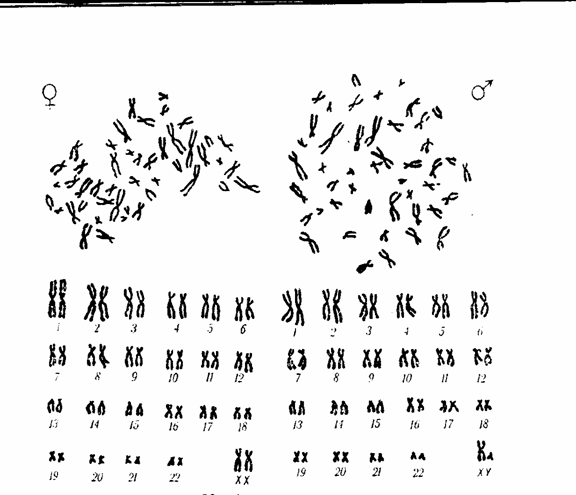
Рис. 6.6. Кариотип и идиограмма хромосом человека
Для того что бы провести анализ хромосом, образующих каріотип, их располагают в виде идиограммы.
Идиограмма – это систематизированный кариотип, в котором хромосомы располагаются попарно в порядке уменьшения их величины. Исключение делается для половых хромосом, которые располагаются последними.
Точно расположить хромосомы по величине сложно, так как некоторые пары хромосом весьма незначительно отличаются по размерам. В связи с этим в 1960 г была предложена Денверская классификация хромосом.
По этой классификации, кроме размеров хромосом, учитывают их форму, положение центромеры, наличие вторичных перетяжек и спутников. 23 пары хромосом разбиты на 7 групп от А до G. Важной характеристикой хромосом является центромерный индекс (ЦИ), который отражает отношение длины короткого плеча к длине всей хромосомы (в %).
Денверская классификация хромосом человека
| Группы | № пар хромосом | Размер (мкм) и тип хромосом | ЦИ (%) |
| А (І) | 1-3 | 11 - 8,3 большие метацентрические и субметацентрические | 38-49 |
| В (ІІ) | 4-5 | 7, 7 большие субметацентрические | 24-30 |
| C (ІІІ) | 6-12, х | 7,2 - 5,7 среднего размера, субметацентрические | 27-35 |
| D (ІV) | 13-15 | 4,2 акроцентрические | |
| E (V) | 16-18 | 3,6-3,2 относительно короткие метацентрические и субметацентрические | 26-40 |
| F (VI) | 19-20 | 2,8 - 2,3 две короткие, метацентрические | 36-40 |
| G (VII) | 21-22, у | 2,3 маленькие акроцентрические | 13-33 |
Основной метод идентификации хромосом на цитологических препаратах – это различные методы диференциации окраски (Q-, G-, R- и др.), которые основаны на применении флуоросцентных красителей. Даные красители специфически связываются с участками ДНК разного строения. Поэтому каждая дифференциально окрашенная хромосома имеет свой специфический рисунок в виде чередования поперечних светлых и темних сегментов (рис 6.7).
При этой окраски каждое плечо хромосомы разделяется на районы, нумерация которых идет от центромеры до теломеры. Полосы внутри районов нумеруються по порядку от центромеры до теломеры.
Методы дифференциальной окраски хромосом (разработанные в конце 1960-х и начале 1970-х годов) легли в основу Парижской классификации хромосом (1971), при которой учитывается не только величина и форма хромосом но и характерный для каждой хромосомы характер чередования поперечных светлых и тёмных сегментов.
 Рис. 6.7 Дифференциальная окраска хромосом (по А. Захарову, 1985)
Рис. 6.7 Дифференциальная окраска хромосом (по А. Захарову, 1985)
В медицинской генетике благодаря этим методам стало возможным более точно установить локализацию генов в хромосомах вплоть до описания конкретного района и полосы. Например, ген кодирующий эстеразу Д, локализуется в четвертой полосе первого района короткого плеча тринадцатой хромосомы. Символически это можно записать так: 13р14. Если установлено, что ген ренитобластомы локализуется в длинном плече 14-ой хромосомы, но не известно в каком районе, то символически это можно записати так: 14q. Методы дифференциальной окраски хромосом рассширили возможности в изучении хромосомных перестроек вплоть до точного описания районов, которые вовлекаются в ту или иную хромосомную абберации.
В наше время широко применяются методы автоматического анализа хромосомного набора с помощью лазерных лучей. Этот метод позволяет выявить некоторые хромосомные абберации, которые не выявляются обычными цитогенетическими методами.
Изучение кариотипа с точным дифференцированием хромосом имеет большое значение для диагностики хромосомных болезней человека, клеточной и генной инженерии.
Хромосомы являются носителями генов – единиц наследственной информации. Совокупность генов заключенных в диплоидном наборе хромосом клетки называется генотипом. При половом размножении генотип образуется при слиянии половых клеток с гаплоидным набором хромосом. Гаплоидный набор хромосом в классической литературе называют геномом. В настоящее время под понятием генома подразумевают совокупность всей наследственной информации в клетках организма – абсолютную величину генотипа, которая включает полный набор генов в клетке, но не отражает их алельного состояния. Геном – это характеристика вида, а генотип – характеристика организма, которая отражает совокупность всех генов особи, с учетом их алельного состояния.
ХАРАКТЕРИСТИКА НУКЛЕИНОВЫХ КИСЛОТ
Доказательства генетической роли ДНК
Название «нуклеиновые кислоты» происходит от латинского слова «нуклеус», т.е. ядро. Их впервые обнаружил в 1868 году И.Ф. Мишер в ядрах лейкоцитов.
Эксперименты 1940-1950-х гг убедительно доказали, что именно нуклеиновые кислоты (а не белки, как предполагали многие) являются носителями наследственной информации у всех организмов. В этих опытах была раскрыта биологическая природа явлений трансформации и трансдукции, на уровне микроорганизмов, механизмы взаимодействия организмов и клетки.
Трансформация (от лат. transformation – преобразование, изменение) – изменение наследственных свойств бактериальной клетки в результате проникновения в нее чужеродной ДНК. Впервые обнаружена в 1928г Ф. Гриффитсом. Гриффитс обнаружил, что при инъекции мышам одновременно двух штаммов пневмококков (R-штамма, невирулентного, и S-штамма, вирулентного, но убитого нагреванием), через несколько дней они погибали и в их крови были найдены вирулентные пневмококки S-штамма (рис.7.1.).
Э.Т. Эйвери совместно с сотрудниками (1944) установил, что фактором, превращающих непатогенных бактерий в патогенные, являются молекулы ДНК.
С открытием и изучением трансформации выяснилось, что ДНК – материальный носитель наследственной информации. Трансформация возможна и у клеток высших организмов.
Трансдукция (от лат. transductio – перемещение) – перенос бактериофагом фрагментов ДНК из одной бактериальной клетки в другую, что приводит к изменению наследственных свойств клетки. Привнесенная информация в процессе репликации ДНК передаётся в ряду клеточных поколений бактерии.
Явление трансдукции является подтверждением генетической роли ДНК, а также используется для изучения структуры хромосом, строения генов, является одним из методов генной инженерии.

Рис.7. 1.Схематическое изображение эксперимента Гриффитса: а – мышь которой введена культура патогенного инкапсулированого штамма S-пневмококков, погибает; б – мышь, которой введена культура непатогенного бескапсульного R-муанта, не погибает; в – мышь, получившая инъекцию культуры S- штамма, убитого нагреванием, не погибает; г-мышь, получившая при инъекциисмесьживойкультурыR-мутанта и убитой нагреванием культуры S- штамма погибает.
Еще одним доказательством того, что нуклеиновые кислоты, а не белки есть материальным субстратом генетической информации были опыты Х. Френкель-Конрата (1950) с вирусом табачной мозаики (ВТМ).
| Белки вирулентного штамма ВТМ |
| РНК вирулентного штамма ВТМ |
| Бели вирулентного штамма ВТМ + РНК авирулентного |
| Белки авирулентного штамма ВтМ + РНК вирулентного |
| Нет заболевания |
| Развивается заболевание |
| Развивается заболевание |
| Нет заболевания |
Схема опытов Х. Френкель-Конрата
Так, с открытием химической природы факторов трансформации и трансдукции у бактерий и механизмов взаимодействия вируса и клетки, была доказана роль нуклеиновых кислот в передаче наследственной информации.
| ВИДЫ НУКЛЕИНОВЫХ КИСЛОТ |
| ДЕЗОКСИРИБОНУКЛЕИНОВАЯ (ДНК) |
| РИБОНУКЛЕИНОВАЯ (РНК) |
| Входит в основном в хроматин ядра, хотя небольшое количество содержится в некоторых органоидах (митохондрии, пластиды) |
| Содержится в ядрышках, кариоплазме, рыбосомах, митохондриях, пластидах и в гиалоплазме |
Структура нуклеиновых кислот
Нуклеиновые кислоты – это полимеры, мономерами которых являются нуклеотиды. Нуклеотид включает в себя азотистое основание, углевод пентозу и остаток фосфорной кислоты (рис.7.2.).
| Остаток фосфорной кислоты |
| Азотистое основание |
| пентоза |
| 2' |
| 4' |
| 5' |
| 1' |
| 3' |
Рис.7.2. Структура нуклеотида
Азотистые основания нуклеотидов делятся на два типа: пиримидиновые (состоят из одного 6-членного кольца) и пуриновые (состоят из двух конденсированных 5- и 6-членных колец). Каждый атом углерода колец оснований имеет свой определенный номер, но с индексом штрих (′). В нуклеотиде азотистое основание всегда присоединено к первому атому углевода пентозы.
Именно азотистые основания определяют уникальную структуру молекул ДНК и РНК. В нуклеиновых кислотах встречаются 5 основных видов азотистых оснований (пуриновые – аденин и гуанин, пиримидиновые – тимин, цитозин, урацил) и более 50 редких (нетипичных)оснований. Основные азотистые основания обозначаются начальными буквами А, Г, Т, Ц, У. Нуклеотиды называются по содержащихся в них азотистых основаниях(табл. 7.1.).
Таблица 7.1. Типы азотистых оснований, нуклеозидов и нуклеотидов РНК и ДНК
| Названия азотистых оснований | Нуклеозиды | Нуклеотиды | Сокращенные обозначения нуклеотидов | ||||
| Полные | Сокращен-ные на рус. и англ.. | ||||||
| РНК | |||||||
| Пуриновые: | |||||||
| Аденин | (А; А) | Аденозин | Адениловая кислота (аденозин-5'-фосфат) | АМФ | |||
| Гуанин | (Г; G) | Гуанозин | Гуаниловая кислота (гуанозин-5'-фосфат ') | ГМФ | |||
| Пиримидиновые: | |||||||
| Цитозин | (Ц; С) | Цитидин | Цитидиловая кислота (цитидин-5'-фосфат) | ЦМФ | |||
| Урацил | (У; U) | Уридин | Уридиловая кислота (уридин-5'-фосфат) | УМФ | |||
| ДНК | |||||||
| Пуриновые: | |||||||
| Аденин | (А, А) | Дезокси- аденозин | Дезоксиадениловая кислота (дезоксиаденозин-5-фосфат) | дАМФ | |||
| Гуанин | (Г; G) | Дезокси- гуанозин | Дезоксигуаниловая кислота (дезоксигуанозин-5-фосфат) | дГМФ | |||
| Пиримидиновые: | |||||||
| Цитозин | (Ц; С) | Дезокси- цитидин | Дезоксицитидиловая кислота (дезоксицитидин-5'-фосфат) | дЦМФ | |||
| Тимин | (Т; Т) | Тимидин | Тимидиловая кислота (тимидин-5'-фосфат) | ТМФ | |||
 Формирование линейной полинуклеотидной цепочки происходит путем образования фосфодиэфирной связи пентозы одного нуклеотида с фосфатом другого. Пентозофосфатный остов состоит из (5′ -3′) связей. Концевой нуклеотид на одном конце цепочки всегда имеет свободную 5′ -группу, на другом - 3′ -группу.
Формирование линейной полинуклеотидной цепочки происходит путем образования фосфодиэфирной связи пентозы одного нуклеотида с фосфатом другого. Пентозофосфатный остов состоит из (5′ -3′) связей. Концевой нуклеотид на одном конце цепочки всегда имеет свободную 5′ -группу, на другом - 3′ -группу.

Рис.7.3. Формирование полипептидных цепочек молекул ДНК и РНК
В природе встречаются два вида нуклеиновых кислот: ДНК и РНК. В прокариотических и эукариотических организмах генетические функции выполняют оба типа нуклеиновых кислот. Вирусы всегда содержат лишь один вид нуклеиновой кислоты.
Основные отличия между ДНК и РНК представлена в таблице 7.2.
Таблиця 7.2.Характеристика нуклеиновых кислот
| Характеристика | ДНК | РНК |
| Структура | двойная спираль | различная для различных РНК |
| Количество цепей | две | одна |
| Азотистые основания в нуклеотидах | аденин(А), гуанин (Г), цитозин (Ц), тимин (Т) | аденин (А), гуанин (Г), цитозин (Ц), урацил (У) |
| Моносахариды в нуклеотидах | дезоксирибоза | рибоза |
| Способ синтеза | Удвоение по принципу комплементарности. Каждая новая двойная спираль содержит одну старую и одну новую синтезированную цепь | Матричный синтез по принципу комплементарности на одной из цепей ДНК |
| Функции | Сохранение и передача в ряду поколений генетической информации | Участвует в синтезе белка; м-РНК(матричная) – передает информацию о структуре белка от ДНК к месту его синтеза; р-РНК(рибосомальная) – входит в структуру рибосом, на которых синтезируется белок; т-РНК(транспортная)–транспортирует молекулы аминокислот к рибосомам. |
ДНК
азотистое основание:
аденин, гуанин, тимин, цитозин
углевод: дезоксирибоза С5Н10О4
остаток фосфорной кислоты
РНК
азотистое основание:
аденин, гуанин, тимин, урацил
углевод: рибоза С5Н10О5
остаток фосфорной кислоты
Дезоксирибонуклеиновая кислота (ДНК)
В 1951 году Э. Чаргаф сформулировал правила нуклеотидного состава ДНК:
1. Клетки разных тканей организма имеют одинаковый нуклеотидный состав ДНК.
2. Организмы одного вида имеют разный нуклеотидный состав.
3. В молекуле ДНК А=Т и Г=Ц, в свою очередь А+Г = Т+Ц. Для каждого вида организмов соотношение А+Г / Т+Ц является специфическим (у человека это соотношение равно 1,52).
Эти правила стали ключом для раскрытия макромолекулярной структуры ДНК.
Структура молекулы ДНК была впервые расшифрована Дж. Уотсоном и Ф. Криком в 1953 году. Согласно их модели, ДНК состоит из двух полинуклеотидных цепей, спирально закрученных одна относительно другой.
Мономерами этих цепей являются нуклеотиды. Нуклеотиды соединяются в цепочку путем образования фосфодиэфирных (ковалентных) связей между дезоксирибозой одного нуклеотида и остатком фосфорной кислоты другого, соседнего нуклеотида (рис.7.4.).
Две полинуклеотидные цепочки объеденяются в молекулу ДНК при помощи водородных связей между азотистыми основаниями нуклеотидов разных цепей. Азотистые основания соедины по принципу комплементарности. (аденин соединяется с тимином с помощью двух водородных связей, а гуанин с цитозином с помощью трех)

Рис.7.4. Принцип комлементарности
Принцип комплементарности – это одна из фундаментальных закономерностей живой природы, определяющая механизм передачи наследственной информации.
Полинуклеотидные цепочки одной молекулы являются антипаралельными, т.е. против 3′-конца одной цепочки находится 5′- конец другой цепочки.
Хотя в молекуле ДНК всего 4 типа разных нуклеотидов, благодаря их различной последовательности и огромному количеству в полипептидной цепочке достигается невероятное разнообразие молекул ДНК.
Нарушение в последовательности нуклеотидов в цепи ДНК приводит к наследственным изменениям в организме человека – мутациям. ДНК точно воспроизводится при делении клеток, что обеспечивает передачу наследственных признаков и свойств в ряде поколений и клеток.
Открытие «двойной спирали» ДНК было одним из самых выдающихся событий в истории биологии. Только через пять лет были получены первые экспериментальные подтверждения модели ДНК в работах М. Мезельсона и Ф. Сталя. После этих открытий наступило время невиданного прогресса в познании величайшей тайны природы – реализации наследственной информации. Началась эра молекулярной биологии.
Видовая специфичность ДНК
Представители разных видов отличаются между собой соотношением (А+Т) и (Г+Ц). У животных преобладает пара А+Т, в микроорганизмов соотношение (А+Т) и (Г+Ц) одинаковое. В этом и заключается видовая специфичность ДНК. Этот показатель используют как один из генетических критериев определения вида.
Структурные уровни ДНК
В ДНК выделяют первичную, вторичную и третичную структуру.
Первичная структура – это последовательность нуклеотидов в полинуклеотидной цепочке.
Вторичная структура – это двойная спираль полинуклеотидных цепей, соединённых водородными связями.
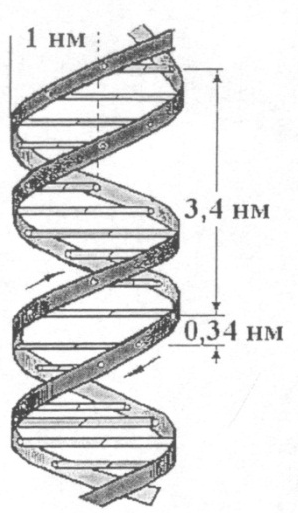 Существует несколько видов спиралей ДНК. В нормальных физиологических условиях наиболее часто встречается правозакрученная спираль В-формы. Это стандартная Уотсон – Криковская структура. Диаметр спирали 2 нм, шаг спирали 3,4 нм, каждый виток спирали содержит 10 пар оснований.
Существует несколько видов спиралей ДНК. В нормальных физиологических условиях наиболее часто встречается правозакрученная спираль В-формы. Это стандартная Уотсон – Криковская структура. Диаметр спирали 2 нм, шаг спирали 3,4 нм, каждый виток спирали содержит 10 пар оснований.
Наряду с В-формой обнаружены участки ДНК, имеющие другую конфигурацию, как правозакрученную (А- и С- формы)так и левозакрученную (Ζ-форма).
А-форма – полный оборот спирали составляет 2,8 2,8 нм, один виток имеет 11 пар азотистых оснований. ДНК в такой форме исполняет роль матрицы во время репликации.
С-форма имеет 9 пар оснований на виток спирали. Ζ-форма – это левая спираль, которая имеет 12 пар оснований на виток. Буква Ζ указывает на зигзагоподобную форму сахарно-фосфатного остова ДНК. В клетке ДНК обычно находится в В-форме, но отдельные участки могут находиться в А-Ζ – или даже иной конфигурации за счет суперспирализации ДНК. Конформация молекул ДНК зависит от условий и является одним из рычагов влияния на работу генов.
Третичная структура – это трехмерная суперспираль ДНК характерна для хромосом эукариот и обусловлена взаимодействием ДНК с ядерними белками. В большинстве прокариот, некоторых вирусов, а также в митохондриях и хлоропластах эукариот ДНК не связана с белками.
Основными свойствами ДНК являются её способности к репликации и репарации
Репликация ДНК
Репликация (ауторепродукция, аутосинтез, редупликация) – удвоение молекул ДНК при участии специальных ферментов. Она происходит перед каждым делением ядра в S-периоде интерфазы. Редупликация обеспечивает точную передачу генетической информации, заключенной в молекулах ДНК, от поколения к поколению.
Гигантские молекулы ДНК эукариот имеют много участков репликации – репликонов, тогда как относительно небольшие кольцевые молекулы ДНК прокариот представляют каждая один репликон. Полирепликативный характер огромных молекул ДНК эукариот обеспечивает возможность репликации без одновременной деспирализации всей молекулы. В остальном в общих чертах процессы репликации прокариот и эукариот весьма сходны.
Процесс репликации ДНК в репликоне происходит в 3 этапа, в которых участвуют несколько разных ферментов.
Первый этап. Репликация ДНК начинается с локального участка, где двойная спираль ДНК (под действием ферментов ДНК-геликазы, ДНК-топоизомеразы и др.) раскручивается, разрываются водородные связи и цепи расходятся. В результате образуется структура, названная репликационной вилкой (рис.7.5).

Рис.7.5. Схема репликации ДНК
На втором этапе происходит типичный матричный синтез. К образовавшимся свободным связям на материнских нитях ДНК присоединяются по принципу комлементарности (А-Т, Г-Ц) свободные нуклеотиды. Этот процесс идет вдоль всей молекулы ДНК. У каждой дочерней молекулы ДНК одна нить происходит от материнской молекулы, а другая является вновь синтезированной. Такая модель репликации получила название полуконс
Дата публикования: 2014-09-25; Прочитано: 9578 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
