 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Задача №1. Вещество А (табл.1) в количестве m г находится при T = 25 ºС и давлении p1 = 1,013 ·105 Па
|
|
Вещество А (табл.1) в количестве m г находится при T = 25 ºС и давлении p1 = 1,013 ·105 Па. Определить теплоту Q, работу A, изменение внутренней энергии DU и изменение энтальпии DH: а) при изотермическом расширении до объема V2 м3; б) при изобарном расширении до того же объема; в) при изохорном нагревании до достижения давления p2 Па; г) при адиабатическом сжатии до p 2 Па. Принять, что вещество А подчиняется законам идеальных газов. Истинную мольную теплоемкость вещества взять из справочника.
Таблица 1
| Вариант | А | m, г | V2, м3 | p2∙ 10–5, Па |
| Br2 | 0,5 | 1,30 | ||
| СО2 | 0,25 | 1,97 | ||
| N2 | 0,30 | 1,93 | ||
| Р4О10 | 0,12 | 1,95 | ||
| SО2 | 0,23 | 1,5 | ||
| Cl2 | 0,12 | 1,97 | ||
| BCl3 | 0,25 | 1,92 | ||
| BF3 | 0,10 | 1,40 | ||
| COCl2 | 0,28 | 1,99 | ||
| COS | 0,32 | 1,92 | ||
| O2 | 0,32 | 1,91 | ||
| NOCl | 0,40 | 1,96 | ||
| NO2 | 0,21 | 1,97 | ||
| N2O | 0,26 | 1,92 | ||
| N2O4 | 0,28 | 1,91 | ||
| N2O5 | 0,21 | 1,93 | ||
| PCl3 | 0,28 | 1,50 | ||
| PCl5 | 0,25 | 1,92 |
Продолжение таблицы1
| H2 | 0,20 | 1,96 | ||
| SO3 | 0,16 | 1,91 | ||
| SbCl3 | 0,18 | 1,90 | ||
| SiCl4 | 0,19 | 1,93 | ||
| SiCF4 | 0,24 | 1,91 | ||
| SiH4 | 0,32 | 1,97 | ||
| HJ | 0,36 | 1,60 | ||
| HF | 0,42 | 1,92 | ||
| HBr | 0,51 | 1,96 | ||
| HCl | 0,52 | 1,91 | ||
| HCN | 0,38 | 1,85 | ||
| ClO2 | 0,61 | 1,75 |
Решение:
Для двуокиси углерода CO2 в количестве 100 г, находящейся при температуре T = 0 ºС и давлении p = 1,013 ·105 Па, определим Q, A, DU и DH: а) при изотермическом расширении до объема 0,2 м3; б) при изобарном расширении до того же объема; в) при изохорном нагревании до достижения давления 2,026 ·105 Па; г) при адиабатическом сжатии до 2,026 ·105 Па.
Математическое выражение I-го закона термодинамики для процессов, связанных с бесконечно малыми изменениями состояния системы, имеет вид
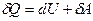 , (1)
, (1)
где Q – теплота; U – внутренняя энергия; A – работа.
Функции, которые однозначно определяют состояние системы, называют функциями состояния. Внутренняя энергия U, а также энтальпия H, которая выражается уравнением
 , (2)
, (2)
являются функциями состояния. Теплота Q и работа A служат формами передачи энергии и связаны с процессом, а не с состоянием системы, т.е. являются функциями процесса.
В двух частных случаях теплота и работа приобретают свойства функций состояния (закон Гесса):
 ; (V = const, T = const) (3)
; (V = const, T = const) (3)
 . (p = const, T = const) (4)
. (p = const, T = const) (4)
В интегральной форме математическое выражение I-го закона термодинамики имеет вид
 . (5)
. (5)
Для решения задачи примем, что CO2 подчиняется законам идеальных газов, а истинная мольная теплоемкость CO2 при постоянном давлении постоянна и равна 37,1 Дж/моль·К.
а) для изотермического расширения
∆U = 0 и ∆H = 0, следовательно Q = A.
Если из всех внешних сил на систему действует только внешнее давление p, то при переходе системы из состояния 1 в состояние 2 работу расширения можно вычислить по уравнению
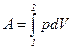 . (6)
. (6)
Для изотермического процесса
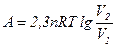 . (7)
. (7)
Определим число молей CO2 по формуле
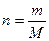 . (8)
. (8)
Число молей CO2 в 100 г составляет n = 100/44 = 2,27 моль.
Первоначальный объем определяем из уравнения Клапейрона – Менделеева
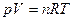 , (9)
, (9)
 = 2,27·8,314·273/1,013·105 = 0,0509 м3.
= 2,27·8,314·273/1,013·105 = 0,0509 м3.
Количество теплоты и работы определяем по уравнению (7)
Q = A = 2,3·2,27·8,314·273 lg (0,2/0,0509) = 7070 Дж = 7,07 кДж.
б) для изобарного процесса
 . (10)
. (10)
Отсюда Qp = ∆H = 2,27·37,1·273/0,0509 (0,2 – 0,0509) = 67400 Дж =
= 67,4 кДж.
Работа расширения газа в изобарных условиях
 , (11)
, (11)
A = 1,013·105 (0,2 – 0,0509) = 15000 Дж = 15,0 кДж.
Из уравнения (5) 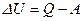 = 67,4 – 15,0 = 52,4 кДж.
= 67,4 – 15,0 = 52,4 кДж.
в) для изохорного процесса
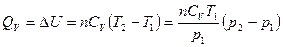 . (12)
. (12)
Выражение для взаимосвязи мольной теплоемкости идеальных газов при постоянном давлении Сp и при постоянном объеме CV имеет вид
 . (13)
. (13)
Теплоемкость при постоянном объеме
CV = Cp – R = 37,1 – 8,31 = 28,8 Дж/моль·К.
QV = ∆U = 2,27·28,8·273/1,013·105 (2,026 ·105 – 1,013·105) = 17900 Дж = = 17,9 кДж.
Из уравнения (2) для изохорного процесса имеем:
 .
.
Отсюда
∆H = 17,9 + 0,0509 (2,026 – 1,013) · 105 = 23100 Дж = 23,1 кДж.
г) для адиабатического сжатия
Q = 0 и A = – ∆U
 , (14)
, (14)
где 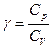 = 37,1/28,8 = 1,29.
= 37,1/28,8 = 1,29.
 = – 970 Дж = – 2,97кДж.
= – 970 Дж = – 2,97кДж.
Из уравнения (2) для адиабатического процесса
 .
.
Выражая конечный объем V2 из уравнения адиабаты  , получим
, получим
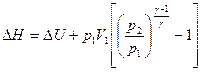 , (15)
, (15)
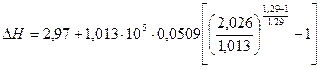 = 3830 Дж = 3,83кДж.
= 3830 Дж = 3,83кДж.
Дата публикования: 2014-11-18; Прочитано: 2786 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
