 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Правила Гунда
|
|
Стійкому стану атома відповідає такий розподіл електронів у межах енергетичного підрівня, при якому їх сумарний спін буде максимальним за абсолютною величиною  . Стійкий стан атома – це стан з найбільшим числом непарних електронів.
. Стійкий стан атома – це стан з найбільшим числом непарних електронів.
Наприклад: стійкій електронній будові атома Карбону 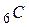 -
- 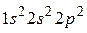 може відповідати тільки такий розподіл
може відповідати тільки такий розподіл
2р – електронів:

 = + 1/2 + 1/2 =1
= + 1/2 + 1/2 =1
1-е правило Клечковського: атомні орбіталі заповнюються в напрямку збільшення суми (n+ 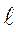 )
)
2-е правило Клечковського: у разі однакових сум (n+ 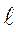 ) раніше заповнюється атомна орбіталь з меншим значенням головного квантового числа n
) раніше заповнюється атомна орбіталь з меншим значенням головного квантового числа n
Електронні аналоги – це елементи, валентні електрони яких розташовані на орбіталях, що описуються загальною для них електронною формулою.
Наприклад:
n  – електронні аналоги розташовані в ІА групі періодичної системи Li(2
– електронні аналоги розташовані в ІА групі періодичної системи Li(2  ), Na(3
), Na(3  ), K(4
), K(4  ), Rb(5
), Rb(5  ), Cs(6
), Cs(6  ), Fr (7
), Fr (7  )
)
n  – електронні аналоги розташовані в ІІІА групі періодичної системи B(2
– електронні аналоги розташовані в ІІІА групі періодичної системи B(2  ), Al(3
), Al(3  ), Ga(4
), Ga(4  )
)
(n-1)d2ns2 – електронні аналоги розташовані в ІVB групі періодичної системи Ti (3d24s2), Zr (4d25s2), Hf (5d26s2)
Дата публикования: 2014-11-18; Прочитано: 754 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
