 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Обработка результатов эксперимента. Для медного электрода
|
|
1. Вычислить величину 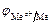 .
.
Для медного электрода
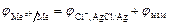 .
.
Для цинкового или свинцового электродов
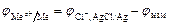 .
.
2. Для нахождения потенциала хлорсеребряного электрода при температуре опыта следует воспользоваться формулой:
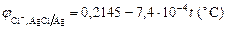 .
.
3. Стандартный электродный потенциал вычисляют из уравнения Нернста:
 ,
,
где 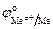 - стандартный потенциал металлического электрода;
- стандартный потенциал металлического электрода;  - активность иона данного металла, которую вычисляют по формуле:
- активность иона данного металла, которую вычисляют по формуле:  ;
; 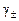 - средний ионный коэффициент активности, который рассчитывают в зависимости от значения ионной силы раствора по уравнениям:
- средний ионный коэффициент активности, который рассчитывают в зависимости от значения ионной силы раствора по уравнениям:
 при значении I < 0,05 моль/кг
при значении I < 0,05 моль/кг
и  при значении I > 0,05 моль/кг,
при значении I > 0,05 моль/кг,
где z + и z − – заряд катиона и аниона соответственно
или берут из справочной литературы, например, из [1].
6. Погрешность вычисления стандартного потенциала по экспериментальным данным Dφ0(эксп) вычисляют по уравнению:
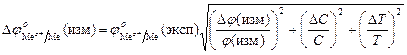 ,
,
где Dφ(изм) – погрешность измерения потенциала, Dφ(изм) = 1 мВ; D С – погрешность приготовления раствора, D С = 0,01; D Т - погрешность измерения температуры, D Т = 1 К.
7. Вычислить расчетную погрешность определения стандартного потенциала Dφo(расч) по формуле:
Dφo(расч) = |φo(эксп) - φo(табл)|,
φ0(табл) – берут из справочника.
8. Полученные данные занести в таблицу:
| Электрод | С, моль/кг | γ± | φo(эксп) | φo(табл) | Dφo(эксп) | Dφo(расч) |
Содержание отчета по лабораторной работе
1. Название работы.
2. Цель работы.
3. Ход эксперимента.
4. Экспериментальные данные (см. протокол к лабораторной работе).
5. Обработка экспериментальных данных.
6. Вывод.
Дата публикования: 2014-11-18; Прочитано: 287 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
