 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Метод Темкина–Шварцмана
|
|
Для практических целей приходится константу равновесия вычислять при температурах более высоких, чем стандартные. Для этого необходимо знать ΔGТ0, ΔНТ0 и ΔST0.
Значительные сокращения математических операций при подсчете указанных величин достигаются методом, предложенным М. И. Темкиным и Л. А. Шварцманом. Возьмем определенный интервал из уравнения Кирхгофа (1.33) в пределах от 298 до Т К, при этом получим
 . (1)
. (1)
Для расчета изменения энтропии химической реакции проинтегрируем в тех же пределах уравнение  , где вместо теплоемкости одного вещества следует подставить изменение теплоемкости Δ Ср системы:
, где вместо теплоемкости одного вещества следует подставить изменение теплоемкости Δ Ср системы:
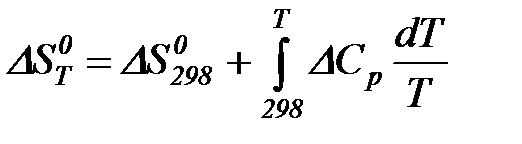 . (2)
. (2)
Значения (1) и (2) подставляем в уравнение 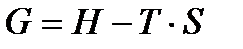 :
:
ΔGT0 = ΔНТ0 -Т ΔST0.
При этом получим
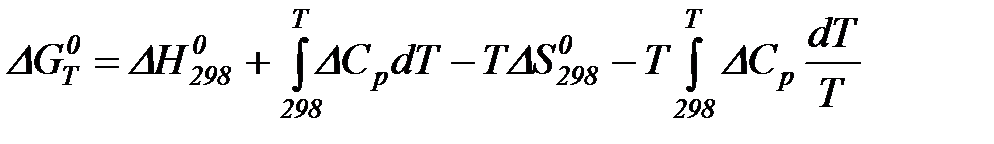 .
.
Подставим в подынтегральные выражения эмпирический степенной ряд:
ΔСр = Δа + Δв Т + ΔсТ2,
 .
.
Интегрируя, получим
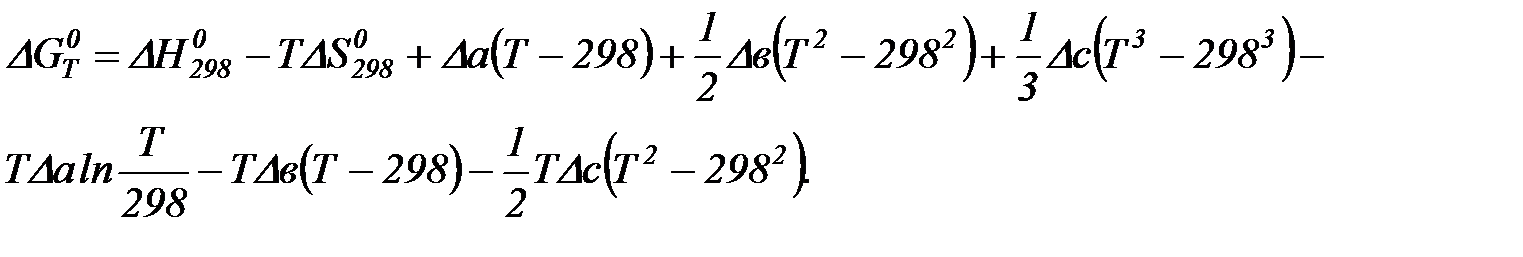
Раскроем скобки:

Сгруппируем члены относительно температурных коэффициентов Δа; Δв и Δс:


Обозначим:  ;
; 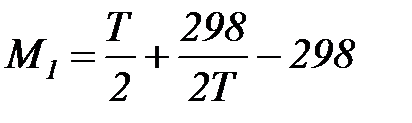 ;
;
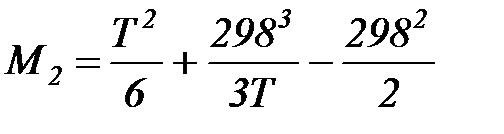 ;
; 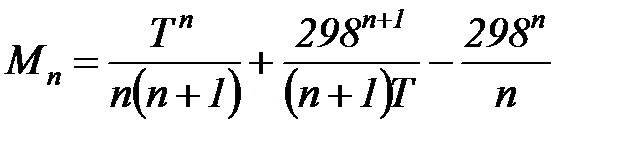 .
.
Подставив Мi в уравнение (4.22), получим
 .
.
Выражение для Мn справедливо, начиная с М1. Коэффициенты М0 … Мn зависят только от температуры. Они рассчитаны и представлены в справочной литературе.
Дата публикования: 2014-11-18; Прочитано: 5597 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
