 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Определение теплоты реакции нейтрализации
|
|
2 KOH + H2SO4 = K2SO4 + 2 H2O ∆Нонейтр. =?
Для определения теплоты процесса служит калориметр (рис.1).
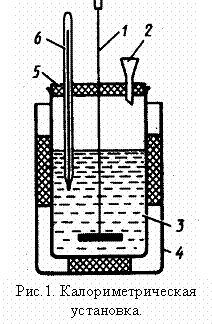
1 – мешалка; 2 – воронка; 3 – внутренний калориметрический сосуд;
4 – наружный калориметрический сосуд; 5 – крышка с тремя отверстиями; 6 – термометр.
Ход работы. Во взвешенный калориметрический стакан налейте 30 мл 1н раствора щелочи KOH, измерьте термометром температуру раствора до реакции (t1). В другой цилиндр налейте 30 мл 1н раствора H2SO4. Быстро влейте раствор кислоты в калориметр к раствору щелочи, осторожно перемешайте раствор и отметьте самую высокую температуру раствора (t2). Приняв теплоемкость раствора Ср = 4,18 Дж/(г∙град.), стекла Сс = 0,75 Дж/(г∙град.), зная массы раствора (60 г) и калориметрического стакана, вычислите количество теплоты, выделившейся в результате реакции (∆Н). Теплоту нейтрализации (стандартную энтальпию нейтрализации ∆Н0нейтр.) рассчитайте по формуле:
∆Н0нейтр. = ∆Н/n,
где n – количество вещества кислоты (или щелочи);
n = C.V = 1моль/л . 0,03 л = 0,03 моль.
Определите абсолютную и относительную ошибки опыта.
Справочная ∆Н0нейтр.= - 57,2 кДж/моль. Результаты опыта занесите в таблицу.
| № | Величина | Обозначение, ед. изм. | Значение |
| 1. | Масса калориметрического стакана | mc,г | |
| 2. | Начальная температура | t1, oC | |
| 3. | Конечная температура | t2, oC | |
| 4. | Теплоемкость системы | ∑С = Срmp+Ccmc, Дж/г) | |
| 5. | Количество выделившейся теплоты | ∆Н = - ∑С∙(t2- t1), Дж | |
| 6. | Теплота нейтрализации экспериментальная | ∆Н0нейтр = ∆Н/0,03, Дж/моль | |
| 7. | Абсолютная погрешность опыта | δ =∆Н0нейтр.теор.- ∆Н0нейтр.эксп. | |
| 8. | Относительная погрешность опыта | δотн. =│δ/∆Н0нейтр. теор.│∙100% |
Сделайте вывод. Объясните вероятные причины отклонений значения ∆Н0нейтр. экспериментального от теоретического.
7.4. Контроль усвоения темы занятия.
Дата публикования: 2014-11-04; Прочитано: 926 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
