 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Методика выполнения работы. Опыт №1. Приготовление раствора соляной кислоты заданной концентрации
|
|
Опыт №1. Приготовление раствора соляной кислоты заданной концентрации
Получить у преподавателя задание на приготовление раствора соляной кислоты определённой массовой доли из исходного раствора кислоты.
Для расчета объема исходной кислоты необходимо знать ее массовую долю и плотность раствора. Плотность раствора можно измерить с помощью ареометра. Кислоту наливают в цилиндр и опускают в нее ареометр так, чтобы он не касался стенок цилиндра. Ареометр представляет собой пустотелую закрытую стеклянную трубку с расширением на нижнем конце. В верхней части трубки находится шкала с делениями, соответствующими различным значениям плотности. Нижняя часть ареометра наполнена свинцовой дробью. Наблюдение нужно вести по нижнему краю мениска жидкости.
Далее, пользуясь данными табл. 4.1, определить массовую долю растворенного вещества в растворе исходной соляной кислоты.
Таблица 4.1
Соотношения массовых долей и плотностей раствора HCl (20єС)
| Массовая доля HCl W, % | Плотность раствора HCl, с, г/см3 |
| 4,0 | 1,019 |
| 8,0 | 1,039 |
| 12,0 | 1,059 |
| 16,0 | 1,079 |
| 20,0 | 1,100 |
| 24,0 | 1,121 |
| 28,0 | 1,142 |
Если в таблице нет замеренных значений плотности, то массовую долю необходимо вычислить методом линейной интерполяции. Пусть замеренная плотность раствора HCl равна 1,089. По табл. 4.1 выбрать значения плотности меньше и больше замеренного и соответствующие им массовые доли.
Найти разность в значениях массовой доли и плотности:
20,0% ---------1,100 г/см3
16,0%--------- -1,079 г/см3
20,0-16,0=4%--------1,100-1,079=0,021 г/см3
Затем из большего значения плотности вычесть замеренное значение (1,089 г/см3): 1,100-1,089 = 0,011 г/см3.
Составить соотношение:
4%-----0,021 г/см3
Х%-----0,011 г/см3
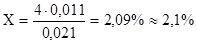 .
.
Полученное значение (2,1%) отнять от 20%:
Wисх(HCl) = 20,0-2,1=17,9%.
Это и будет массовая доля соляной кислоты, позволяющая рассчитать объем исходного раствора, необходимого для приготовления HCl заданной концентрации.
Далее рассчитать объем исходной кислоты и приготовить раствор. С помощью пипетки отмерить рассчитанный объем исходной кислоты HCl, перенести в мерную колбу и довести воду до заданного объема.
Опыт №2. Определение концентрации приготовленного раствора соляной кислоты методом кислотно-основного титрования
В три конические колбочки налить при помощи мерной пипетки по 1 см3
приготовленной соляной кислоты и добавить в каждую по 2–3 капли фенолфталеина. Поставить колбочку на лист белой бумаги. Постоянно перемешивая жидкость, приливать в нее из пипетки небольшими порциями раствор щелочи известной концентрации до появления слабо-розовой окраски раствора. В кислом растворе фенолфталеин бесцветен, а в слабощелочном растворе приобретает малиновую окраску. Появление окраски свидетельствует о полной нейтрализации кислоты щелочью.
Повторить титрование три раза и сделать расчет концентрации приготовленного раствора HCl (Соп). Определить относительную ошибку опыта, сравнивая Соп с заданной концентрацией Сm.
Результаты свести в табл. 4.2.
Таблица 4.2
Дата публикования: 2014-11-04; Прочитано: 383 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
