 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Теплоперенос в химических реакторах
|
|
Характер распределения температуры в химическом реакторе чрезвычайно важен при анализе протекающих в нем процессов, так как температура — один из основных параметров технологического режима. Во-первых, от температуры зависят состояние химического равновесия и предельно достижимая степень превращения реагентов (равновесная). Во-вторых, от температуры зависит скорость химических реакций. Кроме того, от температуры зависит селективность при проведении сложных реакций. Изменение температуры может привести к переходу гетерогенного процесса из кинетической области в диффузионную или наоборот. Нарушение равномерного распределения температуры в реакторе может привести к локальным разогревай, нежелательным побочным явлениям и т.д. Изменение температуры в реакторе в целом или изменение распределения температуры по объему реактора происходит вследствие протекающих в нем процессов, сопровождающихся выделением или поглощением теплоты, а также за счет теплообмена реактора с окружающей средой.
Существенное влияние на характер распределения температуры оказывает гидродинамическая обстановка в аппарате. Например, в реакторе идеального смешения, в силу допущений об идеальности все параметры процесса, в том числе и температура в данный момент времени одинаковы в любой точке реактора. Напротив, в реакторе вытеснения температура может быть разной в разных точках аппарата. Интенсивность перемешивания влияет и на интенсивность теплообмена в аппарате.
Уравнение теплового баланса. Тепловые режимы химических реакторов
В уравнении теплового баланса учитываются все тепловые потоки, входящие в реактор и выходящие из него. Такими потоками являются: 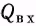 — физическая теплота реакционной смеси, входящей в элементарный объем, для которого составляется баланс (входной поток).
— физическая теплота реакционной смеси, входящей в элементарный объем, для которого составляется баланс (входной поток).  физическая теплота реакционной смеси, покидающей элементарный объем (выходной поток);
физическая теплота реакционной смеси, покидающей элементарный объем (выходной поток); 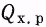 — теплота химической реакции (знак теплового эффекта зависит от того, происходит ли выделение или поглощение теплоты в результате химической реакции).
— теплота химической реакции (знак теплового эффекта зависит от того, происходит ли выделение или поглощение теплоты в результате химической реакции). 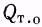 — теплота, расходуемая на теплообмен с окружающей средой (в зависимости от соотношения температур в реакторе и в окружающей среде или в теплообменном устройстве этот поток может быть также направлен и в объем и из него).
— теплота, расходуемая на теплообмен с окружающей средой (в зависимости от соотношения температур в реакторе и в окружающей среде или в теплообменном устройстве этот поток может быть также направлен и в объем и из него). 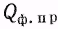 — теплота фазовых превращений.
— теплота фазовых превращений.
Для стационарного режима работы реактора алгебраическая сумма всех тепловых потоков равна нулю:
 (8.1)
(8.1)
В нестационарном режиме происходит положительное или отрицательное накопление теплоты в элементарном объеме:
 (8.2)
(8.2)
Уравнения (8.1) и (8.2) являются общими уравнениями теплового баланса химического реактора. в которых не происходит фазовых превращений.
Изотермический режим характеризуется тем, что температура реакционной смеси, входящей в реактор, равна температуре в реакторе и температуре смеси, покидающей реактор. Это возможно, если выделение или поглощение теплоты в результате химической реакции полностью компенсируется теплообменом с окружающей средой. Для стационарного изотермического режима при постоянстве физических свойств системы можно записать:
(8.3) 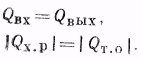 (8,4)
(8,4)
Адиабатический режим характеризуется полным отсутствием теплообмена с окружающей средой. В этом случае вся теплота химической реакции полностью расходуется на нагрев или охлаждение реакционной смеси. Для стационарного адиабатического режима
 (8.5)
(8.5)
Промежуточный режим характеризуется тем, что частично теплота химической реакции расходуется на изменение теплосодержания (нагрев или охлаждение) реакционной смеси, частично — на теплообмен с окружающей средой. Этот режим наиболее часто встречается в реальных химических реакторах. Промежуточный тепловой режим описывается полным уравнением теплового баланса 
Билет №26.
Вода и воздух в химической промышленности
Химическая промышленность является одним из крупнейших потребителей воды и воздуха. Эти виды сырья используются почти всеми химическими производствами для самых разнообразных целей. Вода применяется для получения водорода и кислорода, в качестве растворителя твердых, жидких и газообразных веществ; в качестве реакционной среды, экстрагента или абсорбента, транспортирующего агента; для нагревания и охлаждения веществ и аппаратуры; для образования пульп и суспензий; для промывки разных продуктов; очистки оборудования и т.п. Кроме того, вода широко используется в качестве рабочего тела в гидравлических, тепловых и атомных электростанциях.
Классификация природных вод и характеристика их примесей
Природные воды обычно подразделяют на атмосферные, поверхностные и подземные.
Атмосферные воды, выпадающие на землю в виде дождя и снега, содержат наименьшее количество примесей. В основном, это растворенные газы (О2, СО2, N и др.), соли, бактерии и т.д.
Поверхностные воды — это воды открытых водоемов: рек, озер, морей, каналов и водохранилищ. В состав этих вод входят разнообразные минеральные и органические вещества.
Морская вода представляет собой многокомпонентный раствор электролитов и содержит все элементы, имеющиеся в земной коре. В морской воде растворены многие соли (хлорид натрия до 2,6 %, хлорид и сульфат магния и др.), а также газы, входящие в состав воздуха (азот, кислород и углекислый газ).
Подземные воды — воды артезианских скважин, колодцев, ключей, гейзеров — характеризуются значительным содержанием минеральных солей, выщелачиваемых из почвы и осадочных пород, и небольшим количеством органических веществ.
В зависимости от солесодержания природные воды подразделяют на пресную воду — солесодержание до 1 г/кг; солоноватую — 1 — 10 и соленую — более 10 г/кг.
Промышленная водоподготовка
В процессе водоподготовки применяют механические, физические, химические и физико-химические методы: осветление, умягчение, ионный обмен, обескремнивание и дегазацию. Питьевую воду, кроме того, дезинфицируют. Осветление воды осуществляется в основном методами осаждения примесей, выделяющихся из воды в виде осадка. Эти методы называют также реагентными, так как для выделения примесей в воду вводят специальные реагенты. К процессам осаждения, применяемым для осветления воды, относятся коагуляция, известкование и магнезиальное обескремнивание.
Под коагуляцией понимают физико-химический процесс слипания коллоидных частиц и образования грубодисперсной микрофазы. флокул с последующим ее осажден нем. В качестве реагентов, называемых коагулянтами, обычно применяют сульфаты А12(5О4)3 и FeSO4.
Повышение эффекта коагуляции достигается при добавлении флокулянтов (полиакриламида, активной кремниевой кислоты и др.). При этом ускоряется образование хлопьев и улучшается их структура.
Образовавшуюся хлопьевидную массу, состоящую в основном из гидроксидов А1 и Fe и примесей, выделяют из воды в отстойниках или специальных осветлителях (осадок в них поддерживается во взвешенном состоянии потоком поступающей снизу воды), напорных или открытых фильтрах и контактных осветлителях с загрузкой из зернистых материалов (кварцевый песок, дробленый антрацит, керамзит), а также во флотаторах, гидроциклонах, намывных фильтрах. Известкование воды производится для снижения гидрокарбонатной щелочности воды. Одновременно с этим уменьшаются жесткость, солесодержание, концентрации грубодисперсных примесей, соединений железа и кремниевой кислоты.
Реагентом для этого процесса является гашеная известь Са(ОН)2, которая подается в воду в виде суспензии (известкового молока). Для повышения эффективности удаления кремниевой кислоты в воду добавляют каустический магнезит (70—80 % MgO).
Окончательная очистка от осадка осуществляется с помощью процесса фильтрования. Умягчением воды называется ее очистка от соединений кальция и магния, обусловливающих жесткость воды. Одним из наиболее эффективных способов умягчения воды является известково-содовый в сочетании с фосфатным. Процесс умягчения основывается на следующих реакциях:
1) обработка гашеной известью для устранения временной жесткости, удаления ионов железа и связывания СО2:
2) обработка кальцинированной содой для устранения постоянной жесткости:
3) обработка тринатрийфосфатом для более полного осаждения катионов Са2+ и Mg2+:
Растворимость фосфатов кальция и магния ничтожно мала, что обеспечивает высокую эффективность фосфатного метода.
В настоящее время для умягчения, обессоливания и обескремнивания воды широко применяется метод ионного обмена. Его сущность состоит в том, что твердое тело — ионит — поглощает из раствора электролита положительные или отрицательные ионы в обмен на эквивалентное количество других, одноименно заряженных ионов. В соответствии со знаком заряда обменивающихся ионов различают катиониты и аниониты.
Катиониты - практически нерастворимые в воде вещества, представляющие собой соли или кислоты с анионом, обусловливающим нерастворимость в воде; катион же (натрий или водород) способен вступать в определенных условиях в обменную реакцию с катионами раствора, в котором находится катионит. Катиониты соответственно называются Na-катионитами и Н- катионитами.
Аниониты — основания или соли с твердым нерастворимым катионом. Аниониты содержат подвижную гидроксильную группу (ОН-аниониты).
В качестве Na-катионитов применяют алюмосиликаты: цеолит, пермутит и др.; в качестве Н-катионитов — сульфоуголь, синтетические смолы; к ОН-анионитам относятся искусственные смолы сложного состава, например карбамидные.
Ионный обмен между раствором и ионитом имеет характер гетерогенной химической реакции. Следует отметить, что примеси, удаляемые из воды методом ионного обмена, не образуют осадка и что такая обработка не требует непрерывного дозирования компонентов.
Важная часть комплексного технологического процесса водоподготовки — удаление из воды растворенных газов. Наличие газов в воде объясняется как их сорбцией и протеканием химических реакций в процессе образования примесей в природной воде, так и появлением их в процессе различных стадий очистки. Эти газы можно разделить на химически нeвзаимодействующие (Н2, О2, СН4) и химически взаимодействующие с водой и ее примесями (NH3,CO2, С12), а также на коррозионно-активные (О2, СО2, NH3, C12, H2S) и инертные (N2, Н2, СН4). Концентрация газов в воде зависит от многих факторов; основные из них — физическая природа газа, степень насыщения, давление в системе и температура воды. Основной способ удаления из воды растворенных газов - десорбция (термическая деаэрация). Принцип ее заключается в создании контакта воды с паром, в котором парциальное давление газа, удаляемого из воды, близко к нулю, что является необходимым условием процесса десорбции. Этот процесс осуществляется в основном в деаэраторах (вакуумных, атмосферных, постоянного давления), которые по способу распределения воды и пара разделяют на струйные, пленочные и барботажные.
Для получения дистиллята, необходимого для производства химически чистых реактивов, лекарственных препаратов, проведения различных анализов, в лабораторной практике применяется термическое обессоливание воды. Этот процесс осуществляется в испарителях кипящего типа. При этом дистиллят производят в основном из воды, предварительно умягченной на ионитовых фильтрах.
Воздух.
Используют в основном как сырье или реагент в процессах, а также для энергетических целей. Воздух разделяют на компоненты ректификацией жидкого воздуха, получая при этом кислород, азот и инертные газы, которые используются затем в различных производствах и синтезах. Воздух, применяемый в качестве реагента подвергается специальной очистке от пыли, влаги, каталитических ядов. Воздух используется и как теплоноситель и хладоагент в тех процессах. Сжатый воздух применяется в различных барботажных смесителях, в форсунках для распыления жидкостей в реакторах и топках.
Билет №27
Энергетическая база химической промышленности
Современная химическая промышленность является одним из крупнейших потребителей топлива и электроэнергии; она широко использует тепловую, электрическую и механическую энергию. Тепловые процессы расходуют теплоту различных температурных потенциалов. По видам используемой тепловой энергии они подразделяются на высоко-, средне-, и низкотемпературные и криогенные процессы.
Высокотемпературные процессы до 773 К используют главным образом для изменения физико-химических свойств сырья или полуфабрикатов посредством их обжига, а также для интенсификации химических реакций. Эту энергию получают за счет сжигания различных видов топлива (угля и продуктов его переработки — кокса, доменного и коксового газа, жидкого топлива и природного газа), непосредственно в технологических устройствах.
Среднетемпературные (423—773 К) и низко-температурные (373—423 К) процессы используют тогда, когда необходимы физико-химические изменения свойств обрабатываемых материалов, для осуществления которых требуются повышенные температуры и давления. Это термический пиролиз и крекинг, выпарка, дистилляция, конверсия, сушка и обогрев в химической, нефтеперерабатывающей промышленности и ряде других отраслей; очистка и сортировка обрабатываемых материалов (мокрое обогащение железных руд, промывка материалов в химической, целлюлозно-бумажной, легкой промышленности и т.п.). Основными энергоносителями, обеспечивающими тепловой энергией средне- и низкотемпературные процессы, являются пар и горячая вода. Криогенные процессы протекают при температуре ниже 120 К (сжижение и отверждение газов) и используют для осуществления процессов криохимической технологии (процессы криокристаллизации, криоэкстрагирования, криоизмельчения и криозакалки, а также комбинирования влияния низких температур с другими физическими воздействиями).
Электрическая энергия применяется для проведения электрохимических (электролиз растворов и расплавов) и электротермических (нагревание, плавление, возгонка, синтезы при высоких температурах и др.) процессов. Электрическая энергия используется также для освещения и получения механической энергии.
Механическая энергия необходима главным образом для физических операций: дробления, измельчения, смешения, центрифугирования, работы насосов, компрессоров и вентиляторов, а также для различных вспомогательных операций (транспортировка грузов и т. п.). На расход энергоресурсов оказывают влияние правильный выбор сырья и методов его подготовки.
Тщательно подготовленное сырье (по химическому и агрегатному составу, содержанию примесей), как правило, обеспечивает снижение энергозатрат на процесс в целом.
Классификация топливно-энергетических ресурсов
Основными видами энергетических ресурсов в современных условиях являются горючие ископаемые (уголь, нефть, природный газ, торф, сланцы) и продукты их переработки; энергия воды (гидроэнергия); биомасса (древесина и другое растительное сырье); атомная энергия. Частично используется энергия ветра, а также морских приливов и отливов.
Энергетические ресурсы разделяют на топливные (уголь, нефть, природный газ, сланцы, битуминозные пески, торф, биомасса) и нетопливные (гидроэнергия, энергия ветра, лучистая энергия Солнца, глубинная теплота Земли и др.), возобновляемые и невозобновляемые, первичные и вторичные.
К практически неисчерпаемым относят геотермальные и термоядерные энергетические ресурсы. В геотермальные ресурсы включена глубинная теплота Земли. К невозобновляемым энергетическим ресурсам относятся те, запасы которых по мере их добычи необратимо уменьшаются. К ним относятся уголь, сланцы, нефть, битуминозные пески и природный газ. Все названные выше виды энергоресурсов относятся к первичным.
Вторичными энергетическими ресурсами (ВЭР) называется энергетический потенциал продукции, отходов, побочных и промежуточных продуктов, образующихся в технологических агрегатах, который не используется в самом агрегате, но может быть частично или полностью использован для энергоснабжения других агрегатов.
Вторичные энергетические ресурсы могут использоваться непосредственно без изменения вида энергоносителя для удовлетворения потребности в топливе или теплоте либо с изменением энергоносителя путем выработки теплоты, электроэнергии, холода или механической работы в утилизационных установках.
В зависимости от агрегатного состояния топливо подразделяют на твердое, жидкое и газообразное. К твердым топливам относятся бурые и каменные угли, антрациты, торф, сланцы и дрова, а также продукты их переработки: кокс, полукокс, брикеты торфяные и угольные, термоантрацит, древесный уголь; к жидким — нефть, газовый конденсат и продукты их переработки: бензин, керосин, дизельное топливо, мазут, смолы и т. п.
К газообразным - природный, нефтепромысловый (попутный) и шахтный газы, а также сжиженный нефтезаводской, коксовый, генераторный, водяной, водород и газы процессов брожения.
Технологические характеристики топлива
Теплота сгорания (теплотворность) — это теплота реакции горения топлива, т. е. количество теплоты, которое выделяется при полном сгорании 1 кг твердого или жидкого топлива (кДж/кг) или 1 м3 газообразного топлива (кДж/м3) и при охлаждении продуктов горения до начальной температуры процесса. Различают низшую Qн и высшую QB теплоту сгорания топлива. Низшей теплотой сгорания называется количество теплоты, выделяющееся при сгорании 1 кг водорода с образованием водяного пара. Высшей теплотой — количество теплоты, выделяющееся при сгорании I кг водорода с образованием воды.
Жаропроизводительность — максимальная температура горения, развиваемая при полном сгорании топлива без избытка воздуха, в условиях, когда вся выделяющаяся при сгорании теплота полностью расходуется на нагрев образующихся продуктов сгорания.
Жаропроизводительность положена в основу энергетической классификации топлива. В зависимости от жаропроизводительности топливо подразделяют на две группы: высокой (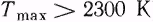 ) и пониженной (
) и пониженной (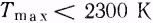 ) жаропроизводительности. К первой группе относятся природный, нефтезаводской, нефтепромысловый, сжиженный, коксовый, водяной, полуводяной газы, каменный уголь, кокс, антрацит, полукокс и древесный уголь. Ко второй группе относятся дрова, торф, бурые угли, сланцы, доменный воздушный, смешанный генераторный газы и газ подземной газификации углей.
) жаропроизводительности. К первой группе относятся природный, нефтезаводской, нефтепромысловый, сжиженный, коксовый, водяной, полуводяной газы, каменный уголь, кокс, антрацит, полукокс и древесный уголь. Ко второй группе относятся дрова, торф, бурые угли, сланцы, доменный воздушный, смешанный генераторный газы и газ подземной газификации углей.
Билет №28
Дата публикования: 2015-11-01; Прочитано: 870 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
