 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Контрольные задания 51- 60
|
|
51) Вычислить молярную концентрацию, молярную концентрацию эквивалентов и моляльность вещества в растворе, в котором массовая доля сульфата меди (II) равна 15 % (ρ = 1,108 г/см3).
52) В одном литре воды растворено 75 г карбоната натрия (ρ = 1,07 г/см3). Определить массовую долю, молярную концентрацию и титр растворенного вещества.
53) Сколько миллилитров 8,5 %-го раствора (ρ = 1,08 г/см3) гидросульфата натрия можно перевести в сульфат натрия с помощью 200 см3 1,5 н раствора гидроксида натрия?
54) Какой объем 0,1 н раствора гидроксида калия следует прибавить к 16,2 г 5 %-го раствора гидрокарбоната калия для образования карбоната калия?
55) Какой объем 0,3 н ортофосфорной кислоты должен прореагировать с 25 г 4 %-го раствора гидроксида натрия для образования дигидроортофосфата натрия?
56) К 100 мл 96 %-й серной кислоты (ρ = 1,835 г/см3) прибавили 400 мл воды. Получился раствор плотностью 1,220 г/см3. Вычислить массовую долю и молярную концентрацию эквивалентов раствора серной кислоты.
57) Какой объем 0,03 н раствора серной кислоты должен прореагировать с 25 мл 8 %-го (ρ = 1,08 г/см3) раствора гидроксида натрия для получения гидросульфата натрия?
58) Какой объем 0,2 н раствора соляной кислоты должен прореагировать с 200 мл 5 %-го раствора гидроксида бария (ρ = 1,05 г/см3) для получения хлорида гидроксобария?
59) Какой объем 0,2 н раствора карбоната натрия следует прибавить к 196 г 2,5 %-го раствора гидроксида бария для получения карбоната бария?
60) В какой массе воды надо растворить 67,2 л хлороводорода (н.у.), чтобы получить 9 %-ый раствор хлороводородной кислоты?
Методические указания:
Способы выражения концентрации растворов.
Массовая доля растворенного вещества ω (х) показывает массу вещества, содержащаюся в 100 г раствора.
ω(х)= 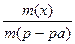 ;
; 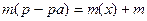 (растворителя)
(растворителя)
в процентах
ω(х)= 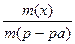 •100%
•100%
Молярная концентрация эквивалента показывает число моль растворенного вещества, содержащееся в 1 литре раствора
См= 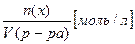 См=
См= 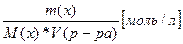
Молярная концентрация эквивалента показывает число
моль - эквивалентов, содержащееся в 1л. раствора

Дата публикования: 2015-11-01; Прочитано: 1165 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
