 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Процессы абсорбции и хемосорбции в гетерогенном катализе
|
|
Многочисленные исследования показали, что каталитическая реакция протекает на поверхности катализатора, поэтому для объяснения механизма катализа необходимо рассмотреть процесс адсорбции. Известно, что адсорбция – это процесс самопроизвольного изменения концентрации вещества на границе раздела фаз, сопровождающийся уменьшением свободной энергии Гиббса, т.е.  < 0.
< 0.
В гетерогенном катализе адсорбентом служит твердый катализатор, а адсорбатом – молекула реагирующего вещества. При этом различают физическую и химическую адсорбцию (хемосорбцию), хотя четкой грани между ними нет.
Физическая адсорбция всегда экзотермична, т.е.  <0. Это объясняется тем, что при физической адсорбции ворастает упорядоченность молекул реагента в адсорбционном слое, по сравнению с газовой или жидкой фазами, и поэтому энтропия всегда уменьшается, т.е.
<0. Это объясняется тем, что при физической адсорбции ворастает упорядоченность молекул реагента в адсорбционном слое, по сравнению с газовой или жидкой фазами, и поэтому энтропия всегда уменьшается, т.е.  <0. При этом в соответствии с уравнением Гиббса
<0. При этом в соответствии с уравнением Гиббса  =
=  – Т
– Т  необходимо, чтобы
необходимо, чтобы  <0.
<0.
Физическая адсорбция имеет невысокую специфичность, т.к. ее величина слабо зависит от химического состава поверхности катализатора. Ско-рость физической адсорбции слабо зависит от температуры, но количество адсорбированного вещества с ростом температуры быстро уменьшается (при р = const).
Хемосорбция – это поверхностная химическая реакция, которую можно рассматривать как химическое взаимодействие газа или растворенного веще-ства с поверхностью твердого катализатора, не сопровождающееся образова-нием объемной фазы.
Величины энтальпии хемосорбции, как и в любой химической реакции, лежат в широком интервале значений. Как правило, и здесь  <0. Но при хе-мосорбции энтропия адсорбции не всегда меньше нуля, поэтому принципиально возможна хемосорбция и с поглощением тепла. Хемосорбция, в от-личие от физической адсорбции, высоко специфична по отношению к хими-ческой природе адсорбента, и поэтому очень чувствительна к чистоте повер-хности катализатора.
<0. Но при хе-мосорбции энтропия адсорбции не всегда меньше нуля, поэтому принципиально возможна хемосорбция и с поглощением тепла. Хемосорбция, в от-личие от физической адсорбции, высоко специфична по отношению к хими-ческой природе адсорбента, и поэтому очень чувствительна к чистоте повер-хности катализатора.
Температурная область протекания хемосорбции не имеет ограничений и может протекать как при низких, так и при высоких температурах. С рос-том температуры количество хемосорбированного вещества уменьшается, а скорость процесса возрастает в соответствии с уравнением Аррениуса.
Из двух видов адсорбции только хемосорбция приводит к заметному изменению энергетического состояния адсорбированной молекулы и сущест-венному увеличению ее реакционной способности за счет снижения энергии активации, что и объясняет каталитический эффект. Но физическая адсорбция может предшествовать хемосорбции, и являться стадией каталитического процесса.
6.2.2. Теория адсорбции Лэнгмюра позволяет дать количественную оценку значимости процесса адсорбции, основанную на модели, предложен-ной автором. Лэнгмюр сделал следующие допущения:
- поверхность адсорбента состоит из определенного числа одинаковых адсорбционных центров;
- вероятность адсорбции на всехцентрах одинакова;
- каждый адсорбционный центр может удерживатьб только одну части-цу (молекулу или атом), поэтому процесс адсорбции заканчивается образованием на поверхности раздела фаз слоя толщинй в одну молекулу (мономо-лекулярный адсорбционный слой);
- силами притяжения и отталкивания между молекулами или атомами, адсорбированными на соседних центрах, можно пренебречь.
Из этих допущений следуют выводы:
- скорость адсорбции пропорциональна числу столкновений молекул адсорбата со свободными адсорбционными центрами на поверхности адсорбента;
- скорость десорбции пропорциональна числу занятых мест на поверхности адсорбента;
- скорость реакции между адсорбированными молекулами пропорциональна произведению величин адсорбции каждого из веществ.
Рассмотрим несколько механизмов адсорбции.
Механизм 1. Процесс хемосорбции вещества А из газовой фазы схематически можно представить следующим образом:
ka
 А(г) + s (А…..s)адс, (6.1)
А(г) + s (А…..s)адс, (6.1)
kd
где s – свободный адсорбционный центр поверхности адсорбента;
(А…..s)адс– адсорбированная частица или «зполненный» центр адсорбции;
ka – константа скорости адсорбции частицы А;
kd – константа скорости десорбции.
Для вывода кинетического уравнения процесса (реакции 6.1) введем понятие степени заполнения поверхности или доли занятых адсорбированными молекулами центров
 = а/ат, (6.2)
= а/ат, (6.2)
где а – величина адсорбции при заданном давлении;
ат – предельная величина адсорбции, равная емкости монослоя.
По закону действующих поверхностей скорость адсорбции va пропорциональна доле свободной поверхности и давлению газа:
va = kap (1 –  ), (6.3)
), (6.3)
где (1 –  ) – доля свободной поверхности.
) – доля свободной поверхности.
Скорость десорбции пропорциональна степени заполнения:
vd = kd  (6.4)
(6.4)
Общая скорость процесса адсорбции равна:
v= va – vd = kap (1 –  ) – kd
) – kd  (6.5)
(6.5)
После установления равновесия между газовой и адсорбционной фазами v= 0. Следовательно:
kap (1 –  ) = kd
) = kd  . (6.6)
. (6.6)
Решая соотношение 6.6 относительно  , и вводя константу адсорбци-онного равновесия, получим:
, и вводя константу адсорбци-онного равновесия, получим:
К = ka/kd, (6.7)
получаем уравнение изотермы Лэнгмюра
 = а/ат = Кр/ (1+ Кр). (6.8)
= а/ат = Кр/ (1+ Кр). (6.8)
Часто вместо К применяют введенную автором теории величину b, которую называют адсорбционным коэффициентом вещества А. Для обратимой адсорбции b имеет физический смысл константы равновесия между веществом на поверхности и в газовой фазе.
К = е  = е
= е  е
е  = bo e
= bo e  , (6.9)
, (6.9)
где bo – коэффициент, связанный с величиной энтропии адсорбции;
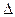 Gо адс – энергия Гиббса адсорбции;
Gо адс – энергия Гиббса адсорбции;
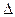 Ноадс – энтальпия адсорбции;
Ноадс – энтальпия адсорбции;
Q – теплота адсорбции.
Для реакции 6.1 условие адсорбционного равновесия выразим через химические потенциалы исходных и конечных продуктов:
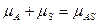 . (6.10)
. (6.10)
Для газовой фазы:
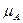 =
=  + RTln
+ RTln 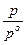 , (6.11)
, (6.11)
где р – давление компонента А в газовой фазе;
ро – стандартное давление; если его измеряют в атм. или бар, то ро = 1.
Для свободных адсорбционных центров:
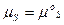 + RTln (1 –
+ RTln (1 –  ). (6.12)
). (6.12)
Для занятых адсорбционных центров:
 + RTln
+ RTln  . (6.13)
. (6.13)
Из условия адсорбционного равновесия можно записать:
 = RTlnр +
= RTlnр +  + RTln (1 –
+ RTln (1 –  ) =
) =  + RTln
+ RTln  . (6.14)
. (6.14)
Перегруппировав слагаемые в 6.14, получим:
RTln 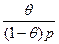 =
=  +
+  –
– 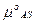 = –
= – 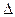 Goадс, (6.15)
Goадс, (6.15)
где 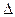 Goадс – изменение энергии Гиббса адсорбции.
Goадс – изменение энергии Гиббса адсорбции.
Величина 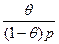 имеет физический смысл константы адсорбционного равновесия. Поэтому запишем:
имеет физический смысл константы адсорбционного равновесия. Поэтому запишем:
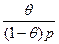 = К. (6.16)
= К. (6.16)
Решая уравнение 6.16 относительно  , которую нельзя измерить непо-средственно, приходим к уравнению Лэнгмюра:
, которую нельзя измерить непо-средственно, приходим к уравнению Лэнгмюра:
 = а/ат = Кр/ (1+ Кр). (6.17)
= а/ат = Кр/ (1+ Кр). (6.17)
Если равновесное давление остается достаточно малым, т.е. выполняется условие Кр << 1, то можно записать:
 = Кр. (6.18)
= Кр. (6.18)
Следовательно, в этом случае  растет пропорционально давлению (рис.6.1).
растет пропорционально давлению (рис.6.1).



 1
1

 = Кр/ (1+ Кр)
= Кр/ (1+ Кр)
 1/2
1/2
 = Кр
= Кр

 tg
tg  =K
=K
 1/К р
1/К р
Рис. 6.1. Изотерма адсорбции Лэнгмюра
Если равновесное давление достаточно велико, чтобы выполнялось условие Кр>> 1, то получаем:
 = 1. (6.19)
= 1. (6.19)
Это значит, что величина  не зависит от давления и поверхность полностью покрыта мономолекулярным слоем реагента. При этом наступает состояние насыщения.
не зависит от давления и поверхность полностью покрыта мономолекулярным слоем реагента. При этом наступает состояние насыщения.
Как следует из рис. 6.1, при значении р = 1/К, Кр = 1 и степень заполнения  =1/2. При этом касательная достигает значения
=1/2. При этом касательная достигает значения  = 1 именно в точке р =1/К.
= 1 именно в точке р =1/К.
Для нахождения параметров уравнения Лэнгмюра – величин предельной адсорбции ат и константы адсорбционного равновесия К – обработку за-висимости адсорбции а от давления р можно проводить тремя способами. Рассмотрим один из них.
Записав уравнение (6.17) в обратных величинах 1/ а и 1/ р, получим:
1/ а= 1/ ат + 1/ Кат . 1/ р. (6.20)
Из графика, построенного в координатах (1/ а, 1/ р), находим ат по отрезку l, отсекаемому прямой на оси ординат ат = 1/ l, и К – по тангенсу наклона прямой и указанному значению ат:
tg  = 1/ Kam и К = l/ tg
= 1/ Kam и К = l/ tg  .
.
Механизм 2. Адсорбция молекулы А2 сопровождается ее диссоциацией на атомы. Схематически это можно изобразить следующим образом:
A A
 |  |  |  |
 А2 + – s – s – – s – s – (6.21)
А2 + – s – s – – s – s – (6.21)
Далее запишем уравнение скорости адсорбции:
va = kap (1 –  A)2. (6.22)
A)2. (6.22)
Соответственно уравнение скорости десорбции таково:
vd = kd  A2. (6.23)
A2. (6.23)
В условиях равновесия va = vd и
kap (1 –  A)2 = kd
A)2 = kd  A2. (6.24)
A2. (6.24)
Решая (6.24) относительно  A и принимая, что К = ka/kd, получим:
A и принимая, что К = ka/kd, получим:
 A/(1 –
A/(1 –  A) = (Kp)1/2 (6.25)
A) = (Kp)1/2 (6.25)
или
 A = (Kp)1/2 / [1 + (Kp)1/2]. (6.26)
A = (Kp)1/2 / [1 + (Kp)1/2]. (6.26)
В начальный момент адсорбции, когда Kp<<1, то  A
A  р1/2. В дальнейшем для нахождения параметров уравнения (6.26) удобно применить ли-нейную зависимость в виде:
р1/2. В дальнейшем для нахождения параметров уравнения (6.26) удобно применить ли-нейную зависимость в виде:
 A– 1 = 1 + (Кр)1/2. (6.27)
A– 1 = 1 + (Кр)1/2. (6.27)
Механизм 3. Рассмотрим случай, когда при однвременной адсорбции двух газов происходит их конкуренция за адсорбционные центры. Пусть  A и
A и  В – степени заполнения поверхности соответственно молекулами А и В (без их диссоциации), рА и рВ – парциальные давления этих газов. Тогда выражения адсорбции и десорбции примут вид:
В – степени заполнения поверхности соответственно молекулами А и В (без их диссоциации), рА и рВ – парциальные давления этих газов. Тогда выражения адсорбции и десорбции примут вид:
va,A = ka,A (1 –  A –
A –  B); (6.28)
B); (6.28)
va,B = ka,B (1 –  A –
A –  B); (6.29)
B); (6.29)
vd,A = kd,A  A; (6.30)
A; (6.30)
vd,B = kd,B  B. (6.31)
B. (6.31)
При равновесии va = vв. Обозначив:
КА = 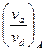 и КВ =
и КВ = 
и решая систему уравнений относительно  A и
A и  В, получим:
В, получим:
 A =
A =  ; (6.32)
; (6.32)
 В =
В =  . (6.33)
. (6.33)
Если КАрА = 1 и КВрВ = 1, то  A
A  рА и
рА и  В
В  рВ.
рВ.
Если один из газов сильно адсорбируется, например КАрА >>1 + КBрB, тогда  A = 1, а
A = 1, а  В
В  рВ / рА, т.е. адсорбция вещества В замедляется адсорбцией вещества А.
рВ / рА, т.е. адсорбция вещества В замедляется адсорбцией вещества А.
6.2.3. Нелэнгмюровская адсорбция. Во многих случаях реальная ад-сорбция не описывается уравнением Лэнгмюра. Причинами, объясняющими отклонения от модели Лэнгмюра, могут быть энергетическая неоднородность поверхностей катализаторов, что приводит к зависимости теплот адсорбции от степени заполнения поверхности адсорбента: уменьшению теплоты адсорбции по мере увеличения степени заполнения; наличие сил притяжения-отталкивания между адсорбированными молекулами.
Ряд авторов предложили уравнения, описывающие частные случаи адсорбции. Среди них следует выделить следующие уравнения.
1. Изотерма Генри.
 = Кр, (6.34)
= Кр, (6.34)
которая в ряде случаев представляет собой начальный участок изотермы Лэн-гмюра и может выполняться в небольшом интервале степеней заполнения.
2. Изотерма Фрейндлиха.
 = С 1 р1/С
= С 1 р1/С 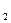 , (6.35)
, (6.35)
где С1 и С2 – постоянные, причем С2 >1.
Изотерму Фрейндлиха часто применяют для описания хемосорбции газов на металлах в области средних заполнений, когда 0,3 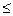

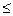 0,7.
0,7.
3. Логарифмическая изотерма (изотерма Темкина):
 = с 1ln(c/p) (6.36)
= с 1ln(c/p) (6.36)
или
 = С1 + С 2ln p, (6.37)
= С1 + С 2ln p, (6.37)
где с1; с2; С1 и С2 – постоянные.
Следует отметить, что эмпирические выражения (6.36) и (6.37) можно получить как в предположении неоднородности поверхности катализатора, так и при учете сил межмолекулярного взаимодействия.
При физической адсорбции, когда энергии межмолекулярных связей соизмеримы, после насыщения первого адсорбционного слоя может наступать полимолекулярная адсорбция с образованием второго и последующих адсорбционных слоев. Полимолекулярная адсорбция наблюдается во многих процессах с участием органических веществ при повышенных давлениях.
Модель для описания полимолекулярной адсорбции предложили С. Брунауэр, П. Эммет и Э. Теллер. Ее основные допущения таковы:
- учитывается только минимальная совокупность парных взаимодействий молекул, которая может привести к возникновению полимолекулярного слоя;
- при значительной разнице в теплотах адсорбции первого и последующих слоев принимается, что
К2 = К3 = К4 = …= Кконд = рs– 1, (6.38)
где К2; К3; К4 и т.д. – константы равновесного взаимодействия пары частиц во втором и далее слоях;
Кконд – константа равновесия процесса конденсации;
Рs – давление насыщенного пара сорбата при температуре опыта.
Уравнение полимолекулярной адсорбции, названное БЭТ (аббревиатура от фамилий авторов модели), имеет следующий вид:
а=  . (6.39)
. (6.39)
Для определения параметров ат и С уравнение БЭТ приводят к линей-ному виду:
y =  . (6.40)
. (6.40)
Строя графическую зависимость в координатах (y, р/рs), находят величину отрезка, отсекаемого на оси ординат, l = 1/amC, и тангенс угла наклона прямой:
tg  =
=  = (C – 1) l.
= (C – 1) l.
С помощью этих данных легко находят искомые параметры:
ат = (1 + tg  )– 1 и С = 1 + tg
)– 1 и С = 1 + tg  / l.
/ l.
Зная ат, можно рассчитать доступную поверхность адсорбента S, если известна эффективная площадка s, занимаемая молекулой адсорбата в плотном слое:
S = amsNA / (6.41)
Считается, что уравнение БЭТ применимо для определения поверхности с точностью 5–10 %, если С > 40. В этих условиях описание полимолекулярной адсорбции до значений p/ps <0,3–0,4 с помощью уравнения БЭТ является достаточно точным.
Использование уравнения БЭТ оказало большое влияние на теорию и практику катализа, позволило установить количественную связь между скоростью каталитических процессов и величиной поверхности катализаторов.
На макропористых адсорбентах, например цеолитных и алюмосиликатных катализаторах, молекулы адсорбата проникают в глубь кристаллической решетки, характеризующейся наличием полостей. Поэтому понятие поверхностной адсорбции здесь неприменимо. В данном примере оценку величины адсорбции проводят с помощью уравнения из теории объемного заполнения М.М. Дубинина:
lg W = lg  , (6.42)
, (6.42)
где W – адсорбированный объем (в жидком состоянии);
Wo – объем пор;
В – константа;
р – равновесное давление адсорбата при температуре Т;
ps – давление насыщенных паров адсорбата при температуре Т.
Применение уравнения (6.42) ограничено низкими значениями ps/p. Для описания адсорбции на цеолитах часто используют эмпирическую формулу:
А = 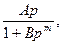 (6.43)
(6.43)
где А; В; т – константы для данного вида адсорбата, причем 0 < m < 1.
Дата публикования: 2015-10-09; Прочитано: 1223 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
