 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Интенсификация гомогенных процессов
|
|
Если реакция протекает в объеме фазы, то она называется гомогенной. К гомогенным реакциям относят, например, реакции в растворах. В гомогенных системах реакция протекает во всем объеме реактора. Скорость реакции в таких процессах можно интенсифицировать изменением состава реакционной среды, температуры и давления.
Влияние состава реакционной среды зависит от величины концентрации реагентов и их физико-химических свойств.
Согласно закону действующих масс уравнение скорости для гомогенной реакции типа aA + bB 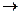 cC + dD записывается так:
cC + dD записывается так:
(– VA) = kCaACbB., (5.1)
где V A – скорость химической реакции;
СА, СВ – молярные концентрации реагентов А и В;
a, b – порядок реакции по реагентам А и В;
k – константа скорости реакции.
Таким образом, скорость реакции пропорциональна произведению кон-центраций реагентов, взятых в степенях, равным порядку реакции, на основе чего следуют выводы:
- чем выше значение концентраций, тем больше скорость реакции;
- скорость реакции в большей степени зависит от реагента, входящего в уравнение скорости с большей степенью;
- если одновременно протекают реакции с разными порядками, то из-менение концентрации сильнее скажется на скорости реакции с более высоким порядком.
Данные закономерности лежат в основе технологического приема – из-бытка одного из реагентов. При этом выгоднее в избытке брать реагент, входящий в уравнение реакции с более высоким стехиометрическим коэффициентом. Но существует ряд причин, по которым во многих газофазных и жид-кофазных процессах реагенты разбавляют растворителем, т. е. понижая их концентрацию. Этому есть несколько причин:
- возможность перегрева реакционной массы при проведении сильно экзотермической реакции с большой скоростью;
- использование низких концентраций – требование селективного тече-ния сложных реакций, если побочная реакция более высокиого порядка;
- улучшения условий протекания сопровождающих реакцию физических процессов, т. к. разбавление позволяет понизить вязкость, облегчить равномерное перемешивание реакционной массы и ее транспорт, обеспечить более интенсивный и равномерный теплообмен.
Влияние температуры на скорость реакции описывается уравнением Аррениуса:
 k = A . е –E /RT (5.2)
k = A . е –E /RT (5.2)
где k – константа скорости;
А – предэкспоненциальный множитель;
Е – энергия активации, кДж/моль;
R – газовая постоянная, кДж/моль;
Т – температура, К.
Из этого уравнения следует, что, поскольку температура входит в показатель степени, то она оказывает очень большое влияние на скорость реакции. По этой же причине существенно влияние на скорость значение энергии активации, но с другим знаком.
Применяемый в химической технологии диапазон давлений очень широк. В нефтепереработке в большой части процессов давление составляет в пределах 1–5 МПа, но есть процессы с давлением до 32 МПа (гидрокрекинг) и в вакууме (ректификация мазута). В нефтехимии известны процессы, про-текающие при давлении до 100 МПа (полимеризация этилена). Имеется несколько причин, по которым повышенное давление, несмотря на высокие энергозатраты, широко применяется в химической технологии:
1. Давление существенно повышает скорость газофазных процессов, т.к. в этом случае резко повышается концентрация реагентов.
2. Давление влияет на положение химического равновесия для обрати-мых реакций, при этом повышение давления смещает равновесие в сторону прямой реакции, если процесс протекает с уменьшением объема.
3. Давление повышает температуры кипения и плавления. Этот эффект используется для проведения процессов в жидкой фазе для веществ, которые при стандартном давлении находятся в газообразном состоянии.
4. Повышение давления во многих случаях позволяет снизить темпера-туру синтеза, что важно в системах с низкой термостабильностью реагентов или продуктов процесса.
Дата публикования: 2015-10-09; Прочитано: 1752 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
