 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Технологические свойства гетерогенных катализаторов
|
|
Основными среди них являются активность (А) и селективность (S) и производительность (П).
6.6.1. Активность (кг/м2 ч) – общая скорость реакции на катализаторе и она может быть рассчитана по формуле
А = Gп / F 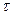 , (6.71)
, (6.71)
где Gп – количество преврашенного реагента за время 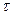 на единице поверхности F.
на единице поверхности F.
Активность катализатора характеризуется мерой его ускоряющего воздействия по отношению к данной реакции.
Время от момента загрузки свежего катализатора в реактор до момента выгрузки отработанного катализатора из реактора называется циклом его работы. Активность катализатора неодинакова в разные периоды эксплуатации катализатора.
Весь цикл работы катализатора, связанный с изменением его активно-сти, можно разделить на три периода:
- разработка катализатора;
- период постоянной активности – срок жизни катализатора;
- дезактивация катализатора.
В период разработки происходит самопроизвольный рост активности катализатора под воздействием реакционной среды.
Период постоянной активности для разных катализаторов может ме-няться в широких пределах: от нескольких минут до нескольких лет, требо-вания к сроку жизни катализатора определяются стоимостью замены дезак-тивированного катализатора свежим катализатором и возможностью его регенерации. При высокой стоимости замены сокращение числа этих операций дает весьма ощутимый экономический эффект.
Период падения активности катализатора связан с его дезактивацией, которая может быть обусловлена явлениями старения, утомления, зауглероживания, синтеринга, отравления контактными ядами.
Старение – это естественный процесс, при котором активность постепенно уменьшается по всему слою катализатора. Старение может быть вызвано различными факторами, например, длительным воздействием высоких температур, истиранием частиц катализатора при трении друг о друга. Как правило, быстрее стареют более мелкие частицы твердого катализатора.
Утомление – это неравномерное падение активности в слое катализатора – опасный процесс, т.к. проявляется задолго до истечения срока жизни катализатора в результате неправильной его загрузки и эксплуатации. Утомление характерно для процессов в стационарном слое катализатора.
Зауглероживание происходит в процессах переработки углеводородного сырья. Катализатор покрывается углеродистыми отложениями (коксом) в форме высококонденсированных ароматических структур, которые образу-ются в результате глубоких химических превращений. Среди подобных процессов можно назвать каталитический крекинг и риформинг, гидрокрекинг, дегидрирование и изомеризацию. Отложения кокса блокируют поверхность катализатора, вследствие чего его активность резко снижается за короткое время, которое иногда составляет 10–30 мин. Зауглероженный катализатор поддается восстановлению. Например, в процессе каталитического крекинга восстановление зауглероженного катализатора достигается в регенераторе при повышенной температуре путем выжига кокса кислородом воздуха.
Синтеринг (спекание) обычно является результатом окислительной регенерации, во время которой температура катализатора достигает 600 о С и выше, либо следствием высокотемпературного процесса с плохо организованным теплоотводом. Спекание сокращает величину активной поверхности в результате укрупнения кристаллитов металлического или оксидного катализатора и повышает гидравлическое сопротивление аппарата. Поэтому одной из задач в решении этой проблемы является стабилизация структуры компонентов катализатора. Стабилизация осуществляется путем структурного про-мотирования. Таким промотором, например, при синтезе аммиака служит оксид алюминия Al2O3, который, внедряясь между кристаллами железа, пре-дотвращает их агломерацию. Аналогичное действие оказывает на никелевый катализатор в процессе гидрирования углеводородов оксид хрома Cr2O3 . Не менее важной является также стабилизация носителя, ибо он обеспечивает металлическому катализатору высокоразвитую поверхность.
Отравление – это частичная, либо полная потеря активности катализа-тора под действием веществ, называемые контактными ядами. При отравле-нии наблюдается специфическое действие яда по отношению и к катализатору, и к самой реакции.
Механизм отравления металлических катализаторов контактными ядами может быть связан:
- с воздействием молекул, содержащих неметаллы N, P, As, O, S, Se. Это могут быть и свободные элементы из этой группы, кроме азота. Они связывают металл катализатора за счет неподеленных электронных пар (сероводород, тиофен, арсин, фосфин и др.);
- с отсоединением металлов (ионов Hg, Pb, Bi, Sn, Cd, Fe и т.д.) с последующим образованием интерметаллических соединений с участием d- электронов;
- с воздействием молекул, содержащих кратные связи (СО, НСN и др.), с более высокими адсорбционными характеристиками, чем другие вещества реакционной массы.
Катализатор защищают от контактных ядов несколькими приемами:
- переводом яда в неактивное состояние;
- очисткой сырья от контактных ядов на стадии его подготовки;
- применением катализаторов, устойчивых к контактным ядам.
В качестве примера применения первого способа защиты можно привести прием удаления СО, содержащегося в поступающем на синтез аммиака водороде, с помощью самого водорода (СО – контактный яд для железного катализатора):
ZnO

 СО + 3Н2 CH4 + H2O (6.72)
СО + 3Н2 CH4 + H2O (6.72)
Получаемый метан – инертная примесь к водороду и поэтому не представляет вреда для катализатора.
Примером второго способа защиты платинового катализатора процесса риформинга является предварительная гидроочистка бензиновых фракций от серо-, азот- и кислородсодержащих соединений перед направлением их на платформинг:
RSH + H2 = RH + H2S (6.73)
RNH2 + H2 = RH + NH3 (6.74)
ROH + H2 = RH + H2O (6.75)
Приведенные выше реакции протекают на стойком к действию катали-тических ядов алюмо-кобальт-молибденовом катализаторе (АКМ).
Именно разработка каталитических композиций, стойких к ядам, является наиболее интересным и перспективным направлением совершенствования каталитических систем.
Указанные выше способы защиты катализаторов от ядов не являются независимыми друг от друга и поэтому могут применяться в одном процессе одновременно.
Еще одной причиной падения активности катализатора является отложение на его поверхности минеральных примесей, содержащихся в сырье. Эти примеси хемосорбируются, изменяя химический состав поверхности катализатора.
6.6.2. Селективность (избирательность) – важнейший показатель качества катализатора, который заключается в преимущественном ускорении им целевой реакции в сравнении с побочными реакциями. Она измеряется величиной относительной скорости образования целевого продукта:
S = – VA / R = – VA / A, (6.76)
где VА – скорость образования целевого продукта, рассчитанная по реагенту А;
A=R – общая скорость реакции (активность).
Если одновременно возможно протекание нескольких параллельных реакций, то можно подобрать для каждой из них собственные селективные катализаторы. Например, дегидратация этанола может протекать в присутствии оксида алюминия или оксида тория преимущественно с образованием этилена и воды:

 С2Н5ОН Н2О + С2Н4 (6.77)
С2Н5ОН Н2О + С2Н4 (6.77)
В присутствии металлических катализаторов (серебра, меди и др.) этанол практически полностью дегидрируется:

 С2Н5ОН СН3СНО + Н2 (6.78)
С2Н5ОН СН3СНО + Н2 (6.78)
В присутствии бифункционального катализатора (Al2O3 + ZnO) с достаточно высокой скоростью идут реакции дегидратации и дегидрирования с образованием 1,3-бутадиена:

 2С2Н5ОН 2Н2О + С4Н6 + Н2 (6.79)
2С2Н5ОН 2Н2О + С4Н6 + Н2 (6.79)
Величина селективности может изменяться довольно в широких пределах, в зависимости от самого катализатора и от технологического процесса. Принято считать приемлемой селективность величиной не менее 0,85.
Селективность зависит от многих факторов. Один из них – число коор-динационных мест у активного атома поверхности. Наибольшей селективностью обладают катализаторы кристаллической структуры с большей однородностью активных центров. Другими факторами, влияющими на селективность, являются природа и структура носителей, а также природа сырья. К примеру, нефтехимическое и углехимическое сырье различаются по групповому составу и характеру примесей. Поэтому промышленные катализаторы должны обладать достаточной гибкостью к переработке сырья разного состава без потери селективности.
6.6.3. Производительность. Ее измеряют количеством продукта, которое можно получить в единицу времени с единицы объема катализатора и измеряют в кг/ ч · м3.
П =  (6.80)
(6.80)
6.6.4. Температура зажигания катализатора (Т з) – это минимальная температура, при которой процесс начинает протекать с достаточной для технологических целей скоростью. Чем выше активность катализатора, тем ниже температура зажигания. Они связаны формулой:
Тз = 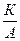 , (6.81)
, (6.81)
где К – константа, определяемая природой катализатора.
При низкой температуре зажигания расширяется рабочий интервал между Т з и режимной температурой процесса, упрощается конструкция реактора, сокращаются энергетические затраты, стабилизируется технологичес-кий режим. Для экзотермических процессов при некотором значении Т з количество выделяющегося тепла становится равным отводимому теплу. В этом случае Т з является той минимальной температурой, при которой обеспечивается автотермичность процесса.
Особенно важно иметь невысокую температуру зажигания катализатора для проведения обратимых экзотермических реакций, когда невысокие температуры проведения процесса позволяют сместить равновесие в сторону получения ее продуктов.
6.6.5. Механическая прочность катализатора должна быть такой, чтобы он не разрушался под собственной массой в реакторах со стационарным слоем катализатора и не истирался в процессах с кипящим слоем катализатора. Именно из-за отсутствия износостойких катализаторов зачастую сдерживается перевод ряда химико-технологических процессов из стационарного в кипящий слой катализатора.
6.6.6. Термостойкость катализатора. К этому показателю требования достаточно жесткие. Катализатор должен выдерживать перегрев в 50–100 о С выше регламентной. Это важно с точки зрения возможности регенерации катализатора. К примеру, в каталитическом крекинге углеводородного сырья рабочая температура в реакторе равна 480–530 о С, а температура регенерации катализатора – 600–620 о С.
Дата публикования: 2015-10-09; Прочитано: 1768 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
