 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Химический состав сухого воздуха в приземном слое
|
|
| № п/п | Газ | Концентрация, % | |
| объемная | массовая | ||
| Азот | 78,09 | 75,5 | |
| Кислород | 20,95 | 23,1 | |
| Аргон | 0,932 | 1,286 | |
| Оксид углерода (IV) | 0,032 | 0,046 | |
| Неон | 1,8 .10–3 | 1,3. 10–3 | |
| Гелий | 4,6. 10–4 | 7,2. 10–5 | |
| Криптон | 1,1. 10–4 | 2,9. 10-4 | |
| Оксид азота (I) | 5,0. 10–5 | 7,7. 10–5 | |
| Водород | 5,0. 10–5 | 7,6. 10–6 | |
| Озон | 2,0. 10–7 | 3,3. 10–6 |
В практических расчетах, не требующих большой точности, принимают, что воздух содержит, % об. (% масс.): азота 79 (77) и кислорода 21 (23).
2.4.1. Воздух как реагент. Как было упомянуто в начале этой главы, воздух ширко применяют в химической технологии как окислитель, содержащий кислород. Примерами таких процессов могут служить реакции:
1. Hедеструктивного окисления, в которых число атомов углерода в образующемся кислородсодержащем соединении такое же, как в исходном соединении, например:
0,5O2

 RCH2CH3 R(ОН)CHCH3; (2.11) одноатомный спирт
RCH2CH3 R(ОН)CHCH3; (2.11) одноатомный спирт

 O
O




 HC – CH3 HC – C
HC – CH3 HC – C
 3O2 O + 3Н2О; (2.12)
3O2 O + 3Н2О; (2.12)


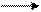 HC – CH3 HC – C
HC – CH3 HC – C
O
2-бутен малеиновый ангидрид
 |





 0,5О2 ОН циклогексанол; (2.13) О2
0,5О2 ОН циклогексанол; (2.13) О2
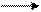

 циклогексан О + Н2О
циклогексан О + Н2О
 циклогексанон
циклогексанон

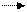




 СН3 + 1,5О2 СООН + Н2О. (2.14)
СН3 + 1,5О2 СООН + Н2О. (2.14)
толуол бензойная кислота
2. Деструктивного окисления (с расщеплением связей С – С):
2,5О2
 СН3СН2СН2СН3 2СН3СООН + Н2О; (2.15)
СН3СН2СН2СН3 2СН3СООН + Н2О; (2.15)
бутан уксусная кислота

 О
О


 НС – С
НС – С




 4,5О2 О + 2Н2О + 2СО2; (2.16)
4,5О2 О + 2Н2О + 2СО2; (2.16)

 НС – С
НС – С
О
бензол малеиновый ангидрид
 2,5О2
2,5О2
 НООС(СН2)4СООН + Н2О. (2.17)
НООС(СН2)4СООН + Н2О. (2.17)
циклогексан адипиновая кислота
3. Окислительной конденсации (окислительное сочетание) – окисление, сопровождающееся связыванием исходных компонентов:
1,5O2
 2RH ROOR + H2O; (2.18)
2RH ROOR + H2O; (2.18)
алкан пероксид
1,5O2
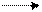 RCH3 + NH3 RCN + 3H2O; (2.19)
RCH3 + NH3 RCN + 3H2O; (2.19)
алкан аммиак нитрил
1,5О2
 СН2 = СН – СН3 + NH3 СН2 = СН – С
СН2 = СН – СН3 + NH3 СН2 = СН – С  N + 3Н2О. (2.20)
N + 3Н2О. (2.20)
акрилонитрил
Воздух, применяемый в качестве реагента, необходимо очищать от пыли, влаги и контактных ядов. Такую очистку ведут в промывных башнях жидкими поглотителями (щелочами, водой, этаноламинами, раствором аммиака), мокрых и сухих фильтрах, аппаратах с твердыми адсорбентами.
Существует два источника загрязнения атмосферы: естественный и антропогенный. Второй источник наиболее опасный. Он имеет место в результате вредных выбросов электроэнергетики, цветной и черной металлургии, нефтедобывающей и нефтеперерабатывающей промышленности и других от-раслей хозяйственной деятельности человека. В табл. 2.4 приведены объемы вредных выбросов промышленности России в 1996–2002 г.г. (тыс. т).
2.4.3. Воздух как теплоноситель. Несмотря на низкую теплопроводность, воздух довольно широко используется в химической технологии в качестве хладагента, особенно в нефтепереработке. Это объясняется низкой стоимостью воздуха по сравнению с другими хладагентами и простотой устройств воздушных холодильников.
2.4.5. Другие области применения воздуха в химической промышленности. Воздух применяют для продувки аппаратов и трубопроводов, для сжигания и распыления жидких и газообразных топлив в форсуночных и горелочных устройствах, для перемешивания текущих сред, для создания «воздушных подушек» в резервуарах и др.
Таблица 2.4
Дата публикования: 2015-10-09; Прочитано: 682 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
