 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Энергия в химической технологии
|
|
2.2.1. Человеческое общество и проблема энергии. Энерговооруженность общества является условием прогресса человечества, и уровень его материального благосостояния определяется количеством энергии, вырабатываемой на душу населения. Потребление энергии на Земле непрерывно возрастает. В 1975 оно составило 0,25Q, в 2000 г. – 0,8Q, а прогноз на 2100 г. составляет колоссальную цифру – 7,3Q, где Q = 2,3 · 1014 кВт · ч.
Выявлена определенная зависимость между потреблением обществом энергии на душу населения и средней продолжительностью жизни. Для достижения устойчивой средней продолжительности жизни, равной 80 лет, потребление энергии на душу населения составляет 7 · 103 кВт · ч. Этот порог достигли или близки к нему такие страны, как Швеция, Япония, Израиль, ФРГ, США. В России же потребление энергии составляет 4 · 103 кВт . ч, что соответствует продолжительности жизни менее 70 лет.
2.2.2. Использование энергии в химической технологии. Химичесое производство – одно из самых энергоемких. Доля энергетических затрат в ней составляет 9 %, в то время как в среднем по промышленности она равна 2,5 %. При доле химической отрасли 6 % во всей промышленности она потребляет до 12 % всей вырабатываемой энергии.
В химической технологии энергия служит для проведения следующих операций:
- химических реакций;
- компрессии газов и жидкостей;
- нагрева материалов;
- проведения тепловых процессов, не связанных с химическими реакциями, (ректификация, испарение и др.);
- проведения механических и гидродинамических процессов (фильтрование, измельчение, сушка и т. д).
В химическом производстве используют электрическую, тепловую, топливную, световую, ядерную и химическую виды энергии.
Электроэнергия необходима для электрохимических, электротермических, электромагнитных и электростатических процессов, а также для переноса различных материалов и приведение в действие машин и механизмов.
Тепловая энергия применяется для высокотемпературной переработки сырья (обжиг, нагрев аппаратуры, реагентов и т. д.). Передачу тепла ведут за счет контакта нагреваемой системы с теплоносителем, в качестве которого наиболее распространены горячий воздух, топочные газы, горячую воду и водяной пар. Тепловая энергия, используемая в химической промышленности, делится на высокопотенциальную (более 350 оС), среднепотенциальную (100–350 оС) и низкопотенциальную (50–100 оС).
Топливная энергия (энергия, полученная при сжигании топлива непо-средственно на технологических установках), применяется для производства тепла и электроэнергии в печах специального назначения.
Световую энергию применяют для проведения процессов фотосинтеза, например, при производстве хлороводорода и галогенопроизводных.
Химическая энергия находит применение в работе химических источников тока.
Ядерная энергия применяется для проведения радиационно-химичес-ких процессов (например, некоторых полимеризационных процессах, а также для анализа, контроля и регулирования технологических процессов.
В химической промышленности на долю электрической энергии приходится примерно 40 %, тепловой – 50 %, топливной – 10 %. Доля остальных видов энергии составляет менее 1 %.
2.2.3. Источники энергии. Классификация источников энергии. Основными источниками энергии для промышленности служат горючие ископаемые и продукты их переработки, энергия воды, пара, биомасса и ядерное топливо. Незначительная доля приходится на энергию ветра, солнца, приливов и геотермальную энергию.
Объем энергии, вырабатываемой в настоящее время на планете составляет примерно 3 · 1014 кВт · ч в год.
Все энергетические ресурсы делятся на первичные и вторичные, возобновляемые и невозбновляемые, топливные и нетопливные. Невозобновляемые энергетические ресурсы связаны с горючими ископаемыми. Среди них каменный уголь, нефть, природный газ, торф, горючие сланцы, битуминозные пески. Остальные виды энергии – это возобновляемые. К ним относятся энергия солнца, ветра, приливов, био- и геотермальная энергии. Все вышеперечисленные виды энергетических ресурсов являются первичными.
Вторичными энергоресурсами называют энергетический потенциал конечных, побочных и промежуточных продуктов и отходов химического производства, используемые для энергоснабжения установок, машин и механизмов. К ним относят теплоту экзотермических реакций, энтальпию отходящих продуктов процесса, а также потенциальную энергию сжатых газов и жидкостей. Предприятия нефтеперерабатывающей, нефтехимической, газовой и химической промышленности, а также металлургии располагают наибольшими ресурсами вторичной энергии, главным образом, в виде тепловой. Схематично классификация источников энергии приведена на рис. 2.1.










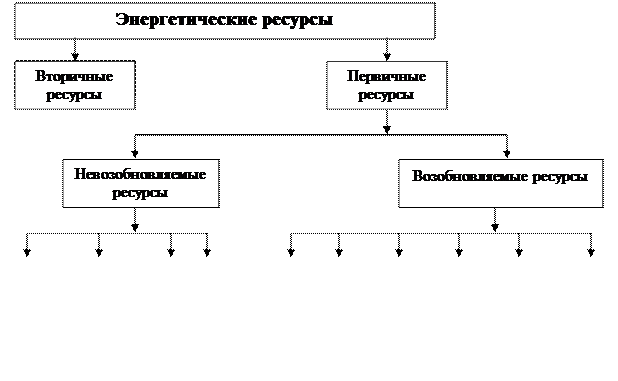
Рис. 2.1. Классификация энергетических ресурсов
2.2.4. Рациональное использование энергии в химической промы-шленности. Большая доля энергии в себестоимости в химическом производстве требует рационального и экономичного подхода к ее использованию. Критерием экономичности при этом является коэффициент использования энергии, равный отношению количества энергии, теоретически необходимой для производства единицы продукции к фактически затраченной энергии:
 = WТ/WП (2.1)
= WТ/WП (2.1)
В случае высокотемпературных эндотермических процессов этот коэф-фициент не превышает 0,7, т.е. свыше 30 % энергии теряется с продуктами реакции или путем теплопередачи через стенку в окружающую среду.
Существует ряд методов снижения тепловых потерь, которые сводятся к двум типам: разработка энергосберегающих технологий и экономичное использование энергии при существующей технологии.
К первому типу относятся следующие мероприятия:
- разработка новых энергоэкономных технологий;
- замена применяемых методов разделения на менее энергоемкие, например, ректификацию на экстракцию и т.д.;
- создание комбинированных энерготехнологических схем, объединя-ющих технологические операции, протекающие с поглощением и выделением энергии.
Ко второму типу энергосберегающих мероприятий относятся:
- уменьшение тепловых потерь за счет эффективной теплоизоляции и уменьшения излучающей поверхности аппаратуры;
- снижение потерь на электросопротивление в электрохимических процессах.
2.2.5. Новые виды энергии в химической технологии. В последние десятилетия в химическую технологию все более интенсивно внедряются новые виды энергии, полученные с применением плазмохимических процессов, ультразвука, фото- и радиационного воздействия, низковольтного электрического разряда, лазерного излучения. Эти экстремальные воздействия способствуют активации молекул реакционной системы, возникновению в ней возбужденных частиц и инициированию химического, в т. ч. с высокой селективностью, процесса. Эта область составляет новый раздел химии – химию высоких энергий (ХВЭ), изучающую состав, свойства и химические превращения в системах, содержащих возбужденные частицы.
Среди этих процессов наиболее перспективными и универсальными являются плазмохимические процессы. Они отличаются протеканием химических процессов в плазменном состоянии.
Различают низкотемпературную (103–104 К) и высокотемпературную (106–108 К) плазму. В химической технологии применяют низкотемпературную плазму. Исследования по применению плазмы в химической промы-шленности проводились более чем в 70 технологических процессах, некоторые из которых внедрены в производство, в т. ч.:
- синтез тугоплавких соединений, таких как карбиды урана и тантала, нитриды титана, алюминия, вольфрама;
- восстановление металлов из оксидов и солей (железо, алюминий, вольфрам, никель, тантал);
- окисление различных веществ (азот, хлороводород, оксид углерода, метан);
- пиролиз углеводородного сырья;
- одностадийный синтез из элементов (аммиака, цианистого водорода, гидразина, фторуглеводородов);
- синтез соединений, образующихся только в условиях плазмы, например, озона, дифторида криптона, оксида серы (II), оксида кремния (II).
В промышленных масштабах плазмохимические процессы применяют для производства ацетилена и водорода из природного газа, ацетилена, этилена и водорода из нефтепродуктов, диоксида титана и т.д.
Плазмохимические процессы отличаются очень малым временем контакта 10–2–10–5 с. При этом под временем контакта понимают истинное время реакции, рассчитываемое по формуле:
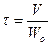 с, (2.2)
с, (2.2)
где V – реакционный объем, м 3
Wo – объем исходной смеси сырья, подаваемый в реактор в единицу времени, м3/с.
Небольшое время контакта определяет незначительные размеры реактора. Плазмохимические процессы легко управляемы, оптимизируются и моделируются и затраты энергии на них не выше, чем в традиционных процессах.
Особое место в ряду перспективных источников энергии занимает водород. Его применение как источника энергии имеет ряд преимуществ:
- широкое распространение в земной коре (горючие ископаемые) и виде практически неисчерпаемых водных ресурсов;
- высокое энергосодержание (в 3,5 раза выше, чем энергосодержание нефти);
- экологическая чистота продуктов сгорания (вода).
В России наиболее экономичный источник водорода – природный газ, из которого водород получают путем парокислородной или паровоздушной конверсии, базирующейся на следующих химических реакциях:

 СН4 + Н2О СО + 3Н2 – 206 кДж/моль (2.3)
СН4 + Н2О СО + 3Н2 – 206 кДж/моль (2.3)

 СН4 + 0,5О2 СО + 2Н2 + 35 кДж/моль (2.4)
СН4 + 0,5О2 СО + 2Н2 + 35 кДж/моль (2.4)
Дата публикования: 2015-10-09; Прочитано: 4028 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
