 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Вода в химической промышленности
|
|
Вода – наиболее распространенное вещество на Земле. При этом основная масса воды сосредоточена в мировом океане, и это соленая вода, которая для промышленности практически непригодна без опреснения. Общая масса пресной воды на Земле составляет чуть больше 2,5 % масс. от мировых запасов (35 млн. км3). При этом почти 99 % пресной воды – это подземные воды и ледники вместе со снежным покровом.
Химическое производство – одно из крупнейших потребителей воды. Этот факт объясняется рядом достоинств воды, из которых можно выделить следующие:
- наличие комплекса ценных физических свойств (высокая теплоемкость, малая вязкость, низкая температура кипения и др.);
- доступность и дешевизна;
- нетоксичность;
- удобство транспортировки и использования в производстве.
В химической промышленности вода используется в следующих направлениях:
1. Для технологических целей в качестве:
- растворителя, среды для проведения некоторых физических и меха-нических процессов;
- промывной жидкости для газов;
- экстрагента и абсорбента;
- для перекристаллизации;
- для флотации;
- в качестве катализатора или инициатора каталитического процесса (взаимодействие щелочных металлов и водорода с хлором, алкилирование на катализаторе Фриделя – Крафтса проводят в присутствии следов воды).
2. В качестве теплоносителя в виде горячей воды и перегретого водяного пара и хладоагента.
3. В качестве сырья или реагента для производства разнообразной химической продукции. Примеры синтеза водорода, ацетилена, минеральных кислот, спиртов приведены ниже.

 СН4 + Н2О СО + 3Н2 (2.5)
СН4 + Н2О СО + 3Н2 (2.5)
СаС2 + 2Н2О = С2Н2 + Са(ОН)2 (2.6)
Р2О5 + 3Н2О = 2Н3РО4 (2.7)

 СН2 = СН2 газ + Н2Огаз С2Н5ОНгаз, (2.8)
СН2 = СН2 газ + Н2Огаз С2Н5ОНгаз, (2.8)
Объемы потребления воды химическим производством зависят от типа производимой продукции и колеблются в широких пределах. Так для производства азотной кислоты требуется 200 т воды /т продукции, вискозного волокна – 1200 т/т, аммиака – 1500 т/т, капронового волокна – 2500 т/ т.
Колоссальный расход технологической воды с учетом большого объема загрязненных сточных вод требует рационального подхода к ее использованию в химической промышленности. Эти задачи решают следующими способами:
- разработкой научно обоснованных норм расхода на технологические нужды;
- максимально полного использования отходов;
- заменой, где возможно, водяного охлаждения на воздушное;
- организацией замкнутых бессточных производств и водооборотных циклов.
Критерием эффективности водооборотного цикла является коэффициент использования воды:
Кв= 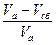 . (2.9)
. (2.9)
где: Vа и Vсб – объемы забираемой из источника свежей воды и сбрасываемой в водоем сточной воды соответственно. В химической промышленности этот коэффициент составляет 0,8–0,9.
2.3.1. Основные показатели качества воды для химической технологии. Вода, используемая в химической промышленности, должна удовлетворять по качеству определенным требованиям. Оно определяется со-вокупностью физических и химических характеристик, среди которых следует отметить следующие: жесткость, окисляемость, рН, доля примесей.
Жесткость – это свойство воды, связанное с присутствием в ней растворенных солей кальция и магния. Жесткость (Ж о) характеризуют концентрацией ионов Са 2+ и Mg 2+ и измеряют в миллимолях на литр воды. По значению Ж о вода бывает мягкой (Ж о< 2), средней жесткости (Ж о = 2–10) и жесткой (Ж о >10).
Окисляемостью называют свойство воды, связанное с присутствием в воде неорганических веществ, легкоокисляющихся соединений железа и сероводорода, способных окисляться различными окислителями и измеряется количеством КМпО 4 или эквивалентным количеством кислорода, затраченным на окисление 1 л воды, т.е. мг/л.
Активная реакция воды характеризует ее кислотность или щелочность (рН). Она определяется присутствием в воде некоторых газов, таких как хлор, оксид углерода (II), гидрокарбонатов, силикатов, реже карбонатов и др., а также растворимых гуминовых кислот и веществ, вносимых в водоем промышленными стоками. Большинство природных вод имеют рН = 6,5–8.
Примеси в природных и сточных водах присутствую во взвешенном, коллоидном или растворенном состоянии. Примеси во взвешенном состоянии – это эмульсии или суспензии. Они кинетически неустойчивы. Примеси в коллоидном состоянии – это гидрофильные и гидрофобные минеральные и органические коллоидные частицы.
2.3.2. Промышленная водоподготовка. Водоподготовкой называют комплекс мероприятий по улучшению качества воды для технологических целей. В нее включают операции по удалению механических примесей, умягчению, осветлению, дегазации.
Осветление – это отстаивание воды с последующей фильтрацией через зернистый материал. Для коагуляции коллоидных примесей и абсорбции окрашенных частиц к ней добавляют электролиты – сульфаты Al или Fe.
Обеззараживание водыпроводят хлором или озоном.
Дегазацию ( удаление из воды растворенных газов) ведут химическим способом, при котором газы поглощаются химическими реагентами, например, в случае диоксида углерода или сероводорода воду обрабатывают моноэтаноламином или раствором гашеной извести. Применяют также физические методы, например, термическую деаэрацию на воздухе либо в вакууме.
Обессоливание применяют в тех производствах, где предъявляются повышенные требования к товарным продуктам на содержание различных металлов, имеющихся в воде. В качестве примера можно назвать производства химически чистых реактивов, полупроводниковых материалов, лекарств и т.д. Обессоливание ведут ионным обменом, дистилляцией, электродиализом. Наглядное представление о методах водоподготовки дает рис. 2.2.

















Рис. 2.2. Методы очистки воды
Дата публикования: 2015-10-09; Прочитано: 2528 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
