 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Дәрістер. Жанама протондану және гидролиз-дену реакцияларының гетерогенді тепе-теңдік жағдайындағы тұнба ерігіштігіне әсері
|
|
Сулы ерітіндіде қиын еритін қосылыстардың аниондары мен катиондары еріткішпен әрекеттесіп протондалуы мүмкін, ол тұнба ерігіштігіне елеулі әсер етеді. Қаныққан ерітіндімен тепе-тең никель сульфидінің тұнбасын алайық:
NiS Û Ni2+ + S2-
тұнба қанық еріт.
Никель иондары сулы ерітінділерде гидролизденеді:
Ni2+ + HOH Û NiOH+ + H+
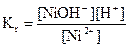 (32)
(32)
Бұдан, никельдің гидролизденген формасының концентрациясы мынаған тең:
 (33)
(33)
Никель иондары ерітіндіде түрлі формада болатындықтан, материалдық баланс теңдеуін құрастырамыз:
СNi = [Ni2+] + [NiOH+] (34)
Бұл теңдеуге никельдің гидролизденген формасы концентрациясының мәнін қоямыз және никель иондарының тепе-теңдік концентрациясын анықтаймыз:
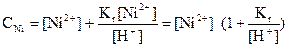 (35)
(35)
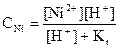
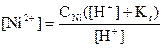 (36)
(36)
Сулы ерітінділерде сульфид-иондар да гидролизге ұшырайды:
S2- + H+ Û HS-
HS- + H+ Û H2S
Онда тұнба үстіндегі қаныққан ерітіндіде түрлі күкіртті формалар болады:
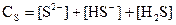 (37)
(37)
Бұдан, сульфид-иондардың тепе-теңдік концентрациясы:
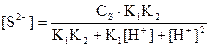 (38)
(38)
Әрине, никельдің түрлі иондарының жалпы концентрациясы күкіртті формалардың және никель сульфидінің ерігіштігінің жалпы концентрациясына тең:
 , (39)
, (39)
Никель сульфидінің иондары қатысының мәндерін ерігіштік көбейтіндісі теңдеуіне қоямыз:
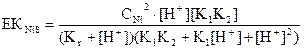 (40)
(40)
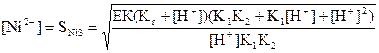 (41)
(41)
Шығарылған теңдеу бойынша бейтарап ортада никель сульфидінің ерігіштігін анықтаймыз:
рН =7, ЕКNiS = 10-24, Kr = 5·10-8,  ,
, 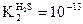
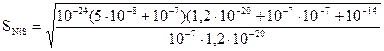 =1,6·10-9 M
=1,6·10-9 M
Гидролиз процесін және оған тұнба иондарының қатысын ескермесек, онда:
SNiS =[Ni2+]=[S2-]= 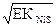 =
= 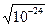 =10-12 M
=10-12 M
Яғни, никель сульфидінің есептелген ерігіштгі 1600 есе көп:
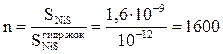
Дата публикования: 2015-10-09; Прочитано: 469 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
