 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Дәрістер. Жанама комплекстүзілу реакциясының реалды ерітінділердегі негізгі аналитикалық реакциялардың жылдамдығына әсері
|
|
Қиын еритін қосылыстар иондары көп сатылы комплекс түзілуге қатыса алады. Лиганд сандары әртүрлі комплекстер түзілуін суда тұнбаның ерігіштігін есептеу кезінде ескеру қажет.
Артық хлорид-иондары болғандағы күміс комплекс түзілу шартында және комплекс түзілу жоқ болған шартында күміс хлоридінің ерігіштігін есептейік.
Гетерогенді тепе-теңдік теңдеуін жазамыз:
AgCl Û Ag+ + Cl-
тұнба қанық. еріт.
Күміс иондарының көпсатылы комплекс түзілуді суреттеп көрсетеміз:
Ag+ + Cl- = AgCl [AgCl] = β1[Ag+][Cl-] β1 = 2,04·103
AgCl + Cl- = [AgCl2]- [AgCl2]- = β1 β2[Ag+][Cl-]2 β2 =1,76·105
[AgCl2]- +Cl- =[AgCl3]2- [AgCl3]2- = β1β2β3[Ag+][Cl-]3 β3 = 4·106
[AgCl3]2- + Cl- =[AgCl4]3- [AgCl4]3- = β1β2β3β4 [Ag+][Cl-]4 β4 = 1,2·106
Онда күміс иондарының тепе-теңдік концентрациясы:
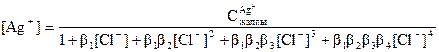 (42)
(42)
Басқа жағынан, күміс иондарының тепе-теңдік концентрациясы тұнба үстіндегі қаныққан ерітіндіде мынаған тең:
 (43)
(43)
ЕКAgCl=1,78·10-10 болғанда және комплекс түзілу болатын хлорид-иондардың концентрациясында ерітіндідегі күміс иондарының құрамы 2,9М тең.
Күміс иондарының тепе-теңдік концентрация теңдеулерін қолданып, былай жазуға болады:
 (44)
(44)
Осыдан, күміс хлоридінің ерігіштігі:
 (45)
(45)

Комплекс түзілудің жанама реакциясы жоқ кездегі күміс хлоридінің ерігіштігін есептейміз:
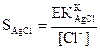

Натрий хлоридінің 0,004 М концентрациясында ерітіндінің иондық күші мынаған тең:


Күміс иондары мен хлор-иондардың белсенділік коэффициентін есептейміз:
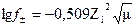
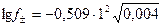 = -0,0362
= -0,0362
f ± = 0,92
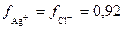
Күміс хлориді ерігіштігінің концентрациялық көбейтіндісінің мәнін анықтаймыз:

Комплекс түзілу жоқ болған жағдайдағы күміс хлоридінің ерігіштігін анықтаймыз:

Суда қиын еритін күміс хлориді катионының комплекс түзудің жанама реакциясы жүргенде тұздың еруі 8 есе көбейеді.
Мынадай жағдайлар мүмкін, қиын еритін электролиттің катионы комплекс түзілуге ұшырайды, ал оның анионы протондалады.
МеХ құрамды тұнба бар деп есептейік:
MeХ Û Ме2+ + Х2-
тұнба қанық еріт.
Тұнба катионы сәйкес құрамды комплекс түзе отырып анионмен әрекеттеседі:
Х2- + 2А2- Û [MeA2]2- + X2-

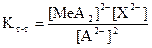 (46)
(46)
Бұл теңдеуді металл ионының концентрациясына көбейтеміз және бөлеміз:
 (47)
(47)
Тұнба үстіндегі қаныққан ерітіндідегі комплекс концентрациясын анықтаймыз:
МеА22- Û МеА + А2- 
МеА Û Ме2+ + А2- 
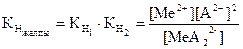
Металл иондарының жалпы концентрациясы үшін материалдық баланс теңдеуін құрамыз:
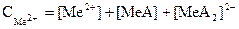 (48)
(48)
Металл иондарының тепе-теңдік концентрациясын және [MeA] комплексінің концентрациясын анықтаймыз:
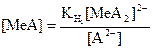 (49)
(49)
 (50)
(50)
Бұдан:
 (51)
(51)
 (52)
(52)
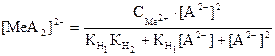 (53)
(53)
Басқа жағынан, тұнба анионы протондалады:
Х2- + Н2О Û НХ + ОН-
НХ + Н2О Û Н2Х + ОН-
Қаныққан ерітіндіде тұнба аниондарының тепе-теңдік концентрациясын анықтаймыз:
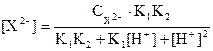 (54)
(54)
(53) және (54) теңдеулерін (46) теңдеуіне қоямыз:



(47) теңдеуін ескереміз:
 (55)
(55)

 болады
болады
Сонда:
 (56)
(56)
Бұл теңдеуді қарапайымдауға болады. Егер А2- күшті қышқылдың анионы болса, гидролизге түспесе және негізгі бір комплекс [MeA2]2- түзілсе, онда  және
және 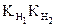 мүшелерін ескермесе болады.
мүшелерін ескермесе болады.
Сонда:
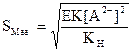 (57)
(57)
Дата публикования: 2015-10-09; Прочитано: 750 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
