 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Вивчення нового матеріалу. Молекули речовини в рідкому стані розташовані майже впритул одна до одної
|
|
Молекули речовини в рідкому стані розташовані майже впритул одна до одної. На відміну від твердих кристалічних тіл, в яких молекули утворюють впорядковані структури в усьому об'ємі кристала і можуть здійснювати теплові коливання біля фіксованих центрів, молекули рідини мають більшу свободу. Кожна молекула рідини, також як і в твердому тілі, "затиснута" з усіх боків сусідніми молекулами і здійснює теплові коливання біля деякого положення рівноваги. Проте, час від часу будь-яка молекула може переміститися в сусіднє вакантне місце. Такі перескоки в рідинах відбуваються досить часто; тому молекули не прив'язані до певних центрів, як в кристалах і можуть переміщатися за усім обсягом рідини. Цим пояснюється плинність рідин. Із-за сильної взаємодії між близько розташованими молекулами вони можуть утворювати локальні (нестійкі) впорядковані групи, декілька молекул, що містять. Це явище називається ближнім порядком (мал. 1).
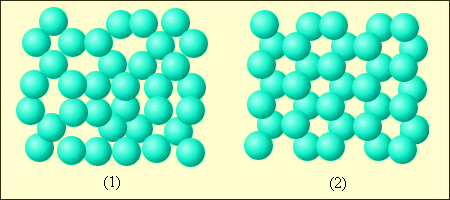
Малюнок 1.
Приклад ближнього порядку молекул рідини і далекого порядку молекул кристалічної речовини: 1 - вода; 2 - лід
Мал..2 ілюструє відмінність газоподібної речовини від рідини на прикладі води. Молекула води H2O складається з одного атома кисню і двох атомів водню, розташованих під кутом 104°. Середня відстань між молекулами пари в десятки разів перевищує середню відстань між молекулами води. На відміну від мал. 1, де молекули води зображені у вигляді кульок, мал. 2 дає уявлення про структуру молекули води.
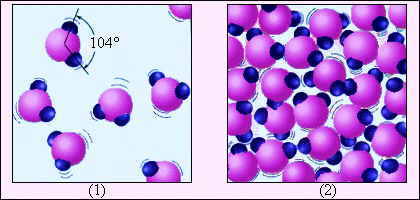
Малюнок 2.
Водяна пара (1) і вода (2). Молекули води збільшені приблизно в 5·107 разів
Внаслідок щільної упаковки молекул стисливість рідин, тобто зміна об'єму при зміні тиску, дуже мала; вона в десятки і сотні тисяч разів менше, ніж в газах. Наприклад, для зміни об'єму води на 1 % треба збільшити тиск приблизно в 200 разів. Таке збільшення тиску в порівнянні з атмосферним досягається на глибині близько 2 км.
Рідини, як і тверді тіла, змінюють свій об'єм при зміні температури. Для не дуже великих інтервалів температур відносна зміна об'єму ΔV / V0 пропорційно зміні температури ΔT:

Коефіцієнт β називають температурним коефіцієнтом об'ємного розширення. Цей коефіцієнт у рідин в десятки разів більше, ніж у твердих тел. У води, наприклад, при температурі 20 °З βв ≈ 2·10-4 К- 1, у сталі βст ≈ 3,6·10-5 К- 1, у кварцевого скла βкв ≈ 9·10-6 К- 1.
Теплове розширення води має цікаву і важливу для життя на Землі аномалію. При температурі нижче 4 °С вода розширюється при пониженні температури (β < 0). Максимум щільності ρв = 103 кг/м3 вода має при температурі 4 °С.
При замерзанні вода розширюється, тому лід залишається плавати на поверхні замерзаючого водоймища. Температура замерзаючої води під льодом дорівнює 0 °С. В щільніших шарах води у дна водоймища температура виявляється близько 4 °С. Завдяки цьому життя може існувати у воді замерзаючих водоймищ.
Найцікавішою особливістю рідин є наявність вільної поверхні. Рідина, на відміну від газів, не заповнює увесь об'єм посудини, в яку вона налита. Між рідиною і газом (чи пором) утворюється межа розділу, яка знаходиться в особливих умовах в порівнянні з іншою масою рідини. Молекули в пограничному шарі рідини, на відміну від молекул в її глибині, оточені іншими молекулами тієї ж рідини не з усіх боків. Сили міжмолекулярної взаємодії, діючі на одну з молекул усередині рідини з боку сусідніх молекул, в середньому взаємно компенсуються. Будь-яка молекула в пограничному шарі притягується молекулами, що знаходяться усередині рідини (силами, діючими на цю молекулу рідини з боку молекул газу (чи пара) можна нехтувати). В результаті з'являється деяка рівнодійна сила, спрямована углиб рідини. Поверхневі молекули силами міжмолекулярного тяжіння втягуються всередину рідини. Але усі молекули, у тому числі і молекули пограничного шару, повинні знаходитися в стані рівноваги. Ця рівновага досягається за рахунок деякого зменшення відстані між молекулами поверхневого шару і їх найближчими сусідами усередині рідини. Як видно з мал. 3.1.2, при зменшенні відстані між молекулами виникають сили відштовхування. Якщо середня відстань між молекулами усередині рідини рівна r0, то молекули поверхневого шару упаковані дещо щільніше, а тому вони мають додатковий запас потенційної енергії в порівнянні з внутрішніми молекулами (см. рис. 3.1.2). Слід мати зважаючи на, що внаслідок украй низької стисливості наявність більш за щільно упакований поверхневий шар не призводить до скільки-небудь помітної зміни об'єму рідини. Якщо молекула переміститься з поверхні всередину рідини, сили міжмолекулярної взаємодії зроблять позитивну роботу. Навпаки, щоб витягнути деяку кількість молекул з глибини рідини на поверхню (тобто збільшити площу поверхні рідини), зовнішні сили повинні зробити позитивну роботу ΔAвнеш, пропорційну зміні ΔS площі поверхні,:
ΔAзовн = σΔS.
Коефіцієнт σ називається коефіцієнтом поверхневого натягу (σ > 0). Таким чином, коефіцієнт поверхневого натягу дорівнює роботі, необхідній для збільшення площі поверхні рідини при постійній температурі на одиницю.
У СІ коефіцієнт поверхневого натягу вимірюється в джоулях на метр квадратний (Дж/м2) або в ньютонах на метр (1 Н/м = 1 Дж/м2).
Отже, молекули поверхневого шару рідини мають надлишкову в порівнянні з молекулами усередині рідини потенційну енергією. Потенційна енергія Eр поверхні рідини пропорційна її площі:
Eр = Aзовн = σS.
З механіки відомо, що рівноважним станам системи відповідає мінімальне значення її потенційної енергії. Звідси витікає, що вільна поверхня рідини прагне скоротити свою площу. З цієї причини вільна крапля рідини набуває кулястої форми. Рідина поводиться так, як ніби по дотичній до її поверхні діють сили, що скорочують (що стягують) цю поверхню. Ці сили називаються силами поверхневого натягу.
Наявність сил поверхневого натягу робить поверхню рідини схожу на пружну розтягнуту плівку, з тією тільки різницею, що пружні сили в плівці залежать від площі її поверхні (тобто від того, як плівка деформована), а сили поверхневого натягу не залежать від площі поверхні рідини.
Деякі рідини, як, наприклад, мильна вода, мають здатність утворювати тонкі плівки. Усім добре відомі мильні бульбашки мають правильну сферичну форму - в цьому теж проявляється дія сил поверхневого натягу. Якщо в мильний розчин опустити дротяну рамку, одна із сторін якої рухлива, то уся вона затягнеться плівкою рідини (мал. 3).
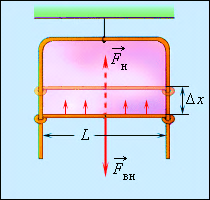
Малюнок 3.
Сили поверхневого натягу прагнуть скоротити поверхню плівки. Для рівноваги рухливої сторони рамки до неї треба прикласти зовнішню силу Якщо під дією сили перекладина переміститься на Δx, то буде виконана робота ΔAзовн = FвнΔx = ΔEp = σΔS, де ΔS = 2LΔx - приріст площі поверхні обох сторін мильної плівки. Оскільки модулі сил однакові, можна записати:
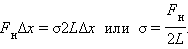
Таким чином, коефіцієнт поверхневого натягу σ може бути визначений як модуль сили поверхневого натягу, діючій на одиницю довжини лінії, що обмежує поверхню.
Через дію сил поверхневого натягу в краплях рідини і усередині мильних бульбашок виникає надлишковий тиск Δp. Якщо подумки розрізати сферичну краплю радіусу R на дві половинки, то кожна з них повинна знаходитися в рівновазі під дією сил поверхневого натягу, прикладених до межі розрізу завдовжки 2πR і сил надлишкового тиску, діючих на площу πR2 перерізи (мал. 4). Умова рівноваги записується у виді
σ2πR = ΔpπR2.
Звідси надлишковий тиск усередині краплі рівний

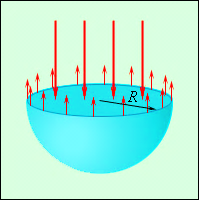
Малюнок 4.
Надлишковий тиск у середині мильної бульбашки в два рази більше, оскільки плівка має дві поверхні:
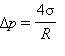
Поблизу межі між рідиною, твердим тілом і газом форма вільної поверхні рідини залежить від сил взаємодії молекул рідини з молекулами твердого тіла (взаємодією з молекулами газу (чи пари) можна нехтувати). Якщо ці сили більше сил взаємодії між молекулами самої рідини, то рідина змочує поверхню твердого тіла. В цьому випадку рідина підходить до поверхні твердого тіла під деяким гострим кутом θ, характерним для цієї пари рідина - тверде тіло. Кут θ називається крайовим кутом. Якщо сили взаємодії між молекулами рідини перевершують сили їх взаємодії з молекулами твердого тіла, то крайовий кут θ виявляється тупим (мал. 5). В цьому випадку говорять, що рідина не змочує поверхню твердого тіла. При повному змочуванні θ = 0, при повному незмочуванні θ = 180°.
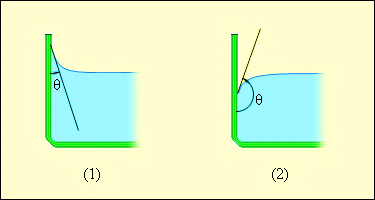
Малюнок 5.
Крайовікутищозмочує (1) інезмочувальної (2) рідин
Капілярними явищами називають підйом або опускання рідини в трубках малого діаметру - капілярах. Змочуючі рідини піднімаються по капілярах, незмочувальні - опускаються.
На мал. 6 зображена капілярна трубка деякого радіусу r, опущена нижнім кінцем в змочуючу рідину щільності ρ. Верхній кінець капіляра відкритий. Під'їм рідини в капілярі триває до тих пір, поки сила тяжіння діюча на стовп рідини в капілярі, не стане рівною по модулю результуючій Fн силі поверхневого натягу, діючій уздовж межі зіткнення рідини з поверхнею капіляра,: Fт = Fн, де Fт = mg = ρhπr2g, Fн = σ2πr cos θ.
Звідси слідує:
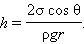
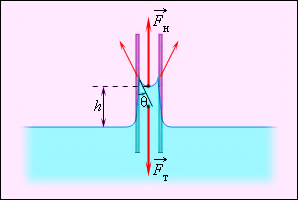
Малюнок 6.
При повному змочуванні θ = 0, cos θ = 1. В цьому випадку

При повному незмочуванні θ = 180°, cos θ = - 1 і, отже, h < 0. Рівень незмочувальної рідини в капілярі опускається нижче за рівень рідини в посудині, в яку опущений капіляр.
Вода практично повністю змочує чисту поверхню скла. Навпаки, ртуть повністю не змочує скляну поверхню. Тому рівень ртуті в скляному капілярі опускається нижче за рівень в посудині.
Запитання для самоперевірки:
1 Які властивості має поверхневий шар рідини?
2 Що називають поверхневим натягом?
3 Виконавши рисунок, установіть фізичний зміст поверхневого натягу як величини, пов’язаної з енергією поверхневого шару рідини.
4 Наведіть приклади дії сил поверхневого натягу.
5 Що називають коефіцієнтом поверхневого натягу? Від чого він залежить? У яких одиницях вимірюється коефіцієнт поверхневого натягу в СІ?
6 Що таке сила поверхневого натягу? Яка формула виражає зміст цього поняття?
7 Як зміниться сила поверхневого натягу води у разі розчинення в ній мила?
8 Якої форми набувають краплі рідини в умовах невагомості? Чому?
9 Виконавши пояснювальний рисунок, розкрийте фізичну сутність явищ змочування і незмочування.
10 Чому плями із жиру на одязі не вдається змити водою?
11 Що називають капілярністю?
12 Обґрунтуйте, в якому випадку рідина у капілярі піднімається, а в якому – опускається.
13 Чому фундамент цегляних будинків покривають гарячим бітумом чи обкладають толем?
14 Виведіть формулу, за якою визначають висоту піднімання чи опускання рідини у капілярі.
15 Наведіть приклади врахування і використання капілярних систем у повсякденному житті.
Тема 5.5. Будова і властивості твердих тіл. (2 год.)
Мета: розкрити основні положення та зосередити увагу студентів на ключових поняттях теми; розвивати уміння аналізувати навчальний матеріал, пам’ять та логічне мислення; навчити глибше розбиратися у фізичних закономірностях й вміти використовувати їх у практичній діяльності; виховувати позитивнее ставлення та зацікавленість до вивчення предмету.
План.
1.Кристали та їх види.
2.Типи кристалів.
3.Аморфні тіла.
4.Застосування кристалів.
Дата публикования: 2015-09-17; Прочитано: 2026 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
