 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Определение железа(III) в растворе
|
|
Цель работы. Методом комплексонометрического титрования определить концентрацию железа(III) в растворе
Вводная часть. Метод основан на том, что устойчивость комплексов ЭДТА с окисленной и восстановленной формами сильно различается. Так, можно оттитровать раствор, содержащий ионы железа(III), проследив за изменением потенциала платинового электрода, погруженного в испытуемый раствор. Протекающие при этом электрохимические реакции:
до ТЭ 
после ТЭ 
обусловливают достаточно резкое изменение потенциала после достижения ТЭ:
до ТЭ:  ;
;
после ТЭ: 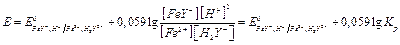 .
.
Титрование можно проводить в достаточно широком интервале рН, в присутствии потенциометрического индикатора – ионов Fe(II). В кислых растворах (рН £ 3) образование комплекса Fe3+ замедляется, что отражается на скорости установления равновесного потенциала.
Дата публикования: 2015-09-17; Прочитано: 256 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
