 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Экспериментальная часть. В колбу внесите 10 мл раствора фосфорной кислоты и оттитруйте раствор 0,2 M щелочью с индикатором метиловым оранжевым
|
|
В колбу внесите 10 мл раствора фосфорной кислоты и оттитруйте раствор 0,2 M щелочью с индикатором метиловым оранжевым.
В чистый стакан внесите 10 мл фосфорной кислоты, погрузите в него стеклянный электрод и проточный мостик от хлоридсеребряного электрода сравнения и оттитруйте раствором щелочи, прибавляя по 0,5 мл. После добавления очередной порции титранта раствор необходимо перемешивать и измерять значение pH. Титрование продолжают до достижения pH 12. Полученные данные вносите в таблицу, и постройте кривую потенциометрического титрования в координатах pH – V. Объемы титранта для 1 и 2 ТЭ находят по табличным данным, рассчитывая VТЭ1 и VТЭ2 в области скачков титрования. Найдя VТЭ1 и VТЭ2 по (7) и (8) рассчитывают pK1 и pK2. Данные вносят в таблицы.
Определение pK1 (найдено: VТЭ1=)
| № | 0< V<VТЭ1 | pH | 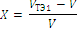
| lg x | pK 1 = pH + lg x |
Определение pK2 (найдено: VТЭ1=; VТЭ2=).
| № | Vтэ1< V<Vтэ2 | pH | 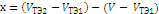
| lg x | pK 2 = pH + lg x |
Определение pK 3 (pHтэ2 =).
| N | pK 2 | 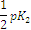
| 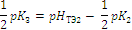
| pK 3 |
Проведите статистическую обработку полученных значений pK1, pK2 и pK3 (среднее, стандартное отклонения, доверительный интервал).
Дата публикования: 2015-09-17; Прочитано: 392 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
