 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Определение свинца(II) в растворе
|
|
Цель работы. Методом потенциометрического титрования определить концентрацию свинца (II) в растворе
Вводная часть. При потенциометрическом титровании ионов свинца невозможно применение электрода первого рода (металлического свинца) из-за его большой электролитической упругости растворения. Поэтому обычно в качестве индикаторного используют электрод второго рода.
Смесь ионов гексацианоферрата(II) и гексацианоферрата (III), представляющая собой обратимую окислительно-восстановительную систему, является потенциалопределяющей в случае использования инертного электрода (обычно платинового). Потенциал такого электрода выражается уравнением Нернста:
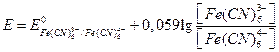 . (1)
. (1)
Электрохимическая реакция, протекающая с участием этой редокс-системы в присутствии ионов Pb2+ (или любого другого катиона, образующего с Fe(CN)64- малорастворимый электролит) выражается уравнением:
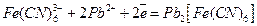 ,
,
 (2)
(2)
Учитывая, что
 (3)
(3)
и подставляя это в выражение (2), получаем
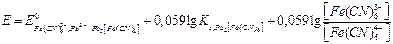 (4)
(4)
Очевидно, что потенциал индикаторного электрода отвечает величине Е, выражаемой уравнением (4), до ТЭ и уравнением (1) — после достижения ТЭ.
Ионы свинца образуют малорастворимые соединения Pb3[Fe(CN)6]2 и Pb2[Fe(CN)6]. Поэтому, если до титрования в испытуемый раствор прибавить немного раствора соли К3[Fe(CN)6], то возможно образование Pb3[Fe(CN)6]2.
При прибавлении раствора титранта К4[Fe(CN)6] ионы свинца переходят в менее растворимое соединение — гексацианоферрат(II) свинца. Поэтому в начале титрования потенциал электрода несколько возрастает за счет увеличения концентрации Fe(CN)63-, а затем уменьшается. Вблизи ТЭ наблюдается достаточно резкий скачок потенциала, обусловленный изменением Е в уравнениях (1) и (4) на величину  .
.
Дата публикования: 2015-09-17; Прочитано: 505 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
