 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Прямые методы кондуктометрии в физико-химических исследованиях
|
|
1.3.1.1. Определение констант ионизации слабых электролитов
Для реакции вида: HA ↔ H+ + A– выражение для константы ионизации имеет вид:
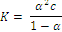
| (1.14) |
Для разбавленных растворов слабых электролитов справедливо уравнение Аррениуса:
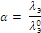
| (1.15) |
Подставляя выражение (1.14) в (1.15) получаем:

| (1.16) |
1.3.1.2. Определение растворимости малорастворимого соединения

 Пусть диссоциация малорастворимого соединения идет по уравнению: MA ↔ M+ + A–. Растворимость этой соли равна S, а насыщенный раствор соли имеет электропроводность χ. Тогда, исходя из уравнения (1.4), можно записать:
Пусть диссоциация малорастворимого соединения идет по уравнению: MA ↔ M+ + A–. Растворимость этой соли равна S, а насыщенный раствор соли имеет электропроводность χ. Тогда, исходя из уравнения (1.4), можно записать:
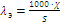 1.17
1.17
Для случая диссоциации малорастворимых солей величина l может быть рассчитана на основании закона Кольрауша, либо взята из справочников для ионных электропроводностей растворов при бесконечном разбавлении.
Дата публикования: 2015-09-17; Прочитано: 505 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
