 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Свинцевий акумулятор
|
|
Пластини свинцевого акумулятора відливають зі свинцю. Кількість енергії, яку можна накопичити в акумуляторі, пропорційна площі поверхні його пластин, що контактують з електролітом. Для збільшення цієї поверхні акумулятор має по декілька додатніх і від’ємних пластин, які зібрані в два напівблока. Пластини виготовляють у вигляді грат з комірками заповненими пористою активною масою (додатні пластини ‑ 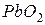 двоокис свинцю; від’ємні пластини ‑ пористий свинець).
двоокис свинцю; від’ємні пластини ‑ пористий свинець).
При зборці акумулятора після кожної від’ємної пластини вставляється додатня. По краях з двох сторін стоять від’ємні пластини, оскільки додатні пластини схильні до викривлення. Тому у свинцевому акумуляторі від’ємних пластин завжди на одну більше, ніж додатніх.
Електролітом у свинцевих акумуляторах служить розчин чистої сірчаної кислоти (її хімічна формула H2SO4) в дистильованій воді. Сірчана кислота має щільність 1,83 г/см3, вода – 1 г/см3. Тому щільність електроліту перевищує 1 г/см3, зазвичай вона знаходиться в межах 1,2…1,4 г/см3.
В процесі першого спеціального заряду нового акумулятора, який називають формуванням акумулятора, в результаті електричних процесів активна маса додатніх пластин перетворюється на перекис свинцю РbО2. Активна маса від’ємних пластин переходить в чистий пористий (губчастий) свинець Рb. Крім того, при цих процесах виділяється сірчана кислота H2SO4, тому щільність електроліту підвищується.
Коли необхідно використовувати енергію, накопичену в акумуляторі, його включають у відповідне електричне коло. Акумулятор віддає енергію, що виробляється за рахунок хімічних процесів, в результаті яких активна маса додатніх і від’ємних пластин перетворюється на сірчанокислий свинець PbSO4, званий також сульфатом свинцю. При цих реакціях виділяється вода, що розбавляє електроліт, тому його щільність падає.
Електрохімічні реакції, що протікають при заряді і розряді акумулятора, описуються наступним узагальненим рівнянням:
розрядка
PbO2 + 2H2SO4 +Pb «2PbSO4 + 2H2O
зарядка
Після ввімкнення на зарядку напруга на виводах акумулятора швидко підвищується з 1,7…1,8 до 2,1…2,2 В і потім дуже повільно до 2,3 В. У кінці заряду відбувається підвищення напруги до 2,6…2,8 В і починається "кипіння" акумулятора, тобто бурхливе виділення газів (водню і кисню) внаслідок розкладання води електричним струмом. Різке підвищення напруги і "кипіння" акумулятора свідчать про закінчення заряду. Після відключення акумулятора від джерела електричної енергії його напруга майже відразу падає приблизно до 2,1 В.
Дата публикования: 2015-09-17; Прочитано: 277 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
