 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Приклади виконання завдань. Приклад 1. Користуючись даними таблиці 6 визначити види хімічних зв’язків у молекулах
|
|
Приклад 1. Користуючись даними таблиці 6 визначити види хімічних зв’язків у молекулах  .
.
Відповідь. До складу молекули 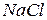 входять атоми елементів, відносні електронегативності яких різко відрізняються: для натрію 0,9 а для хлору 3,0. Завдяки цьому атом натрію віддає електрон зовнішнього енергетичного рівня атому хлору, перетворюючись в позитивно заряджений іон, а атом хлору відповідно в негативно заряджений іон. Між ними виникає електростатична взаємодія, тобто в молекулі
входять атоми елементів, відносні електронегативності яких різко відрізняються: для натрію 0,9 а для хлору 3,0. Завдяки цьому атом натрію віддає електрон зовнішнього енергетичного рівня атому хлору, перетворюючись в позитивно заряджений іон, а атом хлору відповідно в негативно заряджений іон. Між ними виникає електростатична взаємодія, тобто в молекулі 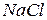 реалізується іонний зв’язок.
реалізується іонний зв’язок.
Схематично цей процес можна представити так:
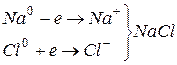
У молекулі 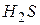 реалізується ковалентний полярний зв’язок, оскільки атоми водню і сірки в незначній мірі відрізняються за величинами відносних електронегативностей (ВЕН) (ВЕН Н=2,1; ВЕН S=2,5). Спільні електронні пари зміщенні до атома сірки. У молекулі
реалізується ковалентний полярний зв’язок, оскільки атоми водню і сірки в незначній мірі відрізняються за величинами відносних електронегативностей (ВЕН) (ВЕН Н=2,1; ВЕН S=2,5). Спільні електронні пари зміщенні до атома сірки. У молекулі 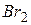 утворюється ковалентний неполярний зв’язок, оскільки молекула складається з атомів одного елемента. Схематично це можна зобразити так:
утворюється ковалентний неполярний зв’язок, оскільки молекула складається з атомів одного елемента. Схематично це можна зобразити так:
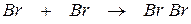
Приклад 2. У молекулах якої з наведених сполук:  - ковалентний зв’язок характеризується найбільшою полярністю?
- ковалентний зв’язок характеризується найбільшою полярністю?
Розв’язання. Полярність зв’язку між атомами залежить від величин відносних електронегативностей взаємодіючих атомів. Користуючись даними таблиці 6, знаходимо різниці ВЕН: для H-S 2,5-2,1=0,4
для H-O 3-2,1=1,4
для HCl 3-2,1=0,9
Найбільшою полярністю характеризується зв’язок Н-О в молекулі 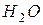 .
.
Дата публикования: 2015-09-18; Прочитано: 231 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
