 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Контрольні завдання. 461. Написати електронні формули атомів елементів з порядковими номерами 9 і 28
|
|
461. Написати електронні формули атомів елементів з порядковими номерами 9 і 28.
462. Написати електронні формули атомів фосфору та ванадію.
463. Яке максимальне число електронів може бути на 1, 2, 3, 4 – му рівнях енергії в атомі? Скільки електронів максимально може знаходитися на 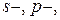
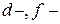 підрівнях? Чому? Сформулювати принцип Паулі.
підрівнях? Чому? Сформулювати принцип Паулі.
464. Скільки  і
і 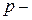 електронів у атомах елементів № 17, 22?
електронів у атомах елементів № 17, 22?
465. Скільки 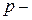 і
і 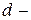 електронів у атомах елементів № 28, 42? Чому на одній орбіталі може знаходитися не більше двох електронів?
електронів у атомах елементів № 28, 42? Чому на одній орбіталі може знаходитися не більше двох електронів?
466. Скільки вільних р - орбіталей у атомах елементів № 6, 13, 15?
467. Які орбіталі атома заповнюються електронами раніше: 4 s чи 3 d; 5 s чи 4 p? Чому? Скласти електронну формулу атома елемента з порядковим номером 23.
468. Скільки і які значення приймає магнітне квантове число у таких випадках:
а) l = l, l =3? Відповідь обґрунтувати.
469. Атомам яких елементів і яким станам (нормальному або збудженому) відповідають електронні формули:
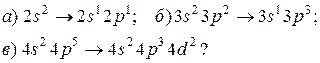
470. Скласти електронні формули: а) атома стронцію; б) іона хрома 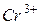 ; в) іона хлору
; в) іона хлору 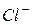 :
:
471. Скласти електронні формули: а) атома заліза; б) іона сірки  ; в) іона міді
; в) іона міді 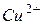 .
.
472. Яке квантове число характеризує форму атомних орбіталей? Вказати максимальне число електронів на орбіталях: а) р; б) d; в) f.
473. Розташувати атомні орбіталі: 4 s, 3 d, 4 d, 5 s, 4 р у порядку зростання їхньої енергії. Відповідь обґрунтувати.
474. Які значення може мати головне квантове число n? В якому випадку електрон має найбільшу і найменшу енергію?
475. Які властивості електрона характеризує спінове квантове число? Чому дорівнює сумарний спін для п’яти електронів на d - орбіталях?
476. Атом має набір повністю заповнених орбіталей: 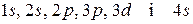 . Навести розподіл електронів за квантовими комірками і вказати, з атомів якого елемента складається проста речовина?
. Навести розподіл електронів за квантовими комірками і вказати, з атомів якого елемента складається проста речовина?
477. Скласти електронні формули і показати, що іони  і
і 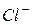 мають однакову кількість електронів.
мають однакову кількість електронів.
478. Які елементи називають  елементами? Яка різниця між хімічними та фізичними властивостями цих елементів?
елементами? Яка різниця між хімічними та фізичними властивостями цих елементів?
479. Виходячи з електронної будови атомів кисню і сірки пояснити, чому сірка може бути шестивалентною, а кисень не більш ніж двохвалентний.
480. Написати електронну формулу атома елемента, в якого електрони зовнішнього енергетичного рівня мають квантові числа:  ±½.
±½.
ПЕРІОДИЧНА СИСТЕМА ЕЛЕМЕНТІВ Д.І.МЕНДЕЛЄЄВА
Дата публикования: 2015-09-18; Прочитано: 544 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
