 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
У результаті гідролізу в розчині виникає надлишок іонів , які зумовлюють лужне середовище ( )
|
|
б) Карбонат натрію – сіль, утворена слабкою багатоосновною кислотою 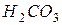 та сильною однокислотною основою
та сильною однокислотною основою 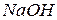 . У даному випадку аніони солі
. У даному випадку аніони солі 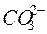 , зв’язуючи іони
, зв’язуючи іони  води, утворюють аніони кислої солі
води, утворюють аніони кислої солі  , тому що іони
, тому що іони  дисоціюють важче, ніж молекули
дисоціюють важче, ніж молекули  . За звичайних умов гідроліз відбувається за першим ступенем. Сіль гідролізує за аніоном. Скорочене іонне рівняння гідролізу:
. За звичайних умов гідроліз відбувається за першим ступенем. Сіль гідролізує за аніоном. Скорочене іонне рівняння гідролізу:
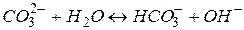 .
.
Додаючи до лівої та правої частин рівняння іони натрію, одержуємо повне іонне рівняння реакції:
 .
.
Рівняння реакції гідролізу 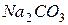 в молекулярній формі:
в молекулярній формі:
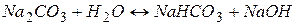
У розчині нагромаджується надлишок гідроксид-іонів, тому розчин солі має лужну реакцію (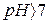 ).
).
в) Сульфат цинку – сіль, утворена слабкою багатокислотною основою 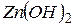 та сильною багатоосновною кислотою
та сильною багатоосновною кислотою 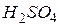 . У даному випадку катіони
. У даному випадку катіони 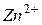 зв’язують гідроксид-іони води, утворюючи катіони основної солі
зв’язують гідроксид-іони води, утворюючи катіони основної солі 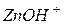 . Молекули
. Молекули 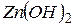 не утворюються, бо іони
не утворюються, бо іони 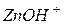 дисоціюють важче, ніж молекули
дисоціюють важче, ніж молекули  . За звичайних умов гідроліз відбувається за першим ступенем. Сіль гідролізує за катіоном. Скорочене іонне рівняння гідролізу:
. За звичайних умов гідроліз відбувається за першим ступенем. Сіль гідролізує за катіоном. Скорочене іонне рівняння гідролізу:

Додаючи до лівої та правої частин рівняння іони 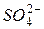 , одержуємо повне іонне рівняння:
, одержуємо повне іонне рівняння:
 ,
,
а в молекулярній формі:
 .
.
У результаті гідролізу в розчині виникає надлишок іонів водню, тому розчин 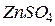 має кислу реакцію (
має кислу реакцію (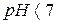 ).
).
Приклад 10. Які продукти утворюються в результаті змішування розчинів 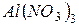 і
і 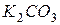 ? Скласти іонні та молекулярні рівняння реакцій.
? Скласти іонні та молекулярні рівняння реакцій.
Відповідь. Сіль 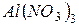 гідролізує за катіоном, а
гідролізує за катіоном, а 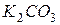 - за аніоном:
- за аніоном:
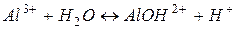 ;
;
 .
.
Якщо розчини даних солей знаходяться в одній посудині, то відбувається взаємне посилення гідролізу кожної з солей, тому що іони  і
і 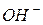 утворюють молекулу слабкого електроліту
утворюють молекулу слабкого електроліту  . Тоді рівновага гідролізу зміщується праворуч, і гідроліз кожної солі йде до кінця з утворенням
. Тоді рівновага гідролізу зміщується праворуч, і гідроліз кожної солі йде до кінця з утворенням 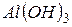 та
та 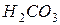 . Іонне рівняння гідролізу:
. Іонне рівняння гідролізу:
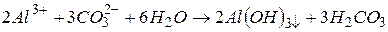
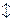
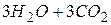
молекулярне рівняння:
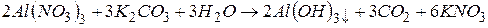 .
.
Дата публикования: 2015-09-18; Прочитано: 530 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
