 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Определение зависимости коагулирующей способности электролитов
|
|
Задачи работы: определение коагулирующей способности электролитов от заряда коагулирующего иона и выполнение правила Шульце-Гарди.
Оборудование и реактивы: золь гидроксида железа (III), 1 М раствор хлорида натрия, 0,1 М карбоната натрия, 0,002 М цитрата натрия, дистиллированная вода, 18 пробирок, штатив, пипетки.
Выполнение работы: подготовить ряд из шести пробирок. В 5 пробирок ряда, со 2-ой по 6-ю пипеткой прилить по 2 мл воды. Далее в первую и вторую пробирки ряда прилить по 2 мл раствора хлорида натрия. Раствор во второй пробирке перемешать и 2 мл его перенести в третью пробирку. Раствор в третьей пробирке перемешать и 2 мл его перенести в четвертую пробирку. Так развести во всех пробирках. Из последней (шестой) пробирки отобрать 2 мл раствора и вылить. Таким образом, в пробирках оказывается по 2 мл раствора электролита, разведенного по сравнению с исходным в следующее число раз: 1-я – 1, 2-я – 2, 3-я – 4, 4-я – 8, 5-я- 16 и 6-я – 32. Затем в каждую пробирку добавить 2 мл золя гидроксида железа (III) и растворы в пробирках перемешать. Определить последнюю, начиная с первой, пробирку, в которой еще наблюдается коагуляция золя. Записать в таблицу результаты опытов, отмечая знаком «+» наличие и знаком «−» отсутствие коагуляции. Опыт повторить аналогично для растворов карбоната и цитрата натрия. Зная исходную молярную концентрацию раствора электролита и разведение его в пробирке, где еще происходит коагуляция (n), рассчитать порог коагуляции каждого электролита по формуле:
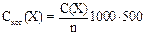 ммоль/л, где 1000 – число миллимолей в 1 моль, 500 – фактор пересчета с 2 мл на 1000 мл золя. Число значности электролитов определить относительно хлорида натрия:
ммоль/л, где 1000 – число миллимолей в 1 моль, 500 – фактор пересчета с 2 мл на 1000 мл золя. Число значности электролитов определить относительно хлорида натрия: 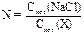 .
.
Результаты записать в таблицу:
| Электролит | Концентрация электролита, моль/л | Коагули-рующий ион | № пробирок 1 2 3 4 5 6 разведения 1 2 4 8 16 32 | Порог коагуляцииммоль/л | Число значности |
| NaCl | Cl− | ||||
| Na2CO3 | 0,1 | CO32− | |||
| Na3C6H5O7 | 0,002 | C6H5O73− |
Порядок оформления работы: дать определение коагуляции, записать ход работы и результаты, определить пороги коагуляции сравниваемых электролитов, сделать вывод о выполняемости правила Шульце-Гарди, влиянии коагулирующих ионов на порог коагуляции.
Дата публикования: 2015-09-18; Прочитано: 1041 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
