 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Осн. кисл. осн. осн
|
|
Li2O + Сl2О7 → 2LiСlО4 СrО + СаО 
осн. кисл. осн. кисл.
Cs2O + SnO2→ Cs2SnO3 FeO + SO3 → FeSO4,
осн. не солетв. кисл. кисл.
MgO + NО 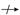 V2O5 + CO2
V2O5 + CO2 
Амфотерними називають оксиди, яких здатні проявляти як основні, так і кислотні властивості.
До амфотерних належать:
1) оксиди деяких елементів головних підгруп –  ,
, 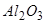 ,
,  ,
, 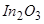 ,
, 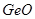 ,
, 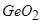 ,
, 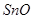 ,
, 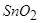 ,
, 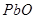 ,
, 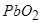 ,
,  ,
, 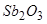 та деякі інші;
та деякі інші;
2) оксиди деяких металів побічних підгруп, частіше такі, в яких метали проявляють проміжні ступені окиснення, наприклад: 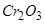 ,
, 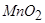 ,
, 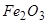 ,
, 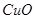 ,
,  .
.
Амфотерні оксиди реагують з речовинами основного характеру, проявляючи кислотні властивості, з речовинами кислотного характеру, проявляючи основні властивості, та між собою з утворенням солей.
 ;
;
ZnO + Na2O = Na2ZnO2;
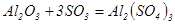 ;
;
Al2O3 + 6NaOH =2Na3AlO3 + 3H2O;
Al2O3 + ZnO = Zn(AlO2)2.
Властивості оксидів металів побічних груп, здатних проявляти різні ступені окиснення, змінюються від основних через амфотерні до кислотних з підвищенням ступеня окиснення елементів, що утворюють оксид.
Наприклад:
| основні | амфотерні | кислотні |
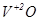
| 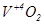
| 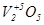
|
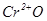
| 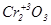
| 
|
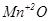
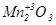
| 
| 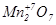
|
Необхідно чітко уявляти собі, що амфотерні оксиди не в однаковій мірі здатні проявляти основні та кислотні властивості. Деякі з них за властивостями ближче до основних оксидів, наприклад 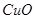 ,
, 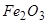 , деякі – до кислотних, наприклад
, деякі – до кислотних, наприклад 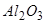 . У переважній більшості амфотерних оксидів елементи проявляють ступені окиснення +2, +3, рідше вищий.
. У переважній більшості амфотерних оксидів елементи проявляють ступені окиснення +2, +3, рідше вищий.
Дата публикования: 2015-09-18; Прочитано: 293 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
