 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Химические свойства толуола
|
|
1.Нитрование толуола приводит к образованию тринитропроизводного:
 (тринитротолуол).
(тринитротолуол).
2.Галогенирование (в кольцо в присутствии катализатора бромида алюминия)

В боковую цепь
в отсутствии катализаторов на свету или при нагревании (т.е. в тех же условиях, что и у алканов) галоген можно ввести в боковую цепь
 + Cl2 –hn®
+ Cl2 –hn®  (хлористый бензил) + HCl
(хлористый бензил) + HCl
3) Окисление
Гомологи бензола горят с образованием углекислого газа и воды, а также окисляются растворами перманганата калия по боковой цепи с образованием бензойной кислоты или ее солей:
С6Н5СН3 + 9О2 ® 7СО2 + 4Н2О (горение);
5С6Н5CH3 + 6KMnO4 + 9H2SO4 ® 5C6H5COOH + 6MnSO4 + 3K2SO4 + 14H2O;
С6Н5CH3 + 2KMnO4  C6H5COOK + 2MnO2¯ + KOH + H2O;
C6H5COOK + 2MnO2¯ + KOH + H2O;
Понятие о механизме электрофильного замещения, влияние электронодонорных и электроноакцепторных заместителей (ориентантов) на скорость и направление реакций. Правила ориентации в ароматическом кольце.
Механизм реакции ароматического электрофильного замещения На первом этапе происходит присоединение электрофила, на втором — отщепление электрофуга:

В ходе реакции образуется промежуточный положительно заряженный интермедиат (на рисунке — 2b). Он носит название интермедиат σ-комплекс. Этот комплекс, как правило, очень реакционноспособен и легко стабилизируется, быстро отщепляя катион. Лимитирующей стадией в подавляющем большинстве реакций является первый этап.
В молекуле бензола p -электронное облако распределено равномерно по всем атомам углерода за счет сопряжения. Если же в бензольное кольцо ввести какой-нибудь заместитель, это равномерное распределение нарушается и происходит перераспределение электронной плотности в кольце. Место вступления второго заместителя в бензольное кольцо определяется природой уже имеющегося заместителя.
Заместители подразделяют на две группы в зависимости от проявляемого ими эффекта: электронодонорные и электроноакцепторные.
Электронодонорные заместители (заместители первого рода): повышают электронную плотность в кольце. К ним относятся гидроксильная группа —ОН; аминогруппа —NН2; радикалы алканов –СН3 и др.; галогены –Cl, –Br. -I. Неподеленная пара электронов в этих группах вступает в общее сопряжение с p -электронной системой бензольного кольца и увеличивает длину сопряженной системы. В результате электронная плотность сосредоточивается в орто- и пара-положениях:
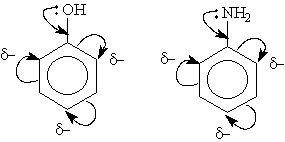
Вновь введеные заместиели направляются в орто- или пара- положения.
Электроноакцепторные заместители снижают электронную плотность в кольцее (заместители второго рода):. К ним относятся нитрогрупла —NO2, сульфогруппа —SO3Н, альдегидная —СНО и карбоксильная —СООН группы. Эти заместители образуют с бензольным кольцом общую сопряженную систему, но общее электронное облако смещается в сторону этих групп. Таким образом, общая электронная плотность в кольце уменьшается, причем меньше всего она уменьшается в мета-положениях:
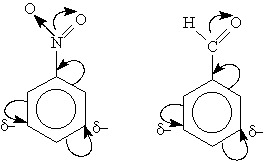
Вновь введеные заместиели направляются в мета-положение.
Закономерности преимущественного направления замещения в бензольном кольце называют правилами ориентации.
Так, толуол, содержащий заместитель первого рода, нитруется и бромируется в пара- и орто -положения:

Нитробензол, содержащий заместитель второго рода, нитруется и бромируется в мета- положение:

Помимо ориентирующего действия заместители оказывают влияние и на реакционную способность бензольного кольца: ориентанты 1-го рода (кроме галогенов) облегчают вступление второго заместителя; ориентанты 2-го рода (и галогены) затрудняют его.
Галогеналканы. Классификация. Изомерия, номенклатура. Методы получения монохлорпроизводных алканов. Реакции замещения на водород, гидрокси- и аминогруппу. Отщепление галогенводородов (правило Зайцева), реакция с натрием (Вюрца).
Дата публикования: 2014-11-18; Прочитано: 3189 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
