 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Дисоціація води. Водневий показник
|
|
Вода дуже незначною мірою дисоціює на іони.

Дисоціація води – ендотермічний процес (поглинання теплоти).
Константа рівноваги

За температури 298 К  , що свідчить про те, що вода є дуже слабким електролітом, і концентрація молекул, які зазнали розщеплення на іони, дуже незначна порівняно з концентрацією недисоційованих молекул.
, що свідчить про те, що вода є дуже слабким електролітом, і концентрація молекул, які зазнали розщеплення на іони, дуже незначна порівняно з концентрацією недисоційованих молекул.
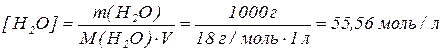

Іонний добуток води 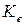 є сталою величиною за даної температури. За стандартних умов (
є сталою величиною за даної температури. За стандартних умов ( )
)  .
.

Для характеристики кислотності розчинів запроваджене поняття водневого показника  :
:

Для розбавлених розчинів, коли концентрація  , коефіцієнт активності
, коефіцієнт активності  і, відповідно, активність
і, відповідно, активність  , тому замість активності іонів гідрогену можна використовувати їх концентрації:
, тому замість активності іонів гідрогену можна використовувати їх концентрації:

В нейтральному середовищі


В кислому середовищі


В лужному середовищі


Наближено реакцію середовища визначають за допомогою індикаторів, які змінюють свій колір залежно від концентрації іонів гідрогену у розчині.
Кислотно – основні індикатори – слабкі органічні кислоти або основи, які змінюють своє забарвлення в разі перетворення кислотної форми на основну і навпаки.
| Індикатор | Кисле середовище | Нейтральне середовище | Лужне середовище |
| Метиловий - оранжевий | Червоний 
| Оранжевий 
| Жовтий 
|
| Фенол - фталеїн | Безбарвний 
| Блідо – малиновий 
| Малиновий 
|
| Лакмус | Червоний 
| Фіолетовий 
| Синій 
|
Для кількісного вимірювання  з точністю до 0,01 використовують
з точністю до 0,01 використовують  - метри.
- метри.
Дата публикования: 2014-11-04; Прочитано: 5656 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
