 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Послідовність виконання роботи
|
|
ЗАВДАННЯ 1. Градуювання монохроматора
Для цього (див.рис.2):
1. Розмістити близько до вхідної щілини монохроматора 1 неонову лампочку 4, яка розміщена в захисному кожусі, і увімкнути її в мережу 220 В.
2. Встановити ширину вхідної щілину монохроматора ~ 0,22 мм.
3. Досягнути чітке зображення спектральних ліній в окулярі 8 монохроматора за допомогою
регулювальних гвинтів 6 та 7, а оптимальну ширину спектральних ліній – незначним регулюванням ширини вхідної щілини монохроматора.
4. Плавно обертаючи барабан 5 довжин хвиль монохроматора, суміщати з візиром монохроматора видимі в окуляр 8 спектральні лінії випромінювання неону та встановлювати відповідність між значеннями 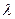 і відносними поділками
і відносними поділками 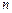 шкали барабана довжин хвиль (для спектру випромінювання неону значення l вказані на робочому місці).
шкали барабана довжин хвиль (для спектру випромінювання неону значення l вказані на робочому місці).
5. Результати вимірювань записати в таблицю 1.
6. Вимкнути з мережі 220 В неонову лампочку і зняти її з оптичної лави.
7. Побудувати графік залежності 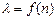 (графік градуювання монохроматора), відкладаючи по осі Х відносні поділки
(графік градуювання монохроматора), відкладаючи по осі Х відносні поділки 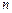 шкали барабана 5 довжин хвиль, а по осі Y − довжини хвиль
шкали барабана 5 довжин хвиль, а по осі Y − довжини хвиль 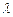 відповідних ліній.
відповідних ліній.
| l, Å | |||||||||
| n, відн. од. |
Таблиця 1
ЗАВДАННЯ 2. Визначення довжин хвиль спектральних ліній випромінювання атомів
Водню та сталої Планка
1. Розмістити на місці неонової лампочки прилад СПЕКТР – 1.
2. Увімкнути прилад СПЕКТР–1 в мережу 220 В і встановити перемикач на ньому в положення “H2”.
3. Переміщаючи окуляр 8 зорової труби монохроматора 1 за допомогою регулювальних гвинтів 6 і 7 добитися чіткого зображення ліній випромінювання атомів водню в окулярі.
4. Дивлячись в окуляр монохроматора, встановлювати почергово поворотом барабана 5 довжин хвиль спектральні лінії випромінювання водню навпроти візира монохроматора і проводити відліки, що відповідають цим лініям, за шкалою барабана монохроматора. Візуальний пошук ліній необхідно починати з найбільш інтенсивної червоної 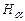 лінії. Одержані результати записати в таблицю 2.
лінії. Одержані результати записати в таблицю 2.
УВАГА! В спектрі водневої трубки поряд з лініями атомного спектру спостерігається спектр молекулярного водню.
Таблиця 2
| Колір і індекс лінії | n, відн.од. | λ, нм | Квантові числа | h·1034, Дж·с | Δ h·1034, Дж·с | δh, 100% | |
| n | k | ||||||
| Яскраво−червона, Ha | |||||||
| Зелено−голуба, Hb | |||||||
| Фіолетово−синя, Hg. | |||||||
Фіолетова,
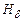
| |||||||
| Сер. | хххх | хххх | хххх | хххх |
5. Користуючись кривою градуювання монохроматора визначити довжини хвиль кожної з ліній випромінювання водню.
6. Розрахувати за формулою (5) сталу Планка, використовуючи довжини 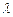 хвиль ліній випромінювання водню:
хвиль ліній випромінювання водню: 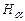 ,
, 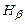 ,
, 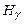 і
і 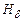 .
.
7. Дані, які одержані в п.п. 5−6, записати в таблицю 2.
8. Проаналізуйте одержані результати і зробіть висновки.
Контрольні запитання
1. Які серії випромінювання, крім серії Бальмера, ще має спектр випромінювання атом водню?
2. Який фізичний зміст мають квантові числа 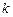 і
і 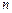 у формулі (1)?
у формулі (1)?
3. Сформулюйте постулати Бора. Як з їх допомогою пояснити лінійчатий характер спектру випромінювання атома водню?
4. Які фізичні величини необхідно знати для того, щоб розрахувати постійну Планка в даній роботі?
5. Знайдіть частоту обертання електрона в атомі водню.
6. Виведіть формулу, яка визначає повну енергію електрона в атомі водню.
Дата публикования: 2014-11-04; Прочитано: 508 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
