 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Второе начало термодинамики
|
|
Понятие энтропии помогло строго математически сформулировать закономерности, позволяющие определить направление тепловых процессов. Огромная совокупность опытных фактов показывает, что для замкнутых систем возможны только такие процессы, при которых энтропия системы возрастает или остается постоянной. Это утверждение носит название второго закона (начала) термодинамики. Математическая запись второго начала имеет вид
dS ³ 0, (10.27)
где S - полная энтропия замкнутой системы.
Применим второе начало термодинамики для выяснения направления некоторых тепловых процессов.

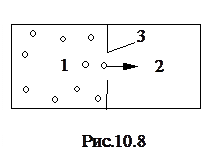 1. Рассмотрим расширение идеального газа в пустоту. Пусть газ первоначально находится в сосуде 1 (рис.10.8). Затем открывается заслонка 3, и молекулы из сосуда 1 могут перемещаться в сосуд 2. Так как в системе нет движущихся частей, то скорость молекул не изменяется и процесс расширения газа будет изотермическим (T1 = T2). Применяя второе начало термодинамики и учитывая равенство (10.26), получим (m /m)R ln (V2 /V1) ³ 0. Отсюда следует, что ln V2 ³ ln V1 или V2 ³ V1 . Применив второе начало термодинамики к газу, мы получили, что газ, предоставленный самому себе, может только расширяться. Второе начало термодинамики показывает, что невозможен процесс, в результате которого газ соберется в какой-то определенной части объема. Хотя, исходя из чисто механических представлений, процесс, обратный расширению газа в пустоту, кажется возможным.
1. Рассмотрим расширение идеального газа в пустоту. Пусть газ первоначально находится в сосуде 1 (рис.10.8). Затем открывается заслонка 3, и молекулы из сосуда 1 могут перемещаться в сосуд 2. Так как в системе нет движущихся частей, то скорость молекул не изменяется и процесс расширения газа будет изотермическим (T1 = T2). Применяя второе начало термодинамики и учитывая равенство (10.26), получим (m /m)R ln (V2 /V1) ³ 0. Отсюда следует, что ln V2 ³ ln V1 или V2 ³ V1 . Применив второе начало термодинамики к газу, мы получили, что газ, предоставленный самому себе, может только расширяться. Второе начало термодинамики показывает, что невозможен процесс, в результате которого газ соберется в какой-то определенной части объема. Хотя, исходя из чисто механических представлений, процесс, обратный расширению газа в пустоту, кажется возможным.
2. Рассмотрим процесс теплообмена при конечной разности температур. Пусть тело с температурой T1 передает тепло DQ телу с температурой T2 (рис.10.9). Полное изменение энтропии системы тел равно DS = DS1 + DS2, где DS1 = - DQ/T1 - уменьшение энтропии первого тела, DS2 = DQ/T2 - увеличение энтропии второго тела. По второму началу термодинамики полное изменение энтропии системы DS = DQ(T1 - T2)/T1T2 ³ 0. Отсюда получаем T1 ³ T2. Итак, из второго начала термодинамики следует, что тепло должно передаваться от более нагретого тела к менее нагретому телу, т.е. второе начало термодинамики определяет направление процесса передачи тепла. Клаузиус предложил записать второе начало как утверждение: невозможен самопроизвольный переход тепла от менее нагретого тела к более нагретому.
 3. Рассмотрим работу тепловой машины. Нагреватель отдает рабочему телу в течение рабочего цикла количество тепла DQ’1 при температуре T1 (рис.10.10), его энтропия изменяется (уменьшается) на величину DS1 = - D
3. Рассмотрим работу тепловой машины. Нагреватель отдает рабочему телу в течение рабочего цикла количество тепла DQ’1 при температуре T1 (рис.10.10), его энтропия изменяется (уменьшается) на величину DS1 = - D 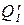 /T1. Рабочее тело отдает количество тепла DQ2 при температуре T2 холодильнику, энтропия которого увеличивается на величину DS2 = DQ2 /T2 . Энтропия рабочего тела не меняется, так как через цикл оно имеет прежние параметры состояния. Согласно второму началу термодинамики DS1 + DS2 ³ 0. Знак равенства соответствует выражению (9.22) для цикла Карно. Итак, полученное из второго начала термодинамики неравенство будет выполняться, когда часть полученного рабочим телом тепла DQ2 будет неизбежно передана холодильнику. В противном случае энтропия замкнутой системы уменьшается. Это указывает на обесцененность тепловой энергии по сравнению с другими видами энергии. Несмотря на огромные запасы тепловой энергии, ее использование возможно лишь при разности температур между телами системы. При тепловом равновесии системы превращение ее тепловой энергии в механическую невозможно. Кельвин предложил записать проведенное рассуждение как следующую формулировку второго начала термодинамики: невозможен процесс, единственным результатом которого явилось бы отнятие от какого либо тела определенного количества тепла и превращение этого тепла полностью в работу. Иными словами, невозможен вечный двигатель второго рода, единственным результатом которого было бы производство работы за счет тепла некоего резервуара.
/T1. Рабочее тело отдает количество тепла DQ2 при температуре T2 холодильнику, энтропия которого увеличивается на величину DS2 = DQ2 /T2 . Энтропия рабочего тела не меняется, так как через цикл оно имеет прежние параметры состояния. Согласно второму началу термодинамики DS1 + DS2 ³ 0. Знак равенства соответствует выражению (9.22) для цикла Карно. Итак, полученное из второго начала термодинамики неравенство будет выполняться, когда часть полученного рабочим телом тепла DQ2 будет неизбежно передана холодильнику. В противном случае энтропия замкнутой системы уменьшается. Это указывает на обесцененность тепловой энергии по сравнению с другими видами энергии. Несмотря на огромные запасы тепловой энергии, ее использование возможно лишь при разности температур между телами системы. При тепловом равновесии системы превращение ее тепловой энергии в механическую невозможно. Кельвин предложил записать проведенное рассуждение как следующую формулировку второго начала термодинамики: невозможен процесс, единственным результатом которого явилось бы отнятие от какого либо тела определенного количества тепла и превращение этого тепла полностью в работу. Иными словами, невозможен вечный двигатель второго рода, единственным результатом которого было бы производство работы за счет тепла некоего резервуара.
Дата публикования: 2014-11-04; Прочитано: 554 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
