 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Скорость реакций
|
|
Количественной характеристикой быстроты течения химической реакции А + B → D + E является ее скорость, т. е. скорость взаимодействия частиц реагентов А и В или скорость появления продуктов D и Е. Изучением скорости химических реакций занимается особый раздел химии – химическая кинетика.
В гомогенных (однородных) системах исследуется скорость реакции между реагентами, не имеющими границы раздела (газовые реакции, реакции в растворах). В гетерогенных системах изучается скорость реакции на поверхности раздела между реагирующими веществами (например, А – твердое вещество, В – газ или А – твердое вещество, В – вещество в растворе).
Для гомогенных систем скорость реакции – это изменение концентраций реагентов или продуктов в единицу времени:
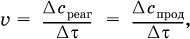
где v – скорость реакции, моль/(л с);
Δcреаг = (с'реаг – с"реаг) ― уменьшение концентрации реагентов, моль/л, за промежуток времени Δτ = τ2 – τ1;
Δcпрод = (с"прод – с'прод) – увеличение концентрации продуктов, моль/л, за тот же промежуток времени.
В начальный момент времени (τ = 0) концентрация реагентов наибольшая, а концентрация продуктов равна нулю. В процессе реакции концентрация реагентов уменьшается, а концентрация продуктов растет.
К факторам, влияющим на скорость реакции, относятся природа реагентов, катализатор, температура, концентрация реагентов.
1. Природа реагентов. Здесь большую роль играет характер химических связей в соединениях, строение их молекул. Например, выделение водорода цинком из раствора хлороводорода происходит значительно быстрее, чем из раствора уксусной кислоты, так как полярность связи Н – Cl больше, чем связи О – Н в молекуле СН3СООН; иначе говоря, из‑за того, что НCl – сильный электролит, а СН3СООН – слабый электролит в водном растворе.
Чем больше поверхность соприкосновения реагирующих веществ, тем быстрее протекает реакция. Поверхность твердого вещества может быть увеличена путем его измельчения или растворения (если вещество растворимо). Реакции в растворах протекают практически мгновенно.
2. Катализаторы. Большое влияние на скорость реакции оказывают катализаторы – вещества, увеличивающие скорость реакции (часто от нуля до очень больших значений), но не входящие в состав продуктов. Увеличение скорости реакции под влиянием катализаторов называется катализом. Во многих случаях катализаторы образуют с одним из реагирующих веществ промежуточное соединение, которое реагирует с другим исходным веществом, в результате получается продукт и высвобождается катализатор.
Иногда употребляют отрицательные катализаторы – ингибиторы, которые, наоборот, замедляют нежелательные химические реакции (например, коррозию металлов).
3. Температура. Для газовых реакций известно, что при повышении температуры на десять градусов (Δ Т = 10 К или Δ t = 10 °C) скорость реакции возрастает в 2–4 раза ( правило Вант‑Гоффа). Для скорости реакции ν2 и ν1 при значениях температуры t 2 и t 1 имеем:
ν 2 = ν 1 γ 0,1(t2‑t1),
где γ – температурный коэффициент скорости реакции, γ = 2–4.
Для реакций в растворах скорость также увеличивается с ростом температуры и часто в той же мере, как и для газовых реакций.
При повышении температуры возрастает число активных молекул, т. е. таких молекул, которые в момент столкновения обладают большей энергией и могут образовать продукты.
Как показывают исследования, активных молекул в реакционной среде при обычных условиях очень мало. Иначе все реакции между газами протекали бы мгновенно, и в воздухе не было бы, например, свободного кислорода, необходимого для дыхания. Реакции между газами при обычных условиях практически не идут (встречаются исключения, например, при 20 °C полностью протекает реакция 2NO + O2 = 2NO2).
4. Концентрация реагентов. Чтобы произошло взаимодействие, частицы реагирующих веществ в гомогенной среде должны столкнуться. Число столкновений пропорционально числу частиц реагирующих веществ в объеме реактора, т. е. молярным концентрациям этих веществ.
Чем большие количества веществ взяты для реакции в данном объеме системы, т. е. чем выше концентрация реагентов, тем больше число столкновений частиц и тем больше скорость реакции. Зависимость скорости реакции от концентрации реагентов распространяется на газовые смеси и растворы.
Установлено, что:
Дата публикования: 2014-11-04; Прочитано: 1714 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
