 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Гипохлориты. Хлораты
|
|
Гипохлорит кальция Са(СlO)2. Соль хлорноватистой кислоты HClO. Белый, при нагревании разлагается без плавления. Хорошо растворим в холодной воде (образуется бесцветный раствор), гидролизуется по аниону. Реакционноспособный, полностью разлагается горячей водой, кислотами. Сильный окислитель. При стоянии раствор поглощает углекислый газ из воздуха. Является активной составной частью хлорной (белильной) извести – смеси неопределенного состава с СаCl2 и Са(ОН)2. Уравнения важнейших реакций:
Са(ClO)2 = СаCl2 + O2 (180 °C)
Са(ClO)2(т) + 4НCl (конц.) = СаCl2 + 2Cl2↑ + 2Н2O (80 °C)
Са(ClO)2 + Н2O + СO2 = СаСO3↓ + 2НClO (на холоду)
Са(ClO)2 + 2Н2O2 (разб.) = СаCl2 + 2Н2O + 2O2↑
Получение:
2Са(ОН)2 (суспензия) + 2Cl2(г) = Са(ClO)2 + СаCl2 + 2Н2O
Хлорат калия КСlO3. Соль хлорноватой кислоты НСlO3, наиболее известная соль кислородсодержащих кислот хлора. Техническое название – бертоллетова соль (по имени ее первооткрывателя К.‑Л. Бертолле, 1786). Белый, плавится без разложения, при дальнейшем нагревании разлагается. Хорошо растворим в воде (образуется бесцветный раствор), гидролиза нет. Разлагается концентрированными кислотами. Сильный окислитель при сплавлении.
Применяется как компонент взрывчатых и пиротехнических смесей, головок спичек, в лаборатории – твердый источник кислорода.
Уравнения важнейших реакций:
4КClO3 = ЗКClO4 + КCl (400 °C)
2КClO3 = 2КCl + 3O2 (150–300 °C, кат. MnO2)
КClO3(т) + 6НCl (конц.) = КCl + ЗCl2| + ЗН2O (50–80 °C)
ЗКClO3(т) + 2H2SO4 (конц., гор.) = 2ClO2| + КClO4 + Н2O + 2KHSO4
(диоксид хлора на свету взрывается: 2ClO2(г) = Cl2 + 2O2)
2КClO3 + Е2(изб.) = 2КЕO3 + Cl2↑ (в разб. HNO3, Е = Br, I)

Получение КClO3 в промышленности – электролиз горячего раствора КCl (продукт КClO3 выделяется на аноде):
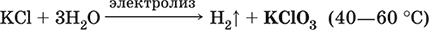
Дата публикования: 2014-11-04; Прочитано: 1826 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
