 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Спиртовое брожение
|
|
Гликолиз является первым этапом спиртового брожения. Образовавшаяся пировиноградная кислота декарбоксилируется при участии декарбоксилазы в ацетальдегид, который затем восстанавливается до этанола. Эта реакция осуществляется алкогольдегидрогеназой с участием НАДН2 (табл.5.2). В ходе этой реакции НАДН2 окисляется до НАД+ (см. рис 5.1), который далее вновь участвует в гликолизе. Именно за счет использования ацетальдегида в качестве конечного акцептора электронов клетка обеспечивает дальнейшее функционирование гликолитического пути и, в следствие этого, дальнейшее образование АТФ для использования в биосинтетических реакциях.
Энергетический и химический баланс брожения приведен наже (ур-ие 5.2)
С 6 Н 12 О 6 + 2 АДФ + 2 Фн® 2СО2 + 2 СН 3СН2 ОН + 2АТФ + 2 Н20 + 61 кдж [d1] [d2]
(5.2)
Таким образом выход АТФ в пути ЭМП составляет 2 молекулы на молекулу глюкозы. Эффективность брожения составляет 26%; 74% энергии, не удерживается клеткой, и в основном рассеивается в виде тепла, поэтому следует применять охлаждение аппаратов. Скорость брожения не постоянна, и наибольшая активность наблюдается первые 24-36 ч. Затем в виду ингибирования клеток этанолом этот процесс замедляется.
Для протекания спиртового брожения в питательной среде должны присутствовать тиамин (витамин В1), а также ионы Zn+2, Co, Mg+2 и Mn+2. (табл.5.2). Например, увеличение концентрации ацетальдегида вследствие замедления его восстановления в этанол происходит из-за недостатка ионов Zn+2 в среде, в результате Ф-1,6-Ф идет на биосинтез глицерина (рис.5.1). Кислород является ингибитором брожения (эффект Пастера), механизм этого процесса будет рассмотрен далее.
Таблица 5. 2 Активаторы и ингибиторы спиртового брожения.
| Фермент | Кофермент, кофактор | Активатор, стимулятор | Ингибитор |
| Пируватдекарбоксилаза | Тиаминпирофосфат | Тиамин, Mg =2, Mn+2 или Со+2 | Ацетальдегид, О2 |
| Алкогольдегидрогеназа | НАДН, Zn+2 | - | - |
Гликолитическая последовательность реакций является примером амфиболического пути, в ходе которого различные промежуточные продукты используются клеткой в биосинтетических реакциях:
– фосфорилированная глюкоза (Гл-1-Ф) является предшественником в синтезе полимеров клеточной стенки и резервных углеводов;
– триозофосфаты используются в синтезе жиров;
– фосфоенолпируват и пируват являются предшественниками некоторых аминокислот (рис.5.2).
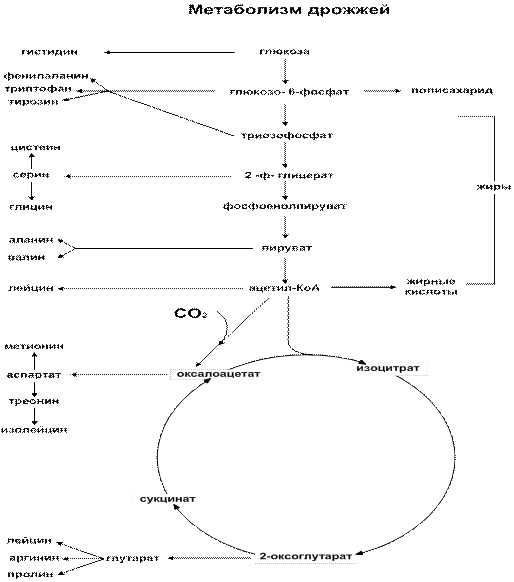
Рисунок 5.2 – Биосинтез аминокислот
Однако, размножающиеся клетки требуют значительно больше промежуточных продуктов для биосинтетических реакций, чем может предоставить путь ЭМП. Это такие вещества, как сукцинат, 2-оксоглутарат, оксалоацетат, которые являются предшественниками в синтезе 8 аминокислот (рис. 5.2). У дышащих дрожжевых клеток, то есть таких, которые используют молекулярный кислород в качестве акцептора водорода и полностью окисляют глюкозу, интез предшественников аминокислот протекает в цикле Кребса (ЦТК).
В анаэробных условиях активность ферментов цикла Кребса низкая. В результате из-за недостатка ключевого фермента 2-оксоглутаратдегидрогеназы, активность которого определяется концентрацией растворенного в среде кислорода, на участке сукцинат – 2-оксоглутарат ЦТК разомкнут (см. рис 5.1).
При недостатке в среде растворенного кислорода у дрожжей функционируют два механизма, которые обеспечивают клетку необходимыми метаболитами: первый предусматривает образование сукцината, фумарата, малата и оксалацетата в окислительном процессе, в то время как второй включает синтез дополнительных ферментов для образования 2-оксоглутарата по восстановительному пути (см.рис 5.1). Согласно обоим механизмам пируват превращается в ацетил-КоА в реакции, включающей пируватдегидрогеназный комплекс, в состав которого входит пируватдегидрогеназа, дигидроамидацетилтрансфераза, дигидроамидредуктаза. В качестве коферментов комплекс содержит Mg+2, тиаминпирофосфат, флавинадениндинуклеотид (ФАД) и никотинамиддинуклеотид (НАД).
Суммарнаяя реакция имеет следующий вид:
Пируват + КоА-SН + НАД+ ® СО2 + Ацетил-SКоА + НАДН2 (5.3)
Таким образом, обмен глюкозы при недостатке кислорода в среде соответствует ЦТК в аэробном метаболизме: окислительный путь ведет от оксалоацетата к 2-оксоглутарату, восстановительный – к сукцинату.
Вовлечение оксалоацетата в разорванный ЦТК предполагает дополнительный синтез оксалоацетата за счет протекания анаплеротической (восполняющей) реакции (ур-ие 5.4). Катализирует эту реакцию АТФ и пируваткарбоксилаза – фермент, в котором биотин является простетической группой, а цинк - коферментом. Это единственная реакция, которую можно рассматривать как анаплеротическую в ходе ЦТК, которая восполняет недостаток оксалоацетата, расходуемого для биосинтетических реакций.
Пируват + СО2 + АТФ ® оксалоацетат + АДФ (5.4)
Дата публикования: 2015-11-01; Прочитано: 993 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
