 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Нақты газдар
|
|
Менделеев-Клапейрон теңдеуі молекулалары бір-бірімен әсерлеспейтін және нүкте деп қарастырылатын идеал газдардың күйін анықтайды. Нақты газдардың молекуларының өлшемдері болады және олар бір-бірімен өзара әсерлеседі. Нақты газдардың күйін анықтайтын теңдеуді алу үшін голланд ғалымы Ван-дер-Ваальс Менделеев-Клапейрон теңдеуіне молекулаларды өлшемдерін және өзара әсерлесуін ескеретін түзету енгізді. Бұл алынған теңдеу нақты газдардың күй теңдеуі немесе Ван-дер-Ваальс теңдеуі деп аталады. Мөлшері 1 моль нақты газ үшін Ван-дер-Ваальс теңдеуі келесі түрде жазылады:
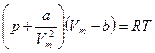 ,
,
мұндағы: 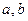 -Ван-дер-Ваальс тұрақтылары, өлшем бірліктері
-Ван-дер-Ваальс тұрақтылары, өлшем бірліктері 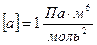 ,
, 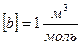 .
.
Бірінші жақша ішіндегі 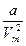 түзетуі молекулалардың арасындағы тартылыс күшінің әсерінен пайда болады. Оны кейде ішкі қысым деп атайды.
түзетуі молекулалардың арасындағы тартылыс күшінің әсерінен пайда болады. Оны кейде ішкі қысым деп атайды. 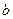 түзетуі молекулалардың өлшемдерін ескереді. Кез-келген мөлшердегі нақты газ үшін Ван-дер-Ваальс теңдеуі
түзетуі молекулалардың өлшемдерін ескереді. Кез-келген мөлшердегі нақты газ үшін Ван-дер-Ваальс теңдеуі  екенін ескере отырып келесі түрде жазылады:
екенін ескере отырып келесі түрде жазылады:
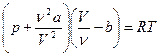 немесе
немесе 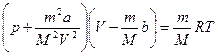 .
.
Нақты газдардың ішкі энергиясы 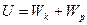 өрнегімен анықталады, мұндағы
өрнегімен анықталады, мұндағы 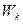 - молекулалардың қосынды кинетикалық энергиясы,
- молекулалардың қосынды кинетикалық энергиясы, 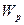 -молекулалардың қосынды өзара әсерлесу энергиясы.
-молекулалардың қосынды өзара әсерлесу энергиясы. 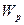 энергиясын анықтайық. Ол үшін молекулалардың арасындағы тартылу күшінің жұмысы
энергиясын анықтайық. Ол үшін молекулалардың арасындағы тартылу күшінің жұмысы 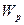 энергиясының кемуіне тең екенін ескереміз, яғни
энергиясының кемуіне тең екенін ескереміз, яғни 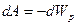 . Молекулалардың арасындағы тартылу күші
. Молекулалардың арасындағы тартылу күші 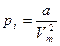 ішкі қысыммен сипатталады. Сондықтан
ішкі қысыммен сипатталады. Сондықтан 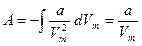 және
және 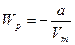 .Молекулалардың қосынды
.Молекулалардың қосынды 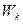 кинетикалық энергиясы олардың қозғалысына тәуелді болады.Сондықтан Ван-дер-Ваальс газының 1 молінің ішкі энергиясы
кинетикалық энергиясы олардың қозғалысына тәуелді болады.Сондықтан Ван-дер-Ваальс газының 1 молінің ішкі энергиясы
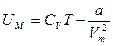 , мұндағы:
, мұндағы: 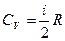 .
.
Дата публикования: 2015-11-01; Прочитано: 1436 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
