 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Адиабатическое размагничивание парамагнетиков
|
|
Адиабатическое размагничивание или магнитно-калорический эффект реализуется в термомагнитных системах. При адиабатическом размагничивании парамагнитных веществ, также как при адиабатическом расширении газа, работа против внешних сил совершается за счет затраты внутренней энергии системы и поэтому приводит к резкому снижению температуры.
Для охлаждения этим способом парамагнитное вещество (обычно брусок парамагнитной соли) выдерживается при постоянной температуре в условиях глубокого вакуума, например, в ванне кипящего гелия. Вещество находится под действием сильного магнитного поля. При выключении поля происходит адиабатическое размагничивание, позволяющее охладить парамагнитное вещество до температуры, близкой к абсолютному нулю. В настоящее время созданы магнитные холодильные машины, использующие этот эффект для получения температур ниже 1К.
В настоящее время адиабатическое размагничивание используют для охлаждения до сверхнизких температур экспериментальных образцов в лабораторных условиях.
РАЗДЕЛ 1 ТЕОРЕТИЧЕСКИЕ ПРОЦЕССЫ ПОЛУЧЕНИЯ ХОЛОДА
Термодинамические основы теории холодильных машин
Основные понятия и законы термодинамики
Искусственным охлаждением называется процесс переноса теплоты от тел с более низким температурным уровнем к телам с более высоким температурным уровнем за счет затраты внешней работы.
Назначение холодильной машины состоит в отводе теплоты от охлаждаемого объекта, имеющего низкую температуру, и передаче отведенной теплоты более теплой окружающей среде. Принцип действия холодильной машины определяется основными законами термодинамики.
Состояние любой термодинамической системы характеризуется следующими параметрами состояния: давлением, температурой, удельным объемом, внутренней энергией, энтальпией, энтропией. При изменении параметров состояния изменяется и состояние системы.
Давление, температура и удельный объем являются термическими параметрами системы, которые можно измерить. Внутренняя энергия, энтальпия и энтропия не могут быть измерены и являются расчетными параметрами.
Внутренняя энергия зависит только от внутреннего состояния системы и обусловлена энергией микрочастиц, входящих в составляющие системы, а также энергией взаимодействия между этими частицами.
Определение энтальпии следует из первого закона термодинамики. Первый закон устанавливает, что количество теплоты, прошедшее через контрольную поверхность термодинамической системы, затрачивается на изменение внутренней энергии и работу, совершенную системой. Энтальпия - это полная энергия рабочего вещества в открытой системе, т.е. энергетический параметр состояния вещества, определяемый из уравнения:

| (1) | |||
| где | U | - | внутренняя энергия вещества, Дж; | |
| Р | - | давление, Па; | ||
| V | - | объем вещества, м3. | ||
В термодинамике обычно используется удельная энтальпия, равная отношению энтальпии к массе вещества.

| (2) | |||
| где | u | - | удельная внутренняя энергия вещества, Дж/кг; | |
| v | - | удельный объем вещества, м3/кг. | ||
Определение энтропии вытекает из второго закона термодинамики, который устанавливает, что перенос теплоты от системы с более низкой температурой к системе с более высокой температурой не может происходить самопроизвольно, а для его осуществления необходимо затратить механическую работу или эквивалентное количество другой энергии. Направление процесса теплообмена системы с окружающей средой, а также направление любых самопроизвольных процессов в изолированной системе характеризуется особым параметром состояния системы - энтропией.
Полный дифференциал энтропии определяется из выражения:
 , ,
| (3) | |||
| где | dQ | - | количество теплоты, участвующее в квазистатическом, т.е. обратимом процессе теплообмена, Дж; | |
| Т | - | абсолютная температура, при которой происходит процесс, К. | ||
На практике про проведении расчетов пользуются понятием удельной энтропии, измеряемой в [Дж/(кг×К)]:
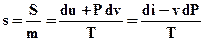 . .
| (4) |
Как известно из термодинамики, перенос теплоты с низшего температурного уровня на высший сопровождается уменьшением энтропии и поэтому не может происходить самопроизвольно. Для того, чтобы осуществить такой процесс, его необходимо сочетать с другим процессом, протекающим с возрастанием энтропии, т.е. с затратой энергии, и компенсирующим уменьшение энтропии в процессе отвода тепла от среды с более низкой температурой.
Дата публикования: 2015-10-09; Прочитано: 1610 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
