 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Моносахариди
|
|
Залежно від числа атомів вуглецю в молекулі розрізняють тріози, тетрози, пентози, гексози і т. д. Наведемо. приклади таких моносахаридів:

Префікси альдо- або кето- показують, де розміщена карбонільна група: на кінці молекулярного ланцюга чи в середині його.
Найбільше значення з моносахаридів мають глюкоза і фруктоза.
Глюкоза - альдогексоза складу C2H12O6. Вона трапляється у рослинних і тваринних організмах. Так, її багато в соку винограду, тому її називають виноградним цукром. Вона міститься також і в інших фруктах і ягодах, у меду, в крові людини.
Глюкоза-безбарвна кристалічна речовина, розчинна у воді. Вивчення хімічної будови і властивостей цього моносахариди показало, що він може існувати в різних формах: альдегідній і двох циклічних, які одночасно співіснують і можуть переходити одна в одну:

У наведених формулах циклічних структур для відображення їх просторової будови шестикутний цикл показаний розміщеним горизонтально (перпендикулярно до площини рисунку), а замісники – над або під циклом.
Явище одночасного існування кількох форм однієї речовини, які перебувають у рівновазі, називається таутомерією. Таутомерні форми не є ізомерами, оскільки не можуть бути виділені в індивідуальному стані, а завжди співіснують разом.
Гідроксильна група біля першого атома вуглецю (C1) в a- і b- формах глюкози називається глікозидною. При переході глюкози в альдегідну форму за рахунок цієї гідроксильної групи утворюється карбонільна група.
Ізомером глюкози є фруктоза, або фруктовий цукор. Склад цієї речовини також відповідає формулі C6H12O6, але на відміну від глюкози фруктоза є кетоноспиртом. Фруктоза має три таутомерні форми, дві з яких – циклічні:

Фруктоза міститься у багатьох фруктах і меду.
Хімічні властивості глюкози обумовлені наявністю гідроксильних і карбонільної (в альдегідній формі) груп.
1) Глюкоза як спирт вступає в реакції етерифікації з органічними кислотами, утворюючи складні ефіри, наприклад:

2) Як альдегід, глюкоза легко окислюється. Під дією аміачного розчину оксиду срібла глюкоза вступає в реакцію срібного дзеркала, окислюючись до спирту кислоти. Глюкоза окислюється також гідроксидом міді (II) з утворенням червоно-коричневого оксиду міді(I) Cu2O. Ця реакція є якісною на глюкозу. Звичайно для її здійснення використовують реактив Фелінга: розчин CuSO4 в гідроксиді натрію з деякими добавками.
При повному окисленні глюкоза руйнується до CO2 і води:
C6H12O6+6O2  6CO2+6H2O.
6CO2+6H2O.
3)Глюкоза може бути відновлена до шестиатомного спирту – сорбіту:
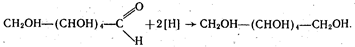
4) Під час взаємодії глюкози з метанолом при наявності хлороводню утворюються глюкозиди:

Водень у глікозидному гідроксилі заміщений на групу CH3, в результаті глюкозиди можуть існувати тільки в циклічній формі і альдегідних властивостей не виявляють.
5) Під дією органічних каталізаторів – ферментів – глюкоза піддається бродінню. Один з видів бродіння – спиртове бродіння, в результаті якого утворюється етиловий спирт:
C6H12O6  2C2H5OH+2CO2.
2C2H5OH+2CO2.
Інший вид – молочнокисле бродіння:
C6H12O6  2CH3-CHOH-COOH
2CH3-CHOH-COOH
Молочна кислота
Глюкоза у великих кількостях виробляється промисловістю. Вона є цінним харчовим продуктом, лікувальним препаратом.
Фізичні властивості. Моносахариди уявляють із себе тверді кристалічні речовини. Усі вони гігроскопічні, добре розчинні у воді, легко утворюють сироп, із якого їх виділити у кристалічному виді дуже тяжко. У спирті моносахариди розчиняються погано, у ефірі зовсім не розчинні. Розчини моносахаридів мають нейтральну реакцію на лакмус та взагалі володіють солодким смаком. Солодкість різних моносахаридів дуже різна. Наприклад, фруктоза приблизно у три рази солодша за глюкозу. Розчини моносахаридів володіють оптичною активністю, для них характерно явище мутаротації.
Лекція № 16
Тема: Дисахариди. Полісахариди.
Мета: Вивчити властивості сахарози, крохмалю та целюлози, їх структурні формули, склад, добування та застосування.
План:
1. Властивості сахарози, добування та застосування.
2. Властивості крохмалю, добування та застосування.
3. Властивості целюлози, добування та застосування.
Олігосахариди (дисахариди).
Олігосахариди – продукти, побудовані з двох або кількох (до десяти) моносахаридів. Серед них найбільше значення мають дисахариди.
Найважливіший дисахарид – сахароза C12H22O11. Її називають також буряковим або тростинним цукром, оскільки сахароза міститься в цукровому буряку і цукровій тростині.
Сахароза – безбарвна кристалічна речовина, розчинна у воді.
Молекули сахарози складаються з двох залишків моносахаридів – глюкози в  - формі і фруктози у формі фруктофуранози:
- формі і фруктози у формі фруктофуранози:

Залишок глюкози сполучений із залишком фруктози за рахунок глікозидного гідроксилу, тому залишок глюкози перебуває тільки в циклічній формі. В результаті на відміну від глюкози сахароза не вступає в реакції, типові для альдегідів.
Характерною властивістю сахарози (і взагалі всіх олігосахаридів) є здатність їх гідролізуватися при наявності кислот з утворенням двох моносахаридів:
C12H22O11+H2O  C6H12O6+C6H12O6.
C6H12O6+C6H12O6.
Глюкоза Фруктоза
Сахароза є важливим харчовим продуктом. У великих кількостях її добувають із цукрового буряка і цукрової тростини.
Полісахариди.
Полісахариди – продукти конденсації великої кількості молекул моносахаридів. Найважливішими природними полісахаридами є крохмаль і целюлоза.
Крохмаль. Крохмаль міститься у багатьох рослинах. Його багато в зернових культурах (рисі, кукурудзі, пшениці) і в картоплі, з якої крохмаль звичайно добувають у промисловості. У рослинах крохмаль утворюється в результаті фотосинтезу.
За зовнішнім виглядом крохмаль – білий порошок. У воді не розчинний. У гарячій воді крохмаль набрякає і утворює клейстер, який є колоїдним (не істинним) розчином.
Крохмаль – це суміш двох полісахаридів однакового складу (C6H10O5) n – амілози і амілопектину.
Амілоза – лінійний полімер, що складається із залишків глюкози в  - формі:
- формі:

Амілопектин також побудований із залишків  - глюкози, проте ці залишки сполучаються іншим способом, утворюючи розгалужену структуру:
- глюкози, проте ці залишки сполучаються іншим способом, утворюючи розгалужену структуру:

Масова частка амілози в крохмалі звичайно становить 10-20%, амілопектину – 80-90%.
З будови макромолекул амілози і амілопектину видно, що в крохмалі немає карбонільних груп, тому він не виявляє хімічних властивостей, типових для альдегідів і кетонів.
Для крохмалю (і для всіх полісахаридів) характерний гідроліз. При частковому гідролізі крохмалю утворюються декстрини – полісахариди складу (C6H10O5) n, молекулярна маса яких менша, ніж крохмалю. Декстрини утворюються також під час термічної обробки крохмалю. В результаті повного гідролізу крохмалю утворюється глюкоза:
(C6H10O5) n + n H2O  n C6H12O6.
n C6H12O6.
Повний гідроліз крохмалю здійснюється при наявності кислот.
Гідроліз крохмалю до глюкози відбувається в процесі травлення. Глюкоза всмоктується кишками, поступає в кров і накопичується в печінці, перетворюючись там на тваринний полісахари – глікоген. Вуглеводи з печінки йдуть на живлення всіх тканин організму.
Специфічною реакцією є взаємодія з йодом. При цьому крохмаль утворює сполуку, що має темно-синє забарвлення. Цю реакцію використовують для якісного визначення крохмалю і йоду.
Крохмаль використовується в харчовій промисловості. З нього добувають глюкозу, дестерини і патоку – продукт неповного гідролізу крохмалю (суміш глюкози і декстринів).
Целюлоза. Целюлоза входить до складу багатьох рослинних організмів. Волокна бавовнику складаються в основному з целюлози (її масова частка 98%). Целюлоза становить приблизно половину маси деревини, утворюючи оболонку рослинних клітин. У траві і листі дерев міститься 10-25% целюлози.
Природна целюлоза – тверда біла волокниста речовина. У воді практично не розчинна.
Целюлоза складається із структурних залишків 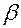 -глюкози, сполучених у лінійні макромолекули:
-глюкози, сполучених у лінійні макромолекули:

Склад целюлози передається такою самою формулою, як і крохмалю, (C6H10O5) n.
Целюлоза піддається гідролізу при нагріванні з розчинами неорганічних кислот:
(C6H10O5) n + n H2O  n C6H12O6.
n C6H12O6.
Як і при гідролізі крохмалю, кінцевий продукт гідролізу целюлози – глюкоза.
До складу кожної структурної ланки целюлози входять три гідроксильні групи, тому целюлоза може давати складні ефіри з органічними і неорганічними кислотами:
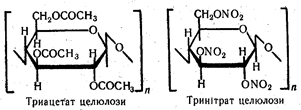
Целюлоза добре горить, утворюючи CO2 і воду. Під час термічної обробки целюлози без доступу повітря утворюються деревне вугілля, вода і ряд органічних речовин, наприклад метанол, ацетон, оцтова кислота.
Целюлоза має різноманітне застосування. У вигляді деревини вона є важливим будівельним матеріалом. У свою чергу, з деревини виділяють целюлозу, що йде на виробництво паперу і картону. З целюлози бавовнику та льону виробляють нитки і тканини.
Ефір оцтової кислоти (триацетат) застосовують у виробництві кіноплівки та електроізоляційної плівки. Крім того, з цього поліефіру виробляють ацетатне волокно – важливий текстильний матеріал. З целюлози добувають і штучні волокна – віскозне та мідно-аміачне. При добуванні цих волокон целюлозу спочатку переводять у розчинну сполуку, а потім регенерують. Тому волокна обох цих видів – чиста целюлоза.
Широке застосування мають ефіри целюлози з азотною кислотою. Тринітрат целюлози – вибухова речовина, застосовується у виробництві пороху. Суміш моно- і динітратів целюлози використовують у виробництві целулоїду, лаків, вибухових речовин.
Гідролізом целюлози в промисловості виробляють глюкозу, бродінням якої добувають етиловий спирт.
Лекція № 17
Тема: Білки.
Мета: Вивчити якісні реакції на білки, структуру білка, значення білків, властивості.
План:
1. Структура білка. Класифікація білків.
2. Кольорові реакції білків.
3. Значення білків.
Білки
Білками називають природні полімерні речовини, які складаються із залишків  -амінокислот. Амінокислоти в білках сполучені пептидними зв'язками С—N. Структуру ланцюга такого білкового полімеру можна подати так:
-амінокислот. Амінокислоти в білках сполучені пептидними зв'язками С—N. Структуру ланцюга такого білкового полімеру можна подати так:

де 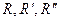 — бічні радикали однакових або різних
— бічні радикали однакових або різних  -амінокислот.
-амінокислот.
Число залишків амінокислот, які входять до пептидного ланцюга, буває дуже значним, тому відносні молекулярні маси білків можуть досягати кількох мільйонів.
До поширених білків належать альбумін (міститься в курячих яйцях), гемоглобін (у крові людини), казеїн (у коров'ячому молоці), міоглобін та міозин (у м'язах). Білки є одними з найважливіших біологічних речовин: вони необхідні для життєдіяльності організмів.
Серед білків виділяють прості білки, або протеїни, пептидні ланцюги яких створюються тільки  -амінокислотами, і складні білки, або протеїди, які
-амінокислотами, і складні білки, або протеїди, які
складаються із залишків  - амінокислот та небілкових речовин.
- амінокислот та небілкових речовин.
Структура білка. Сучасні експериментальні методи дали змогу встановити структуру природних білків. Розрізняють первинну, вторинну, третинну і четвертинну структури білка.
Первинна структура білка —це структура пептидного ланцюга, тобто амінокислотний склад і послідовність черговості залишків амінокислот у ланцюгу білкової молекули.
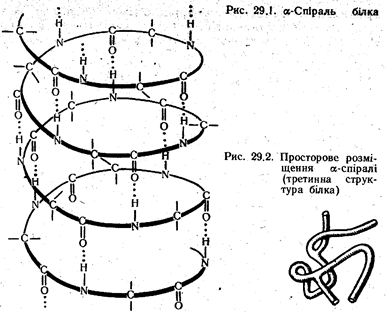
Пептидний ланцюг має певну просторову форму, яка становить вторинну структуру білка. У природних білках пептидний ланцюг має форму спіралі, звичайно її називають  -спіраллю. Спіралеподібна форма молекули зберігається за рахунок виникнення водневих зв'язків між атомами водню і кисню в пептидній групі, які розміщуються між витками спіралі.
-спіраллю. Спіралеподібна форма молекули зберігається за рахунок виникнення водневих зв'язків між атомами водню і кисню в пептидній групі, які розміщуються між витками спіралі.
У свою чергу,  - спіраль може займати певне положення в просторі, яке визначає третинну структуру білка. На рис. 29.2 показаний фрагмент просторового розміщення спіралеподібної молекули одного з білків. Таке положення білкової молекули також пов'язане з наявністю водневих зв’язків. Білкові молекули, які мають певне просторове розміщення (третинну структуру), називають глобулами.
- спіраль може займати певне положення в просторі, яке визначає третинну структуру білка. На рис. 29.2 показаний фрагмент просторового розміщення спіралеподібної молекули одного з білків. Таке положення білкової молекули також пов'язане з наявністю водневих зв’язків. Білкові молекули, які мають певне просторове розміщення (третинну структуру), називають глобулами.
Під четвертинною структурою білка розуміють просторове розташування самих глобул.
Свою біологічну функцію білки виконують при умові, що зберігаються вторинна і третинна структури. Руйнування третинної і вторинної структур називається денатурацією білка. При денатурації зберігається тільки первинна структура білка, тобто пептидний ланцюг. Денатурацію білків може викликати дія хімічних речовин (кислот, лугів, спиртів, ацетону), нагрівання, підвищений тиск, радіоактивне опромінення.
Хімічні властивості. Важливою властивістю білків є здатність їх до гідролізу під дією кислот або біологічно активних речовин— ферментів. В результаті гідролізу руйнуються пептидні ланцюги білків і утворюється суміш  -амінокислот. Під час гідролізу протеїдів крім амінокислот утворюються і інші речовини.
-амінокислот. Під час гідролізу протеїдів крім амінокислот утворюються і інші речовини.
Для білків характерні кольорові реакції, за допомогою яких здійснюють якісний хімічний аналіз білків:
а) біуретова реакція — дія на білок розчину лугу і розчину сульфату міді (II), при цьому розчин набуває фіолетового забарвлення;
б) ксантопротеїнова реакція (для білків, що містять бензольні ядра)—дія концентрованої азотної кислоти з появою жовтого забарвлення. При добавлянні лугу жовте забарвлення змінюється на оранжеве;
в) цистеїнові реакція (для білків, що містять сірку) — кип'ятіння розчину білка з ацетатом свинцю (II) з появою чорного забарвлення;
г) реакція Меллона (для білків, що містять фрагменти фенолу) — кип'ятіння розчину білка з реактивом Меллона (розчином, який містить Нg(NО3)2 і НNО2) з появою червоного забарвлення;
д) реакція з нітропрусидом натрію (для білків, що містять групи —SН), з яким білки дають червоне забарвлення в аміачному середовищі.
Добування і застосування. Білки виділяють переважно з рослин і тварин. Ведуться роботи з штучного добування білкових речовин. Так, синтезовані білки інсулін і рибонуклеаза.
Білки є необхідним компонентом харчових продуктів. У процесі приготування їжі (кип'ятіння, смаження тощо) вони звичайно денатуруються: в такому вигляді вони легше перетравлюються. Білки, які людина вживає з їжею, зазнають гідролізу. Амінокислоти, що утворилися, йдуть на побудову білків організму.
Білки входять до складу багатьох лікарських препаратів.
Лекція №18
Тема: Нуклеїнові кислоти.
Мета: Вивчити будову нуклеїнових кислот, їх класифікацію та функції.
План:
1. Будова нуклеїнових кислот.
2. Біологічна роль нуклеїнових кислот.
3. Мономери та полінуклеїди.
Нуклеїнові кислоти - це складні високомолекулярні біополімери, мономерами яких є нуклеотиди. Молекула нуклеотиду складається із залишків нітратної основи, вуглеводу (пентози) і фосфорної кислоти.
Залежно від виду пентози, що входить до складу нуклеотиду, розрізняють два типи нуклеїнових кислот: дезоксирибонуклеїнову (ДНК) та рибонуклеїнову (РНК). До складу ДНК входить залишок дезоксирибози, а РНК - рибози.
У молекулах ДНК і РНК містяться залишки таких нітратних основ: аденіну (скорочено позначається літерою А), гуаніну (Г), цитозину (Ц). Крім того, до складу ДНК входить залишок тиміну (Т), а РНК - урацилу (У). До складу молекул ДНК та іРНК входять по чотири типи нуклеотидів, які відрізняються за типом нітратної кислоти.
Нуклеїновим кислотам, подібно до білків, притаманна первинна структура – певна послідовність розташування нуклеотидів, а також складніша просторова будова, яка формується за рахунок водневих зв’язків.
Окремі нуклеотиди сполучаються між собою у ланцюг за допомогою особливих «містків», які за участю залишків фосфорної кислоти виникають між залишками пентоз двох сусідніх нуклеотидів. Біологічні властивості нуклеїнових кислот визначаються співвідношенням і послідовністю розташування нуклеотидів у цьому ланцюзі.
Дата публикования: 2015-09-18; Прочитано: 1873 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
